ЭЛЕМЕНТЫ ТЕРМОХИМИИ
Термохимия – раздел химии, в котором рассматриваются тепловые явления, происходящие в процессе химических реакций.
Нужен репетитор по химии? Записывайтесь на занятия в каталоге TutorOnline!
Все химические реакции можно разделить на два типа: реакции, идущие с выделением теплоты, их называют экзотермические, и реакции, идущие с поглощением теплоты эндотермические. Критерием таких процессов является тепловой эффект реакции.
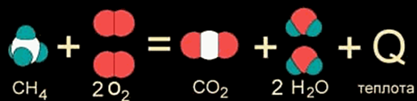
Как правило, к экзотермическим реакциям относятся реакции окисления, т.е. взаимодействия с кислородом, например сгорание метана
СН4 + 2O2 = СО2 + 2Н2О + Q (1)
а к эндотермическим реакциям – реакции разложения. Знак Q в конце уравнения указывает на то, выделяется ли теплота в процессе реакции (+ Q) или поглощается (- Q):
СаCO3 = СаO + CO2 -Q (2)
При химических процессах может выделяться или поглощаться не только тепловая, но и другие виды энергии: электрическая, световая, механическая и др.
Тепловые эффекты прямой и обратной реакций одинаковы по числу, но противоположны по знаку, например, оксид кальция (СаО) при взаимодействии с водой образует гидроксид кальция (Са(ОН)2). Процесс сопровождается выделением большого количества теплоты:
СаО + Н2О = Са(ОН) + 108 кДж (3)
А реакция разложения гидроксида кальция (Са(ОН)2) осуществляется с поглощением такого же количества теплоты извне
Са(ОН)2 = СаО + Н2О — 108 кДж (4)
Если тепловой эффект реакции определяется при постоянном давлении, температуре, то он будет соответствовать стандартной энтальпии реакции, обозначаемой ∆Н, которая противоположна по знаку величине теплового эффекта реакции. Например, если в процессе экзотермической реакции во взаимодействие вступают алюминий (Аl) и оксид железа (Fe2O3), то в конце уравнения это обозначится следующим образом:
2Аl + Fe2O3 = 2Fe + Al2O3 (+Q) или (-∆Н) (5)
А в случае эндотермической реакции значения этих тепловых величин будут иметь противоположные знаки:
С + СО2 = 2СО (-Q) или (+∆Н) (6)
Это объясняется тем, что выделяющаяся в процессе экзотермической реакции теплота как энергия, теряется системой (-∆Н), а при эндотермических процессах, наоборот – приобретается (+∆Н). Величина (Н) называется энтальпией системы. Часто её называют так же теплосодержанием или теплотой образования ∆Н данного вещества. В расчётах применяют справочные значения тепловых эффектов образования (или сгорания) одного моля вещества, отнесённые к 298К (250С) и Р = 101,325 кПа (1 атм). Эти условия считаются стандартными и поэтому используемые значения тепловых эффектов называют стандартными теплотами образования(или сгорания) вещества и обозначают как ∆Н0298. Например, тепловой эффект реакции взаимодействия графита с кислородом, выраженный через изменение энтальпии, следует записать как ∆Н0298 = — 393,6 кДж, а так как при этом из простых веществ образуется 1 моль СО2, то данный тепловой эффект является теплотой образования СО2, выраженной в кДж/моль. Главной характеристикой топлив являются их теплоты сгорания. Тепловой эффект реакции горения одного моля вещества называется теплотой сгорания данного вещества. Следовательно, исходя из вышеприведённых положений, теплота сгорания одного моля графита (12 г) составляет 393,6 кДж/моль.
Уравнение химической реакции, в котором указан тепловой эффект, называется термохимическим уравнением.
На практике это имеет большое значение. При строительстве тепловых трасс, доменных печей, котельных и т.п. теплотопотребляющих промышленных объектов, необходимо предусмотреть или приток энергии для поддержания процессов, или наоборот, отвод избытка теплоты, чтобы не было перегрева вплоть до взрыв
Расчёт теплового эффекта реакции между простыми веществами не предоставляется затруднительным. Например, для реакции образования хлористого водорода:
Н2 + Cl2 = 2НCl (7)
Энергия затрачивается на разрыв двух химических связей Н–Н и Cl — Cl. При этом энергия выделяется при образовании двух химических связей Н- Cl. Значения энергий этих связей можно найти в справочных таблицах и по разности между ними определить тепловой эффект (Q) реакции (7):
ЕН–Н = 436 кДж/моль, ЕCl–Cl = 240 кДж/моль,
ЕН–Cl = 240 кДж/моль,
Q = 2 х 430 — ( 1 х 436 — 1 х 240 ) = 184 кДж.
Приведённая в качестве примера термохимическая реакция (7) является экзотермической. Теплоты образования простых веществ при стандартных условиях приняты равными нулю.
Термохимические уравнения имеют особую форму записи. Они отличаются от обычных уравнений тем, что:
1). В термохимических уравнениях обязательно указывают агрегатные состояния веществ (жидкое, твёрдое, газообразное) Это связано с тем, что одна и та же реакция может иметь различный тепловой эффект в зависимости от фазового состояния вещества
2). Коэффициенты в термохимическом уравнении равны количеству веществ ( в молях), вступивших в реакцию. Например, дана реакция сгорания ацетилена:
2С2Н2(г) + 5О2(г) = 4СО2(г) + 2Н2О (+Q) (8)
При сгорании одного моль ацетилена С2Н2 выделяется 1257кДж теплоты. Поэтому, относительно одного моль С2Н2 необходимо все коэффициенты перед реагентами поделить на 2, тогда получим следующую запись термохимического уравнения:
С2Н2 + 5/2О2 = 2СО2 + Н2О + 1257 кДж (9)
Или другая тождественная запись:
С2Н2 + 2,5О2 = 2СО2 + Н2О + 1257 кДж (10)
Например, дано термохимическое уравнение сгорания метана:
СН4 + 2О2 = СО2 + 2Н2О + 802 кДж (11)
Необходимо вычислить, какое количество теплоты выделится при сгорании 20 г метана?
Поскольку 1 моль метана имеет массу 16 г, а 20 г метана соответственно составляют
n = m/Mr = 20:12 = 1,25 моль,
то, составив пропорцию: при сгорании
1 моль СН4 выделяется 802 кДж теплоты
1,25 СН4 ———«——-Х кДж теплоты
Определим, что на сгорание 20г метана потребуется
Х = 1,25 х 802 / 1 = 1002,5 кДж
Приведём другой пример . Дано уравнение реакции сгорания оксида азота(+4):
4NО2(г) + O2(г) + 2H2O(г) = 4НNО3(ж) + 448 кДж (12)
Необходимо составить термохимическое уравнение относительно сгорания одного моль оксида азота. Определить: какой объём оксида азота потребуется на образование 4258 кДж теплоты в процессе данной реакции?
Для составления термохимического уравнения относительно одного моль оксида азота(+4) необходимо все коэффициенты, стоящие перед реагентами, разделить на коэффициент, стоящий перед NО2, т.е. на «4», тогда уравнение примет вид:
NО2(г) + 1/4O2(г) + 1/2H2O(г) = НNО3(ж) +112 кДж (13)
В уравнении изменится количество выделяющейся теплоты, оно станет равным 112, т.е. в четыре раза меньше, чем в приведённом уравнении. В соответствии с уравнением (13) 1 моль оксида азота(NО2) или 22,4 л в данной реакции образует 112 кДж теплоты, а Х л соответственно 4258 кДж:
22,4 моль NО2 при сгорании образуют 112 кДж теплоты.
Х л —————-«————-4258 кДж теплоты.
Хг = 22,4 х 4258 / 112 = 851,6 кДж
Важнейшим законом термохимии является закон Г.И.Гесса (1840): тепловой эффект реакции зависит только от начального и конечного состояния веществ и не зависит от промежуточных стадий процесса. При помощи закона Гесса можно рассчитывать такие тепловые эффекты реакции, которые измерить трудно или невозможно. Например, теплоту образования угарного газа(СО) можно вычислить, если полное сгорание углерода
С (графит) + О2 = СО2 (∆Н1) (14)
разбить на стадии:
С (графит) + 0,5О2 = СО (∆Н2) (15)
СО + 0,5О2 = СО2 (∆Н3) (16)
Зная, что ∆Н1 = -393,6 кДж/моль и ∆Н3 = — 283,1 кДж/моль, из равенства ∆Н1 = ∆Н2 + ∆Н3
находим, что ∆Н2 = — 110,5 кДж/моль.
В качестве другого примера можно привести образование сульфата алюминия при сгорании алюминия и серы ромбической согласно реакции:
2Al(к) + 3S(ромб) + 6О2(г) = Al2(SO4)3(к) (17)
∆Н может быть найдена по тепловым эффектам отдельных стадий:
2Al + 1,5О2 = Al2O3 ∆Н1= -1670,2 кДж/моль (18)
3S + 1,5О2 = SO3 ∆Н2= -395,3 кДж/моль (19)
Al2O3 + 3SO3 = Al2(SO4)3 ∆Н3= -579,7 кДж/моль (20)
Тогда ∆Н = ∆Н1 + 3∆Н2 + ∆Н3 = (- 1670,2) – 3х (-395,3) – (579,7) = — 3435,8 кДж/моль.
На основании закона Гесса термохимические уравнения можно разбивать на отдельные стадии независимо от того, осуществимы они на практике или нет. Из закона Гесса вытекает важное следствие: тепловой эффект химической реакции равен сумме теплот образования получающихся веществ за вычетом суммы теплот образования исходный веществ:
∆Н = ∑ (𝘮 ∆Н) продукты — ∑ (𝘯 ∆Н) реагенты,
где 𝘮 и 𝘯 – число молей каждого вещества в уравнении реакции. Например, теплоту сгорания ацетилена (10) можно рассчитать, зная теплоты образования С2Н2 , СО2 и Н2О (∆Н002 = 0), как ∆Н0 = 2 ∆Н СО2 + ∆НН2О — ∆НС2Н2 = -2 х 393,6 — 281 — (+226,8) = -1295 кДж/моль.
НАЧАЛА ТЕРМОДИНАМИКИ
Среди многообразия химических реакций, термохимические занимают особое положение. Если рассуждать с точки зрения эволюции жизни на Земле, то в конечном итоге, действительно, от этих процессов зависит жизнь на нашей планете. А что касается человеческой цивилизации в целом, то здесь мы имеем прямую зависимость её развития от термохимических явлений. Ведь благодаря именно данным процессам произошёл отрыв человечества в развитии от всех других видов живых организмов, населяющих нашу планету. С древнейших времён, начиная от пассивного использования огня в качестве средства для согревания и приготовления примитивной пищи, человечество пришло к активному использованию этого явления (изготовление гончарных изделий – плавка меди, железа и других металлов – паровые двигатели – двигатели внутреннего сгорания – управление ядерными реакциями)
Если можно было бы предложить создать проект монумента человеческому прогрессу, то на его фронтоне надо было бы начертать уравнение химической реакции
С + О2 = СО2
Именно со сгорания дров, угля, торфа начался отсчёт человеческой цивилизации. В настоящее время наше с вами существование просто немыслимо без тепловых процесов. Но кроме приведённой выше реакции существует великое множество других термодинамических процессов. Почему именно углероду дано такое предпочтение? Может быть его собрату по IV-й группе – кремнию более выгоден данный процесс?
Si + О2 = SiО2
Тем более, что кремний по массе составляет 27,6% земной коры. Это несравненно больше, чем запасы древесины и её ископаемых на нашей планете. Чего же проще? Кидай в топку кремнезём! Его ведь целая планета! Правда надо оговорить тот факт, что чистого кремния в природе не существует. В наличии только его оксид — SiО2. Но на то и химики, чтобы придумать что-нибудь? А может быть для более сильного окислителя, чем кислород – фтору окисление углерода более выгодно термодинамически?
C + 2F2 = СF4
Как во всём этом разобраться? И возможно ли вообще предсказать осуществления того или иного процесса, ведь на бумаге можно написать уравнение любой химической реакции, а возможна ли она практически? Придётся начинать всё по порядку.
Одним из самых важных и очевидных законов природы является закон сохранения энергии: энергия не возникает из ничего и не исчезает бесследно, она только переходит из одной формы в другую. Аналогичным является закон сохранения массы вещества: массы веществ вступивших в реакцию равны массам веществ, образовавшихся в процессе данной реакции.
Поэтому и при экзотермической и при эндотермической обратимых реакциях одного и того же процесса как количество затрачиваемой и расходуемой энергии равны, но противоположны по знаку, так и массы веществ распадающихся и вновь образующихся равны:
СаО + Н2О = Са(ОН)2 + 108 кДж
Mr=56 Mr=18 Mr=74
Са(ОН)2 = СаО + Н2О — 108 кДж
Mr=74 Mr=56 Mr=18
Но всё дело в том, что в приведённых выше двух реакциях уже указано, какая из них экзотермическая, а какая эндотермическая. А можно ли так, как говорится «на вскидку» по одному только уравнению реакции определить: какая это реакция? В принципе, в большинстве случаев, возможно. К экзотермическим реакциям, в основном, относятся реакции соединения и как их разновидность – реакции окисления.(8,11,12,14). А к реакциям эндотермическим, соответственно – реакции разложения (2,4). Ещё раз уточним: в большинстве случаев. Поскольку реакция окисления:
0,5N2 + 0,5O2 = NО — 90 кДж
требует расхода энергии и является эндотермической, а реакция разложения нитрата натрия
2NaNO3 = 2NaNO2 + O2 (+Q)
осуществляется с выделением большого количества теплоты и является экзотермической.
Значит, принцип «на вскидку» не годится. Но каким же принципом тогда следует руководствоваться в определении реакций данного типа? В приводимых выше примерах (10), (14-20) указывалось, что стандартные теплоты образования веществ (∆Н) являются справочными данными. Такие данные скрупулёзно составлялись на протяжении десятилетий для многочисленных термодинамических реакций. С этой целью использовался прибор калориметр. Именно по этим данным в настоящее время мы можем установить, какой является та или иная реакция: экзотермической или эндотермической.
Теперь попробуем заглянуть как бы внутрь термохимической реакции. Как она начинается? Что способствует её осуществлению? В качестве примера приведём ещё раз две реакции (14) и (2):
С(графит) + О2 = СО2 + 393,3 кДж
СаСО3 = СаО + СО2 (-Q)
Представим себе, что химическими символами (С) и (О2) будут обозначаться не элемент «углерод» и простое вещество «кислород», а дрова (или уголь, торф) и воздух (атмосфера). А в качестве соединения СаСО3 — не карбонат кальция, а известное всем вещество: мел (или известняк). Первую реакцию будем проводить для того, чтобы нагреть печь и вскипятить чайник, а вторую – чтобы получить негашёную известь (СаО) в дальнейшем используемую для побелки садовых деревьев. Для разжигания печи приготовим щепки и, поместив сверху них дрова, зажжём огонь спичками.
Во втором случае, поместим в металлическое ведро мелко накрошенный мел, поставим на плиту и такими же действиями, как в случае разжигания огня в печи, разведём костёр под ведром.
Стоп! Тут что-то не так! Ведь мы установили, что первая реакция экзотермическая, протекает с выделением теплоты, а вторая реакция – эндотермическая, протекает с поглощением теплоты. А мы в обоих случаях разводим огонь, т.е. передаём этим процессам извне тепловую энергию. Значит, обе реакции эндотермические – идут с поглощением теплоты! Да, идут с поглощением теплоты, но это только на первом этапе. Некоторым экзотермическим реакциям требуется небольшой «толчок» — первоначальная подача энергии, а спустя некоторое время, когда загорятся дрова, процесс будет сопровождаться с выделением энергии в окружающую среду и во многие сотни, тысячи раз превзойдёт по величине первоначальное значение этой энергии. А второй процесс ка был так и останется эндотермическим. Ведь с прекращением подачи тепловой энергии мел перестанет разлагаться: реакция остановится. И всё-таки, почему в одних случаях процесс окисления (горения) является экзотермическим, а в других – эндотермическим процессом? И что является движущей силой эндотермических реакций, в ходе которых тепловая энергия поступает из окружающей среды? Ни у кого не вызывает удивление такое явление, как остывание со временем горячего чайника. Это нормально. А почему бы этому же чайнику, уже остывшему, холодному, взять, да и нагреться самому по себе? Вот это уже вызовет удивление.
Так вот, эта самая сила связана со стремлением любой системы к наиболее вероятному состоянию, характеризующимся максимальным беспорядком, называемым энтропией. Это одно из важнейших понятий в термодинамике. Энтропия обозначается символом «S». К примеру, при экзотермических реакциях, при проведении процессов плавления, кипения, переходов из жидкостей к газообразному состоянию, энтропия приобретает максимальное значение, поскольку при тепловых явлениях кинетическая энергия атомов, молекул, ионов возрастает, усиливаются беспорядочные колебания этих частиц. И наоборот, самый большой порядок в химических системах – в идеальном кристалле при температуре абсолютного нуля. Энтропия в данном случае равна нулю
Энтропия имеет численные значения, единицей её измерения является Дж/(моль . К); К примеру энтропия алмаза равна 2,4 Дж/(моль . К), пропана – 269,9 Дж/(моль . К). Энтропия газов значительно превышает энтропию жидких и тем более твёрдых тел. Поскольку в газообразных веществах постоянно происходит беспорядочное распределение молекул по всему объёму.
Существуют экспериментальные и теоретические методы определения энтропий различных химических соединений. Используя их, можно количественно рассчитать изменения энтропии при протекании конкретной реакции аналогично тому, как это делается для теплового эффекта реакции. Составлены специальные справочные данные, которые включают сравнительную характеристику этих величин с учётом температуры.
Подтянуть знания по химии можно записавшись на урок к онлайн-репетиторам TutorOnline
© blog.tutoronline.ru,
при полном или частичном копировании материала ссылка на первоисточник обязательна.
Тепловой эффект химической реакции. Термохимические уравнения. Расчеты теплового эффекта реакции.
Любая химическая реакция сопровождается выделением или поглощением энергии в виде теплоты.
По признаку выделения или поглощения теплоты различают экзотермические и эндотермические реакции.
Экзотермические реакции – такие реакции, в ходе которых тепло выделяется (+Q).
Эндотермические реакции – реакции, при протекании которых тепло поглощается (-Q).
Тепловым эффектом реакции (Q) называют количество теплоты, которое выделяется или поглощается при взаимодействии определенного количества исходных реагентов.
Термохимическим уравнением называют уравнение, в котором указан тепловой эффект химической реакции. Так, например, термохимическими являются уравнения:
Также следует отметить, что термохимические уравнения в обязательном порядке должны включать информацию об агрегатных состояниях реагентов и продуктов, поскольку от этого зависит значение теплового эффекта.
Расчеты теплового эффекта реакции
Пример типовой задачи на нахождение теплового эффекта реакции:
При взаимодействии 45 г глюкозы с избытком кислорода в соответствии с уравнением
C6H12O6(тв.) + 6O2(г) = 6CO2(г) + 6H2O(г) + Q
выделилось 700 кДж теплоты. Определите тепловой эффект реакции. (Запишите число с точностью до целых.)
Решение:
Рассчитаем количество вещества глюкозы:
n(C6H12O6) = m(C6H12O6) / M(C6H12O6) = 45 г / 180 г/моль = 0,25 моль
Т.е. при взаимодействии 0,25 моль глюкозы с кислородом выделяется 700 кДж теплоты. Из представленного в условии термохимического уравнения следует, что при взаимодействии 1 моль глюкозы с кислородом образуется количество теплоты, равное Q (тепловой эффект реакции). Тогда верна следующая пропорция:
0,25 моль глюкозы — 700 кДж
1 моль глюкозы — Q
Из этой пропорции следует соответствующее ей уравнение:
0,25 / 1 = 700 / Q
Решая которое, находим, что:
Q = 2800 кДж
Таким образом, тепловой эффект реакции составляет 2800 кДж.
Расчёты по термохимическим уравнениям
Намного чаще в заданиях ЕГЭ по термохимии значение теплового эффекта уже известно, т.к. в условии дается полное термохимическое уравнение.
Рассчитать в таком случае требуется либо количество теплоты, выделяющееся/поглощающееся при известном количестве реагента или продукта, либо же, наоборот, по известному значению теплоты требуется определить массу, объем или количество вещества какого-либо фигуранта реакции.
Пример 1
В соответствии с термохимическим уравнением реакции
3Fe3O4(тв.) + 8Al(тв.) = 9Fe(тв.) + 4Al2O3(тв.) + 3330 кДж
образовалось 68 г оксида алюминия. Какое количество теплоты при этом выделилось? (Запишите число с точностью до целых.)
Решение
Рассчитаем количество вещества оксида алюминия:
n(Al2O3) = m(Al2O3) / M(Al2O3) = 68 г / 102 г/моль = 0,667 моль
В соответствии с термохимическим уравнением реакции при образовании 4 моль оксида алюминия выделяется 3330 кДж. В нашем же случае образуется 0,6667 моль оксида алюминия. Обозначив количество теплоты, выделившейся при этом, через x кДж составим пропорцию:
4 моль Al2O3 — 3330 кДж
0,667 моль Al2O3 — x кДж
Данной пропорции соответствует уравнение:
4 / 0,667 = 3330 / x
Решая которое, находим, что x = 555 кДж
Т.е. при образовании 68 г оксида алюминия в соответствии с термохимическим уравнением в условии выделяется 555 кДж теплоты.
Пример 2
В результате реакции, термохимическое уравнение которой
4FeS2(тв.) + 11O2(г) = 8SO2(г) + 2Fe2O3(тв.) + 3310 кДж
выделилось 1655 кДж теплоты. Определите объем (л) выделившегося диоксида серы (н.у.). (Запишите число с точностью до целых.)
Решение
В соответствии с термохимическим уравнением реакции при образовании 8 моль SO2 выделяется 3310 кДж теплоты. В нашем же случае выделилось 1655 кДж теплоты. Пусть количество вещества SO2, образовавшегося при этом, равняется x моль. Тогда справедливой является следующая пропорция:
8 моль SO2 — 3310 кДж
x моль SO2 — 1655 кДж
Из которой следует уравнение:
8 / х = 3310 / 1655
Решая которое, находим, что:
x = 4 моль
Таким образом, количество вещества SO2, образовавшееся при этом, составляет 4 моль. Следовательно, его объем равен:
V(SO2) = Vm ∙ n(SO2) = 22,4 л/моль ∙ 4 моль = 89,6 л ≈ 90 л (округляем до целых, т.к. это требуется в условии.)
Больше разобранных задач на тепловой эффект химической реакции можно найти здесь.
Вычислить тепловой эффект реакции важно для того, чтобы правильно организовать многие процессы на промышленных производствах. Это необходимо там, где используется подача энергии или где, наоборот, требуется ее отведение. Поскольку одни виды энергии могут превращаться в другие, то применение теплового эффекта химического взаимодействия позволяет превратить внутреннюю энергию веществ в работу (механическую, электрическую и т.д.).
С выделением или поглощением тепла идут процессы в живых организмах. Точный расчет тепловых эффектов превращения белков, жиров, углеводов и других веществ позволяет организовать правильную диету спортсменам, людям с теми или иными заболеваниями.
Содержание:
1. Что такое тепловой эффект химической реакции
2. Как вычислить тепловой эффект реакции и составить термохимическое уравнение
3. Расчеты по термохимическим уравнениям
Что такое тепловой эффект химической реакции
Химические реакции практически всегда сопровождаются какими-либо тепловыми явлениями.
Так, горение, нейтрализация кислоты щелочью, реакция металла (например, магния) с хлором и т.д. происходят с выделением достаточного количества тепла. А вот, чтобы разложить мел (карбонат кальция), необходимо все время его нагревать. Если нагревание (то есть подвод тепла) прекратить, то и реакция тоже прекратится. Это говорит о том, что разложение карбоната кальция идет с поглощением тепла.
В чем же дело? Любое вещество является продуктом взаимодействия частиц (атомов или ионов). В ходе образования вещества энергия взаимодействия как бы прячется в химических связях (ковалентных, ионных). Это так называемая внутренняя энергия, которая частично высвобождается в ходе химического взаимодействия. Она же – тепловой эффект реакции. Измеряя его, можно судить о том, как изменилась внутренняя энергия вещества.
Тепловой эффект химической реакции обозначают буквой Q и измеряют в кДж (или в ккал в случае, когда речь идет об обеспечении энергией живых организмов).
Если в результате химического взаимодействия теплота выделяется, то это экзотермические реакции (+Q); если теплота поглощается – эндотермические (-Q).
Как вычислить тепловой эффект реакции и
составить термохимическое уравнение
Взаимодействие веществ принято отражать (записывать) с помощью химического уравнения. Если в таком уравнении указан тепловой эффект, то тогда уравнение будет называться термохимическим.
Например, обычное уравнение реакции:
А это уже термохимическое уравнение данной реакции:
Уравнение говорит о том, что при взаимодействии 1 моля PbO с 1 молем СО, идущем с образованием 1 моля Pb и 1 моля CO2, выделяется 64 кДж теплоты.
Особенности термохимических уравнений:
1) указывается агрегатное состояние веществ (однако, если все вещества находятся в одном агрегатном состоянии, то его могут не указывать);
2) указывается тепловой эффект реакции в соответствии с ее стехиометрией (то есть, в соответствии с правильно расставленными коэффициентами);
3) тепловой эффект записывается в левой части уравнения;
4) если речь идет о горении вещества, то уравнение составляется по отношению к 1 молю этого вещества; тепловой эффект такой реакции называется теплотой сгорания:
5) если речь идет об образовании вещества, то уравнение также составляется по отношению к 1 молю этого вещества; тепловой эффект такой реакции будет называться теплотой образования:
А теперь разберем несколько задач, требованием которых является составление термохимического уравнения.
Что нужно сделать для решения таких задач?
1) записать условие задачи;
2) составить уравнение реакции;
3) вычислить ее тепловой эффект;
4) записать полученное значение теплового эффекта в уравнение реакции.
Пример 1. Кальций массой 8 г сгорает с выделением 127 кДж теплоты. Напишите термохимическое уравнение (тху) реакции.
Пример 2. При разложении 6,86 г оксида ртути (II) тратится 3,64 кДж тепловой энергии. Напишите термохимическое уравнение (тху) реакции.
Пример 3. Реакция 6 г углерода с водородом приводит к выделению 37,42 кДж теплоты. Напишите термохимическое уравнение (тху) реакции образования метана.
Расчеты по термохимическим уравнениям
В термохимических расчетах чаще используются уже готовые термохимические уравнения. Требуется найти массы/объемы образующихся/исходных веществ, количество выделившейся/поглощенной теплоты.
Рассмотрим несколько примеров.
Пример 4. По термохимическому уравнению: N2(г.) + O2(г.) = 2NO(г.) – 180,7 кДж вычислите тепловой эффект реакции, в которой участвует азот объемом 5,6 л (при н.у.).
Поскольку реакция эндотермическая, то поглотится 45,2 кДж энергии.
Пример 5. Тепловой эффект реакции горения этилена составляет 1400 кДж (в расчете на 1 моль этилена). Сколько этилена (при н.у.) необходимо сжечь, чтобы получить 560 кДж теплоты?
Пример 6. Пользуясь термохимическим уравнением сгорания пропана
C3H8 + 5O2 = 3CO2 + 4H2O + 2220,03 кДж,
определите количество выделившейся теплоты, если в реакцию вступит кислород: а) массой 16 г; б) объемом 67,2 л; в) количеством вещества 2,5 моль. Сколько оксида углерода (IV) по объему и по массе получится, если при горении пропана выделится 277,5 кДж теплоты?
Если вы готовитесь к выпускному экзамену (ЕГЭ по химии), то имейте ввиду, что вычислить тепловой эффект реакции требует задание № 27 (версия 2022 года).
Чтобы самыми первыми узнавать о новых публикациях на сайте, присоединяйтесь к нашей группе ВКонтакте.
Лекция 6. Термохимия. Тепловой эффект химической реакции
Подобно тому, как одной из физических характеристик человека является физическая сила, важнейшей характеристикой любой химической связи является сила связи, т.е. её энергия.
Напомним, что энергия химической связи – эта та энергия, которая выделяется при образовании химической связи или та энергия, которую нужно истратить, чтобы эту связь разрушить.
Химическая реакция в общем случае – это превращение одних веществ в другие. Следовательно, в ходе химической реакции происходит разрыв одних связей и образование других, т.е. превращения энергии.
Фундаментальный закон физики гласит, что энергия не возникает из ничего и не исчезает бесследно, а лишь переходит из одного вида в другой. В силу своей универсальности данный принцип, очевидно, применим и к химической реакции.
Тепловым эффектом химической реакции называется количество теплоты,
выделившееся (или поглотившееся) в ходе реакции и относимое к 1 моль прореагировавшего (или образовавшегося) вещества.
Тепловой эффект обозначается буквой Q и, как правило, измеряется в кДж/моль или в ккал/моль.
Если реакция происходит с выделением тепла (Q > 0), она называется экзотермической, а если с поглощением тепла (Q < 0) – эндотермической.
Если схематично изобразить энергетический профиль реакции, то для эндотермических реакций продукты находятся выше по энергии, чем реагенты, а для экзотермических – наоборот, продукты реакции располагаются ниже по энергии (более стабильны), чем реагенты.
Ясно, что чем больше вещества прореагирует, тем большее количество энергии выделится (или поглотится), т.е. тепловой эффект прямо пропорционален количеству вещества. Поэтому отнесение теплового эффекта к 1 моль вещества обусловлено нашим стремлением сравнивать между собой тепловые эффекты различных реакций.

Лекция 6. Термохимия. Тепловой эффект химической реакции Пример 1. При восстановлении 8,0 г оксида меди(II) водородом образовалась металлическая медь и пары воды и выделилось 7,9 кДж теплоты. Вычислите тепловой эффект реакции восстановления оксида меди(II).
Решение. Уравнение реакции CuO (тв.) + H2 (г.) = Cu (тв.) + H2O (г.) + Q (*)
|
В реакцию вступило ν = |
m |
= |
8,0 |
= 0,1мольоксида меди(II). |
|
M |
63,5 +16 |
Составим пропорцию при восстановлении 0,1 моль – выделяется 7,9 кДж при восстановлении 1 моль – выделяется x кДж
Откуда x = + 79 кДж/моль. Уравнение (*) принимает вид
CuO (тв.) + H2 (г.) = Cu (тв.) + H2O (г.) + 79 кДж
Термохимическое уравнение – это уравнение химической реакции, в котором указаны агрегатное состояние компонентов реакционной смеси (реагентов и продуктов) и тепловой эффект реакции.
|
Изменение агрегатного состояния вещества также обычно |
сопряжено |
|
с тепловыми эффектами. Наиболее известные Вам примеры |
связаны с |
|
изменением агрегатного состояния воды. |
Так, чтобы расплавить лед или испарить воду, требуется затратить определенные количества теплоты, тогда как при замерзании жидкой воды или конденсации водяного пара такие же количества теплоты выделяются. Именно поэтому нам холодно, когда мы выходим из воды (испарение воды с поверхности тела требует затрат энергии), а потоотделение является биологическим защитным механизмом от перегрева организма. Напротив, морозильник замораживает воду и нагревает окружающее помещение, отдавая ему избыточное тепло.
На данном примере показаны тепловые эффекты изменения агрегатного состояния воды. Теплота плавления (при 0oC) λ = 3,34×10 5 Дж/кг (физика), или Qпл. = — 6,02 кДж/моль (химия), теплота испарения (парообразования) (при 100oC) q = 2,26×10 6 Дж/кг (физика) или Qисп. = — 40,68 кДж/моль (химия).
|
кристаллизация |
конденсация |
|
Q > 0 |
Q > 0 |
|
H2O |
H2O |
||||
|
испарение |
|||||
|
ж. |
г. |
||||
|
Q < 0 |
|||||
обр,298.
Лекция 6. Термохимия. Тепловой эффект химической реакции Разумеется, возможны процессы сублимации, когда твердое вещество
переходит в газовую фазу, минуя жидкое состояние и обратные процессы осаждения (кристаллизации) из газовой фазы, для них также возможно рассчитать или измерить тепловой эффект.
Ясно, что в каждом веществе есть химические связи, следовательно, каждое вещество обладает некоторым запасом энергии. Однако далеко не все вещества можно превратить друг в друга одной химической реакцией. Поэтому договорились о введении стандартного состояния.
Стандартное состояние вещества – это агрегатное состояние вещества при температуре 298 К, давлении 1 атмосфера в наиболее устойчивой в этих условиях аллотропной модицикации.
Стандартные условия – это температура 298 К и давление 1 атмосфера. Стандартные условия (стандартное состояние) обозначается индексом0.
Стандартной теплотой образования соединения называется тепловой эффект химической реакции образования данного соединения из простых веществ, взятых в их стандартном состоянии. Теплота образования соединения обозначается символом Q0 Для множества соединений стандартные теплоты образования приведены в справочниках физикохимических величин.
Стандартные теплоты образования простых веществ равны 0. Например, Q0обр,298 (O2, газ) = 0, Q0обр,298 (C, тв., графит) = 0.
Например. Запишите термохимическое уравнение образования сульфата меди(II). Из справочника Q0обр,298 (CuSO4) = 770 кДж/моль.
Cu (тв.) + S (тв.) + 2O2 (г.) = CuSO4 (тв.) + 770 кДж.
Замечание: термохимическое уравнение можно записать для любого вещества, однако надо понимать, что в настоящей жизни реакция происходит совершенно по-другому: из перечисленных реагентов образуются при нагревании оксиды меди(II) и серы(IV), но сульфат меди(II) не образуется. Важный вывод: термохимическое уравнение – модель, которая позволяет производить расчеты, она хорошо согласуется с другими термохимическими данными, но не выдерживает проверки практикой (т.е. неспособна правильно предсказать возможность или невозможность реакции).
(B j ) —∑ai ×Qобр0 ,298 i
Лекция 6. Термохимия. Тепловой эффект химической реакции
Уточнение. Для того, чтобы не вводить Вас в заблуждение, сразу добавлю, что химическая термодинамика может предсказывать возможность / невозможность реакции, однако для этого требуются более серьезные «инструменты», которые выходят за рамки школьного курса химии. Термохимическое уравнение по сравнению с этими приемами – первая ступенька на фоне пирамиды Хеопса – без него не обойтись, но высоко не подняться.
Пример 2. Вычислите тепловой эффект конденсации воды массой 5,8г. Решение. Процесс конденсации описывается термохимическим уравнением H2O (г.) = H2O (ж.) + Q – конденсация обычно экзотермический процесс Теплота конденсации воды при 25oC 37 кДж/моль (справочник).
|
Количество вещества ν = |
m |
= |
5,8 |
= 0,32 моль |
|
M |
||||
|
18 |
Следовательно, Q = 37 × 0,32 = 11,84 кДж.
В 19 веке русским химиком Гессом, изучавшим тепловые эффекты реакций, был экспериментально установлен закон сохранения энергии применительно к химическим реакциям – закон Гесса.
Тепловой эффект химической реакции не зависит от пути процесса и определяется только разностью конечного и начального состояний.
С точки зрения химии и математики данный закон означает, что мы вольны для расчета процесса выбрать любую «траекторию расчета», ведь результат от нее не зависит. По этой причине очень важный закон Гесса имеет невероятно важное следствие закона Гесса.
Тепловой эффект химической реакции равен сумме теплот образования продуктов реакции за вычетом суммы теплот образования реагентов (с учетом стехиометрических коэффициентов).
С точки зрения здравого смысла данное следствие соответствует процессу, в котором сначала все реагенты превратились в простые вещества, которые затем собрались по-новому, так что получились продукты реакции.
В форме уравнения следствие закона Гесса выглядит так Уравнение реакции: a1A1 + a2A2 + … + a nAn = b1B1 + b2B2 + … b
При этом ai и bj – стехиометрические коэффициенты, Ai – реагенты, Bj – продукты реакции.
Тогда следствие закона Гесса имеет вид Q = ∑b j ×Qобр0 ,298
j
Лекция 6. Термохимия. Тепловой эффект химической реакции Поскольку стандартные теплоты образования многих веществ
а) сведены в специальные таблицы или б) могут быть определены экспериментально, то становится возможным предсказать (рассчитать) тепловой эффект очень большого количества реакций с достаточно высокой точностью.
Пример 3. (Следствие закона Гесса). Рассчитайте тепловой эффект паровой конверсии метана, происходящей в газовой фазе при стандартных условиях:
CH4 (г.) + H2O (г.) = CO (г.) + 3 H2 (г.)
Определите, является ли данная реакция экзотермической или эндотермической?
Решение: Следствие закона Гесса
|
Q = 3Q0 |
(H |
, г) +Q0 |
(CO, г) −Q0 |
(CH |
, г) −Q0 |
(H |
O, г) — в общем виде. |
||
|
обр,298 |
2 |
обр,298 |
обр,298 |
4 |
обр,298 |
2 |
|||
|
Qобр0 |
,298 (H 2 , г) = 0 |
— простое вещество в стандартном состоянии |
Из справочника находим теплоты образования остальных компонентов смеси.
|
Q 0 |
(H |
O, г) = 241,8 |
кДж |
, Q0 |
(СO, г) = 110,5 |
кДж |
, Q 0 |
(CH |
, г) = 74,6 |
кДж |
. |
|
обр,298 |
2 |
моль |
обр,298 |
моль |
обр,298 |
4 |
моль |
||||
Подставляем значения в уравнение
Q = 0 + 110,5 – 74,6 – 241,8 = -205,9 кДж/моль, реакция сильно эндотермична.
Ответ: Q = -205,9 кДж/моль, эндотермическая
Пример 4. (Применение закона Гесса). Известны теплоты реакций
C (тв.) + ½ O (г.)= CO (г.) + 110,5 кДж
2
С (тв.) + O2 (г.) = CO2 (г.) + 393,5 кДж Найти тепловой эффект реакции 2CO (г.) + O2 (г.) = 2CO2 (г.). Решение Умножим первое и второе уравнение на 2
2C (тв.) + O2 (г.)= 2CO (г.) + 221 кДж 2С (тв.) + 2O2 (г.) = 2CO2 (г.) + 787 кДж
Вычтем из второго уравнения первое
O2 (г.) = 2CO2 (г.) + 787 кДж – 2CO ( г.) – 221 кДж,
откуда
2CO (г.) + O2 (г.) = 2CO2 (г.) + 566 кДж Ответ: 566 кДж/моль.
Замечание: При изучении термохимии мы рассматриваем химическую реакцию извне (снаружи). Напротив, химическая термодинамика – наука о поведении химических систем – рассматривает систему изнутри и оперирует понятием «энтальпии» H как тепловой энергии системы. Энтальпия, таким
Лекция 6. Термохимия. Тепловой эффект химической реакции образом, имеет тот же смысл, что и количество теплоты, но имеет противоположный знак: если энергия выделяется из системы, окружающая среда её получает и греется, а система энергию теряет.
Литература:
1. учебник, В.В. Еремин, Н.Е. Кузьменко и др., Химия 9 класс, параграф 19,
с. 96-100.
2. Учебно-методическое пособие «Основы общей химии» Часть 1.
Составители – С.Г. Барам, И.Н. Миронова. – взять с собой! на следующее семинарское занятие
3. А.В. Мануйлов. Основы химии. http://hemi.nsu.ru/index.htm
§9.1 Тепловой эффект химической реакции. Основные законы термохимии.
§9.2** Термохимия (продолжение). Теплота образования вещества из элементов.
Стандартная энтальпия образования.
Внимание!
Мы переходим к решению расчетных задач, поэтому на семинары по химии отныне и впредь желателен калькулятор.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Что такое тепловой эффект химической реакции
В процессе химических реакций может выделяться или поглощаться тепло.
Определение
Экзотермическими реакциями называют процессы, в результате которых выделяется теплота, обозначаемая параметром «+».
Эндотермическими реакциями являются нормальные процессы, сопровождающиеся поглощением теплоты. В этом случае теплота Q обозначается со знаком «-».
Осторожно! Если преподаватель обнаружит плагиат в работе, не избежать крупных проблем (вплоть до отчисления). Если нет возможности написать самому, закажите тут.
Определение
Тепловым эффектом химической реакции называют изменение внутренней энергии системы, что является результатом химической реакции и трансформации исходных веществ или реагентов в продукты реакции в количествах, которые соответствуют формуле химической реакции.
Химические реакции сопровождаются некоторыми численными закономерностями. С их помощью можно определить знак, которому соответствует тепловой эффект. К данным закономерностям относят:
- Экзотермические реакции, протекающие самопроизвольно, запускаются с помощью инициации, включая нагрев и другие действия. Примером таких процессов является произвольное горение угля после поджига: (C+O_{2} = CO_{2} + Q)
- Устойчивые вещества образуются из простых веществ в результате экзотермических реакций, а реакции разложения обычно являются эндотермическими. Примером является распад нитрата калия, сопровождающийся поглощением тепла: (2KNO_{3}rightarrow 2KNO_{2} + O_{2}-Q)
- Более устойчивые вещества образуются из менее устойчивых, как правило, в процессе экзотермических реакций. Справедливо и обратное утверждение: более устойчивые вещества образуются из менее устойчивых, тепло при этом поглощается. Устойчивость определяют приблизительно, исходя из активности и стабильности вещества в обычных условиях. В привычном мире нас окружают в большинстве своем относительно устойчивые вещества. В качестве примера можно рассмотреть процесс горения аммиака, при котором активные неустойчивые вещества взаимодействуют между собой, что сопровождается образованием устойчивых веществ, а именно, азота и воды. Экзотермическая реакция будет записана в таком виде: (4NH_{2} + 3O_{2} rightarrow 2N_{2} + 6H_{2}O + Q)
Обозначить количество теплоты можно буквой Q. Величина измеряется в кДж (килоджоули) или Дж (джоули). Теплота, которая выделяется во время реакции, пропорциональна количеству вещества, с помощью которого запущена реакция.
Температурная зависимость теплового эффекта (энтальпии) реакции
Понятие стандартной теплоты образования используют для обозначения теплового эффекта реакции, при которой образуются один моль вещества из простых веществ, его составляющие, характеризующиеся устойчивыми стандартными состояниями. К примеру, стандартной энтальпией образования 1 моля метана из углерода и водорода является тепловой эффект реакции:
(C+2H_{2}=CH_{4}+74,9) кДж/моль
Обозначением стандартной энтальпии образования является (Delta H^{0}_{f})
Примечание
В данном случае индексом f выражают formation или образование. Верхний индекс О служит для указания соответствия величины стандартному состоянию вещества, то есть один моль индивидуального химического соединения, имеющего чистый вид, при стандартизированных условиях в таком агрегатном состоянии, которое отличается устойчивостью в этих условиях.
Энтальпия образования простых веществ имеет нулевое значение. При этом данное условие соответствует агрегатному состоянию, сохраняющему стабильность при температуре 298.15 К.
Пример
К примеру, йод в кристаллическом виде обладает стандартной энтальпией образования (Delta H^{0}(I_{2})=0) кДж/моль. В жидком состоянии показатель йода изменится таким образом:
(Delta H^{0}(I_{2})=22) кДж/моль.
Энтальпии образования простых веществ в стандартных условиях представляют собой их основные энергетические характеристики.
Тепловой эффект какой-либо реакции рассчитывают, как параметр, равный разнице суммы теплоты образования всех продуктов и суммы теплоты образования всех реагентов в этой реакции, согласно закону Гесса.
Формула выглядит следующим образом:
(Delta H_{R}^{0}=sum{Delta H^{0}_{f}}_{p}-sum{Delta H^{0}_{f}}_{r})
Термохимические эффекты включают в химические реакции.
Определение
Термохимическими уравнениями являются химическими уравнениями с указанием количества теплоты, которая выделилась или была поглощена.
Если реакция сопровождается выделением теплоты во внешнюю среду, и тепловой эффект характеризуется отрицательным значением, то такая реакция относится к экзотермическому типу. При наблюдении положительного теплового эффекта и поглощения тепла реакции называют эндотермическими. Тепловой эффект, как правило, относится к одному молю прореагировавшего исходного вещества с максимальным стехиометрическим коэффициентом.
При известных мольных теплоемкостях веществ, которые участвуют в реакции, можно определить, какова температурная зависимость энтальпии реакции. Если температура от Т1 до Т2 увеличивается, то изменение энтальпии реакции необходимо рассчитывать, согласно закону Кирхгофа. При этом данный интервал температур не предполагает зависимость от температуры, а фазовые превращения отсутствуют. Уравнение имеет следующий вид:
(Delta H(T_{2})=Delta H(T_{1})+int_{1}^{2}{Delta C_{p}(T_{1},T_{2})d(T)})
При наблюдении фазовых превращений в данном температурном интервале, расчет выполняют с учетом теплоты соответствующих превращений и изменения температурной зависимости теплоемкости веществ, подвергшимся таким превращениям:
(Delta H(T_{2})=Delta H(T_{1})+int_{1}^{T_{varphi }}{Delta C_{p}(T_{1},T_{varphi })d(T)}+int_{T_{varphi }}^{2}{Delta C_{p}(T_{varphi },T_{2})d(T)})
где (Delta C_{p}(T_{1},T_{varphi })) является изменением теплоемкости в температурном интервале от Т1 до фазового перехода, (Delta C_{p}(T_{varphi },T_{2})) представляет изменение теплоемкости в температурном интервале от фазового перехода до конечных показателей, (T_{varphi }) является температурой фазового перехода.
Закон Кирхгофа для теплового эффекта, уравнение
Определение
Закон Кирхгофа: температурный коэффициент теплового эффекта химической реакции определен изменением теплоемкостью системы в процессе реакции.
С помощью уравнения Кирхгофа, которое вытекает из вышеизложенной закономерности, выполняют расчет теплового эффекта при разных температурных показателях. В дифференциальной форме закон записан таким образом:
(left(frac{d(Delta _{r}H)}{dT} right)_{p}=Delta _{r}C_{p})
(left(frac{d(Delta _{r}U)}{dT} right)_{V}=Delta _{r}C_{V})
В форме интеграла закон Кирхгофа обладает следующим видом:
(Delta _{r}H_{T_{2}}=Delta H_{T_{1}}+int_{T_{1}}^{T_{2}}{Delta _{r}C_{p}(T)dT})
(Delta _{r}U_{T_{2}}=Delta U_{T_{1}}+int_{T_{1}}^{T_{2}}{Delta _{r}C_{V}(T)dT})
где (C_{p}) и (C_{V}) являются изобарной и изохорной теплоемкостью; (Delta _{r}C_{V}) представляет собой разницу изохорных теплоемкостей продуктов реакции и исходных веществ; (Delta _{r}C_{p}) — разность изобарных теплоёмкостей продуктов реакции и исходных веществ; соответствующими тепловыми эффектами являются (Delta _{r}H) и (Delta _{r}U.)
Если разность Т2-Т1 не отличается большими значениями, то (Delta _{r}C_{p}=const) и (Delta _{r}C_{V}=const)
В этом случае интегральная форма уравнения будет записана в таком виде:
(Delta _{r}H_{T_{2}}=Delta H_{T_{1}}+Delta _{r}C_{p}(T_{2}-T_{1}))
(Delta _{r}U_{T_{2}}=Delta U_{T_{1}}+Delta _{r}C_{V}(T_{2}-T_{1}))
Если разница между температурами достаточно большая, то требуется учитывать такие температурные зависимости теплоемкостей:
(Delta _{r}C_{p}=f(T))
(Delta _{r}C_{V}=f(T))
Термохимическое уравнение, как делать расчеты
При решении задач по термохимии использую термохимические уравнения. В данных формулах записывают реакции с количеством тепла, которое выделилось в процессе реакции на число моль вещества в соответствии с коэффициентами в уравнении.
В качестве примера можно рассмотреть термохимическое уравнение, соответствующее процессу сгорания водорода:
(2H_{2}+O_{2}=2H_{2}O+ 484) кДж,
Данная формула демонстрирует высвобождение 484 кДж тепла в процессе сгорания 2 моль водорода, 1 моль кислорода. Следует отметить образование 2 моль воды, что сопровождается выделение 484 кДж тепла.
Определение
Теплотой образования вещества называют количество теплоты, которое выделяется при формировании 1 моль данного вещества из простых веществ.
Наглядным примером является процесс сгорания алюминия, представить который можно таким образом:
(2Al+frac{3}{2}O_{2} rightarrow Al_{2}O_{3}+1675) кДж
Теплота, которая выделяется при образовании оксида алюминия, составляет 1675 кДж/моль. Записать термохимическую формулу, исключая дробные коэффициенты, можно в таком виде:
(4Al+3O_{2} rightarrow 2Al2O_{3} + 3350) кДж
Теплота, которая характерна для образования оксида алюминия, составит 1675 кДж/моль. Это объясняется с помощью теплового эффекта образования 2 моль оксида алюминия, который учтен в термохимическом уравнении.
Определение
Теплотой сгорания вещества называют количество тепла, которое выделяется в процессе горения 1 моль данного вещества.
Примером такого явления служит горение метана:
(CH_{4} + 2O_{2} rightarrow CO_{2} + 2H_{2}O + 802) кДж
В этом случае теплота сгорания метана составит 802 кДж/моль.
Примеры решения задач
Задача 1
По итогу реакции, термическая формула которой записана таким образом:
(N_{2}+O_{2}rightarrow2NO-180)
образовано 98 л (н.у.) оксида азота (II). Требуется определить количество теплоты, затраченное на эту реакцию в кДж. Искомое значение можно записать с точностью до целых.
Решение
Согласно термическому уравнению, для образования 2 моль оксида азота (II) необходимо затратить 180 кДж тепла. 2 моль оксида азота при н.у. в объеме составляют 44.8 л. Для поиска решения целесообразно воспользоваться простой пропорцией:
- получить 44,8 л оксида азота (II) можно с помощью 180 кДж тепла;
- для образования 98 л оксида азота требуется х кДж теплоты.
Таким образом:
х = 180 * 98 / 44.8 = 393.75 кДж.
Если округлить значение до целых, то Q = 394 кДж.
Ответ: количество теплоты, которое потратили на реакцию, составляет 394 кДж.
Задача 2
По итогам реакции, термохимическая формула которой имеет вид:
(2H_{2}+O_{2}=2H_{2}O+ 484) кДж
было высвобождено 1452 кДж тепла. Требуется найти массу выделившейся в процессе реакции воды в граммах. Запись числа рекомендуется округлить до целых.
Решение
Согласно термохимическому уравнению, в процессе образования 2 моль воды будет образовано 484 кДж тепла. Масса 2 моль воды составляет 36 грамм. Простая пропорция:
- во время формирования 36 грамм воды будет выделено 484 кДж тепла;
- в процессе образования х грамм воды высвободится 1452 кДж теплоты.
В таком случае:
х = 1452 * 36 / 484 = 108 г.
(m(H_{2}O)=108) г.
Ответ: в процессе реакции будет выделено 108 грамм воды.
Задача 3
Во время реакции, которая характеризуется следующим термохимическим уравнением:
(S+O_{2}=SO_{2}+ 296) кДж
было затрачено 80 грамм серы. Требуется рассчитать количество теплоты, выделяющееся во время реакции в кДж. Конечный результат допускается округлить до целых.
Решение
Исходя из термохимического уравнения, в процессе сгорания 1 моль серы будет выделено 296 кДж теплоты. Масса 1 моль серы составляет 32 грамма. Для расчетов можно записать простую пропорцию:
- сгорание 32 грамм серы сопровождается выделением 296 кДж теплоты;
- сгорание 80 грамм серы сопровождается выделением х кДж теплоты.
Таким образом:
х = 80 * 296 / 32 = 740 кДж
Q = 740 кДж.
Ответ: во время химической реакции будет образовано 740 кДж теплоты.