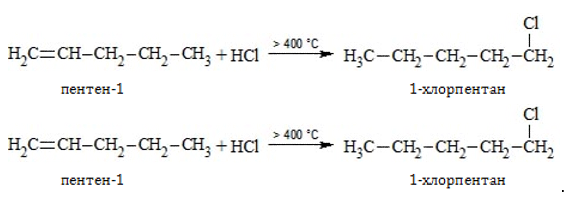Изомеры пентена
Содержание
- 1 Строение пентена
- 2 Изомерия пентена
- 2.1 Структурные изомеры
- 2.2 Пространственные изомеры
- 3 Физические свойства
- 4 Химические свойства
- 5 Получение пентенов
- 6 Применение пентенов
Пентен – ненасыщенный углеводород ациклического строения, четвертый член гомологического ряда алкенов. Пентен содержится в продуктах нефтепереработки. Вследствие структурных и геометрических отличий в строении молекул одинакового состава пентену присуще свойство изомерии. Изомеры пентена находят применение в производстве топлива и в органическом синтезе.
Строение пентена
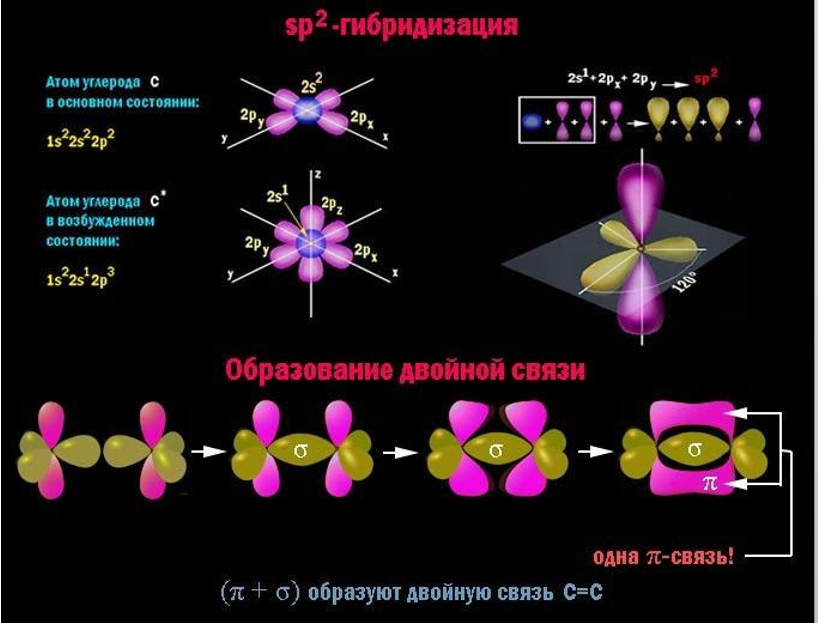
Химическая формула пентена – . До полного насыщения валентностей углерода молекуле пентена не хватает двух атомов водорода. Гибридизация орбиталей у двух из пяти углеродных атомов принадлежит к типу
, то есть затрагивает не все валентные электроны.
Гибридные электронные облака, расположенные в одной плоскости с центрами взаимодействующих атомов, вступают в прочную -связь.
-орбитали этих атомов остаются негибридными и путем бокового перекрывания образуют
-связь, которая менее устойчива, так как находится вне оси, соединяющей атомные ядра.
Сочетание представляет собой двойную связь
, на которую углеродные атомы затрачивают по две свободных валентности из четырех. Поэтому пентен, подобно всем углеводородам ряда алкенов, имеет в молекуле на два водородных атома меньше, чем соответствующие предельные соединения – алканы.
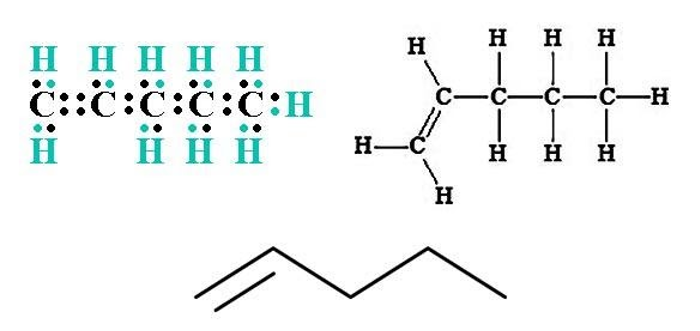
Электронная, структурная и скелетная формулы пентена с простейшей неразветвленной углеродной цепью имеют вид:
Изомерия пентена
Количественный состав молекулы и присутствие в ней двойной связи обусловливают существование различных вариантов порядка соединения и взаимного расположения атомов.
Структурные изомеры
Структура молекулы определяется позицией, которую занимает в молекуле двойная связь, и формой (ветвлением) углеродного скелета. По этим признакам соединения состава насчитывают пять изомерных форм:
Межклассовые изомеры пентена
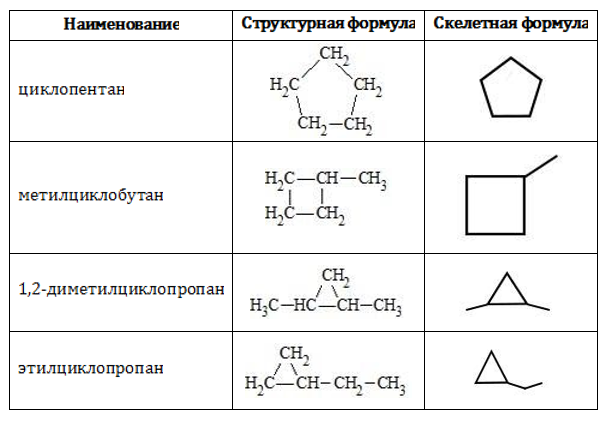
Соединения состава существуют в классе циклоалканов:
Перечисленные в таблице алициклические углеводороды также изомерны пентену.
Это интересно:
Общая формула циклоалканов
Окисление алкенов перманганатом калия
Пространственные изомеры
Цис- и транс-изомеры с химической формулой возникают у пентена-2. Они различаются расположением алкильных и водородных заместителей относительно связи
:
Таким образом, у пентена существует шесть изомеров, относящихся к ряду алкенов, и четыре межклассовых изомера из ряда циклоалканов.
Физические свойства
Пентены представляют собой бесцветные, легкие, подвижные жидкости, кипящие при низких температурах. Пары пентенов тяжелее воздуха, в смеси с ним способны образовывать взрывоопасные смеси. Все изомеры, принадлежащие к классу алкенов, имеют общие физические свойства:
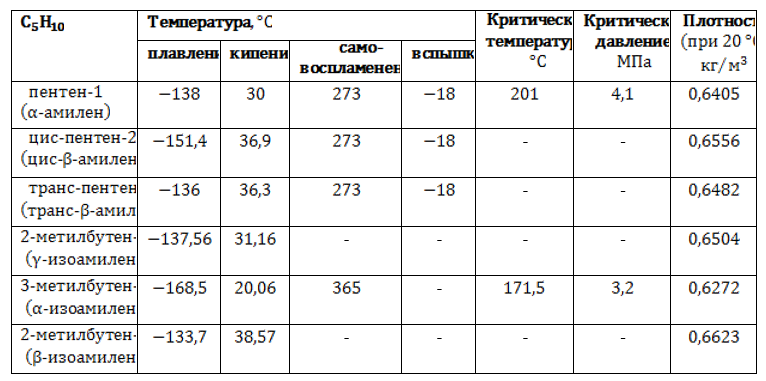
Различия в свойствах, обусловленные особенностями строения изомеров, представлены в таблице:
Химические свойства
Пентены проявляют в химических взаимодействиях все свойства, присущие алкенам.
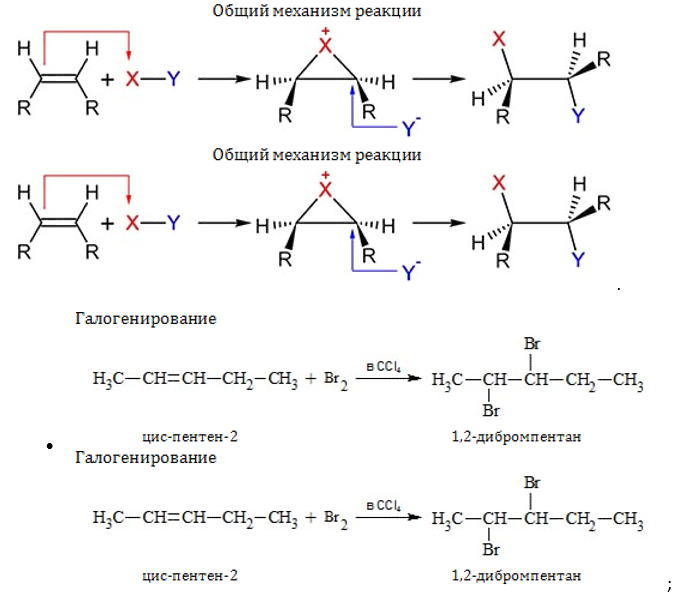
- Электрофильное (ионное) присоединение:
- Радикальное присоединение с разрывом
-связи:
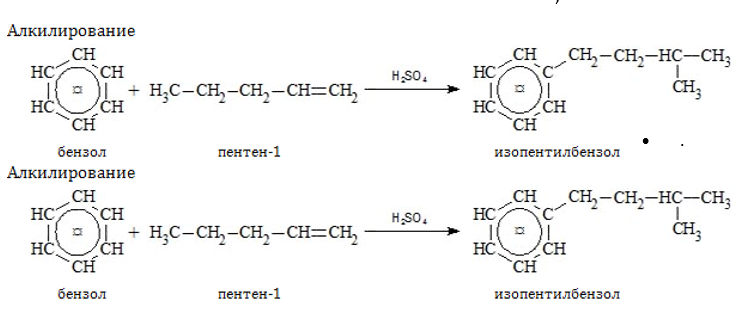
- Радикальное замещение с сохранением
-связи:
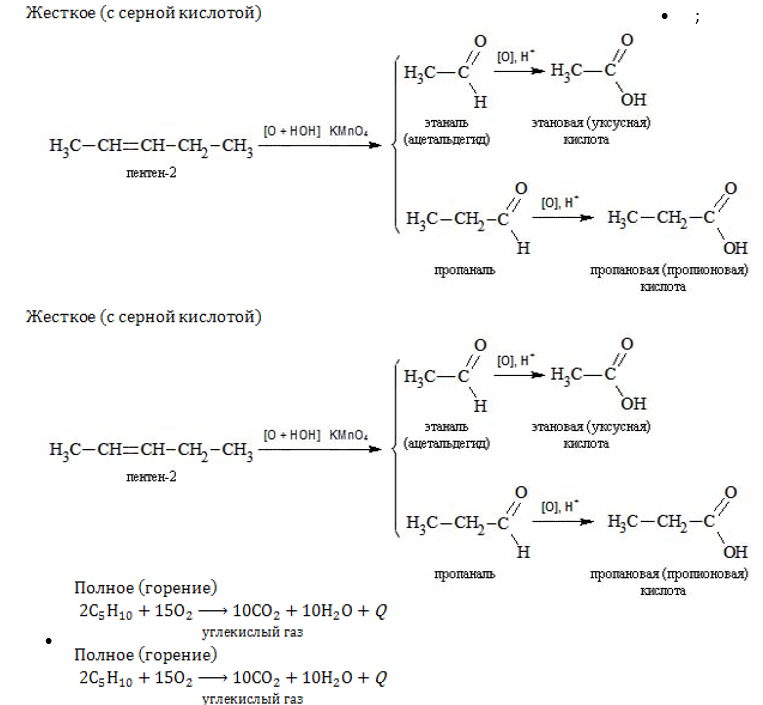
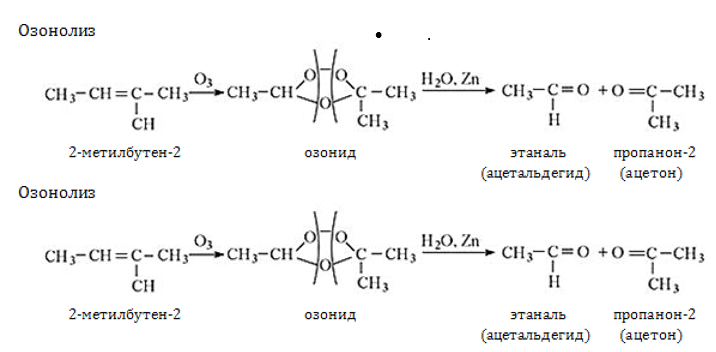
- Окисление:
- Изомеризация:
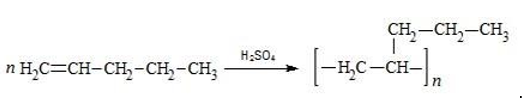
- Полимеризация:
- Разложение:
Получение пентенов
Применение пентенов
В промышленности используются все изомеры пентена:
- пентен-1 в составе смеси углеводородов применяется в производстве бензина;
- пентен-1 и пентен-2 используются в синтезе амиловых (пентанолы) и гексиловых (гексанолы) спиртов и соответствующих альдегидов – пентаналя и гексаналя;
- 2-метилбутен-1 и 2-метилбутен-2 применяются в органическом синтезе: получении сложных эфиров, спиртов и изопрена;
- 3-метилбутен-1 находит применение в производстве пластических масс, а также добавляется в состав топлива с целью повышения октанового числа.
Продукты полимеризации пентенов используются в качестве компонентов смазочных масел и типографской краски.
Изомеры пентена в смеси с добавлением изопентана (так называемый технический пентен) служит сырьем для синтеза бутадиена.
При работе с пентенами необходимо использовать средства защиты дыхательных путей и перчатки, так эти соединения оказывают раздражающее воздействие. Поскольку смесь паров пентеновых углеводородов взрывоопасна, следует соблюдать правила техники безопасности.
Оценка статьи:
Загрузка…
Напишите пожалуйста все структурные формулы пентена c5h10.
На этой странице вы найдете ответ на вопрос Напишите пожалуйста все структурные формулы пентена c5h10?. Вопрос
соответствует категории Химия и уровню подготовки учащихся 10 — 11 классов классов. Если ответ полностью не удовлетворяет критериям поиска, ниже можно
ознакомиться с вариантами ответов других посетителей страницы или обсудить с
ними интересующую тему. Здесь также можно воспользоваться «умным поиском»,
который покажет аналогичные вопросы в этой категории. Если ни один из
предложенных ответов не подходит, попробуйте самостоятельно сформулировать
вопрос иначе, нажав кнопку вверху страницы.
Напишите структурную формулу пентена
Найди верный ответ на вопрос ✅ «Напишите структурную формулу пентена …» по предмету 📙 Химия, а если ответа нет или никто не дал верного ответа, то воспользуйся поиском и попробуй найти ответ среди похожих вопросов.
Искать другие ответы
From Wikipedia, the free encyclopedia

1-Pentene |
|

cis-2-Pentene |
|

trans-2-Pentene |
|
| Names | |
|---|---|
| IUPAC names
Pent-1-ene |
|
| Other names
amylene, n-amylene, n-pentene, beta-n-amylene, sym-methylethylethylene, pentylene |
|
| Identifiers | |
|
CAS Number |
|
|
3D model (JSmol) |
|
| ChemSpider |
|
| ECHA InfoCard | 100.042.636 |
| EC Number |
|
|
PubChem CID |
|
| UNII |
|
|
CompTox Dashboard (EPA) |
|
|
InChI
|
|
|
SMILES
|
|
| Properties | |
|
Chemical formula |
C5H10 |
| Molar mass | 70.135 g·mol−1 |
| Density | 0.64 g/cm3 (1-pentene)[1] |
| Melting point | −165.2 °C (−265.4 °F; 108.0 K) (1-pentene)[1] |
| Boiling point | 30 °C (86 °F; 303 K) (1-pentene)[1] |
|
Magnetic susceptibility (χ) |
-53.7·10−6 cm3/mol |
| Hazards | |
| Safety data sheet (SDS) | MSDS |
|
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
Infobox references |
Pentenes (also called Pentylenes) are alkenes with the chemical formula C
5H
10. Each contains one double bond within its molecular structure. Six different compounds are in this class, differing from each other by whether the carbon atoms are attached linearly or in a branched structure, and whether the double bond has a cis or trans form.
Straight-chain isomers[edit]
1-Pentene is an alpha-olefin. Most often, 1-pentene is made as a byproduct of catalytic or thermal cracking of petroleum, or during production of ethylene and propylene via thermal cracking of hydrocarbon fractions.
The only commercial manufacturer of 1-pentene is Sasol Ltd, where it is separated from crude made by the Fischer–Tropsch process.[2]
2-Pentene has two geometric isomers, cis-2-pentene and trans-2-pentene. Cis-2-Pentene is used in olefin metathesis.
Branched-chain isomers[edit]
The branched isomers are 2-methylbut-1-ene, 3-methylbut-1-ene (isopentene), and 2-methylbut-2-ene (isoamylene).
Isoamylene is one of three main byproducts of deep catalytic cracking (DCC), which is very similar to the operation of the fluid catalytic cracking (FCC). The DCC uses vacuum gas oil (VGO) as a feedstock to produce primarily propylene, isobutylene, and isoamylene. The rise in demand for polypropylene has encouraged the growth of the DCC, which is operated very much like FCC. Isobutylene and isoamylene feedstocks are necessary for the production of the much debated gasoline blending components methyl tert-butyl ether and tert-amyl methyl ether.
Production of fuels[edit]
Propylene, isobutene, and amylenes are feedstock in alkylation units of refineries. Using isobutane, blendstocks are generated with high branching for good combustion characteristics. Amylenes are valued as precursors to fuels, especially aviation fuels of relatively low volatility, as required by various regulations.[3]
References[edit]
- ^ a b c Record in the GESTIS Substance Database of the Institute for Occupational Safety and Health
- ^ «RSA Olefins | cChange». www.cchange.ac.za. Retrieved 2017-10-19.
- ^ Bipin V. Vora, Joseph A. Kocal, Paul T. Barger, Robert J. Schmidt, James A. Johnson (2003). «Alkylation». Kirk‐Othmer Encyclopedia of Chemical Technology. doi:10.1002/0471238961.0112112508011313.a01.pub2. ISBN 0471238961.
{{cite encyclopedia}}: CS1 maint: uses authors parameter (link)
I. Напишите структурную формулу пентена-2. Какие из атомов углерода в молекуле пентена-2 находятся в sp2 – гибридном состоянии?
II. Напишите структурные формулы веществ:
Этан; 2-метилпропан; 2,2 – диметилпропан; пропан
Укажите, в молекуле какого из этих веществ имеется третичный атом углерода
III. Изобразите схему образования водородной связи между молекулами одноатомных спиртов
IIII. Напишите уравнения реакций:
1) гидратации пропена
2) восстановления пропаналя
4) окисления пропаналя
Какую из этих реакций нельзя использовать для получения спиртов и почему?
V. Как называется промышленный процесс переработки нефти? В чем он заключается? Назовите продукты нефтепереработки.
VI. К какому классу веществ относятся углеводороды с общей формулой CnH2n – 6 ? Приведите структурные формулы трех веществ этого класса.
VII. Напишите уравнения реакции серебряного зеркала для глюкозы и для формальдегида. Почему сахароза не вступает в реакцию серебряного зеркала?
VIII. Допишите уравнение реакции и определите ее вид:
kat, t°
СН ≡ СН + НОН →
IX. Напишите структурную формулу звена молекулы целлюлозы.
X. Что такое изомеры? Какие углеводороды являются межклассовыми изомерами алкинов? Приведите структурные формулы бутина -1 и его межклассового изомера.