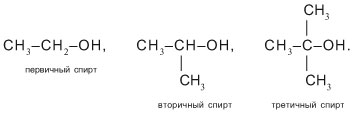
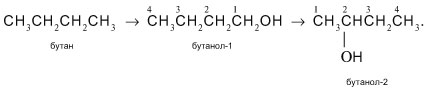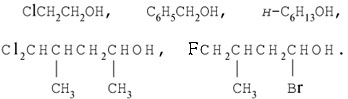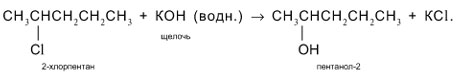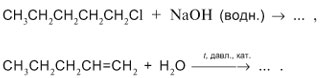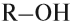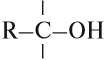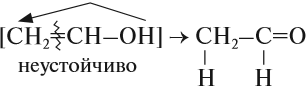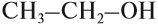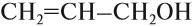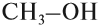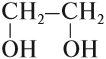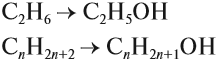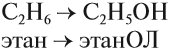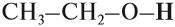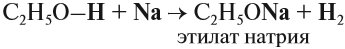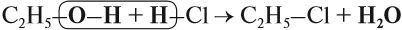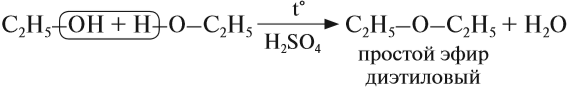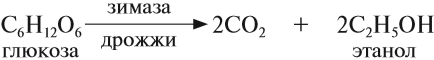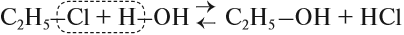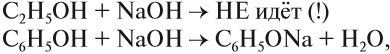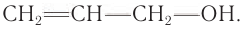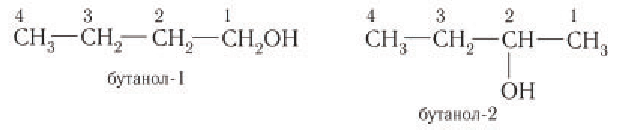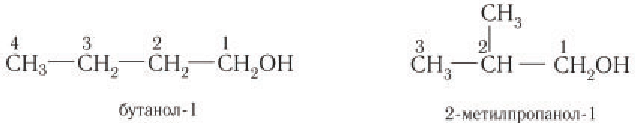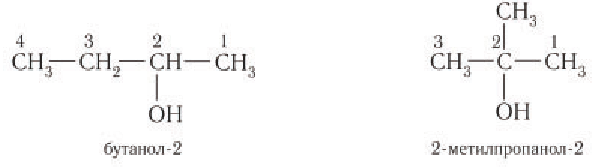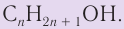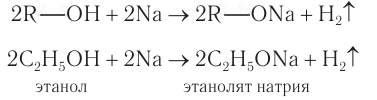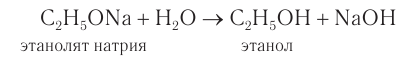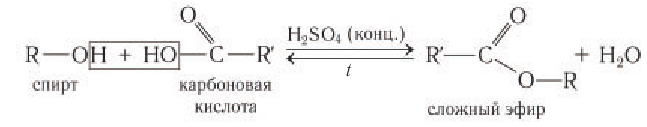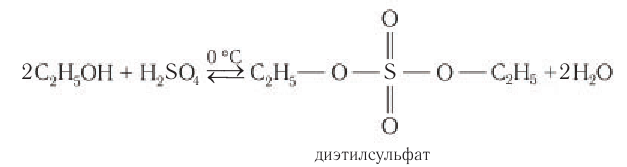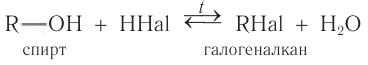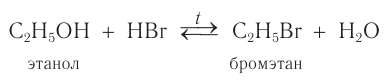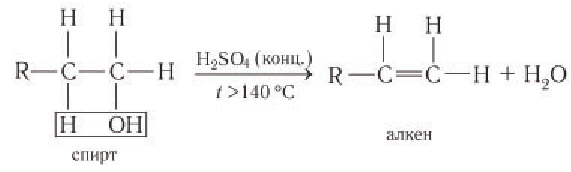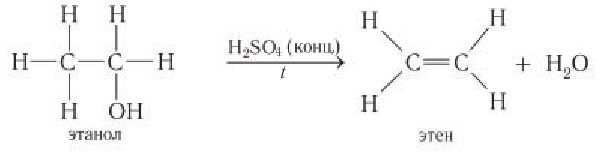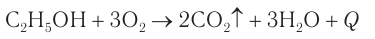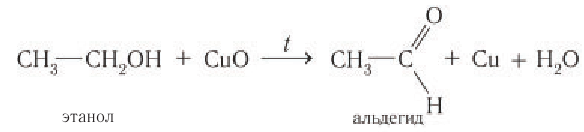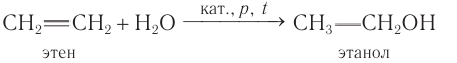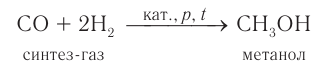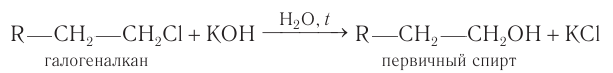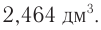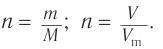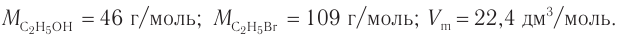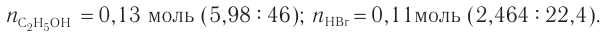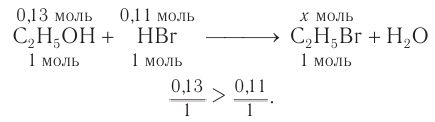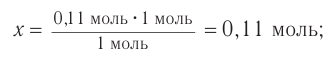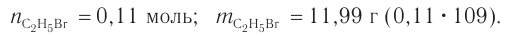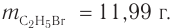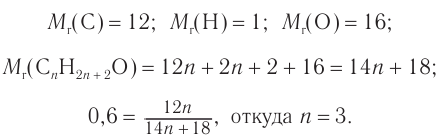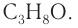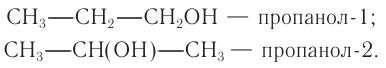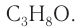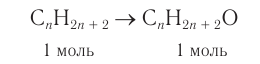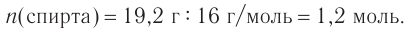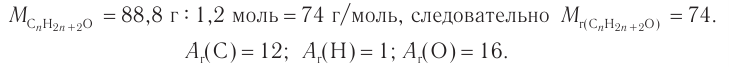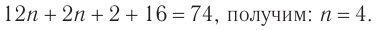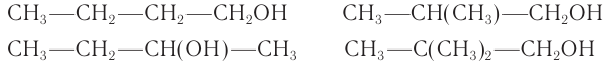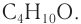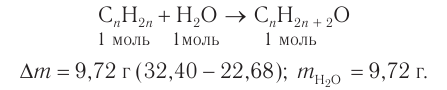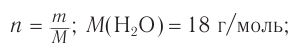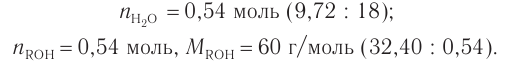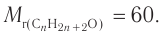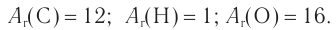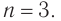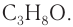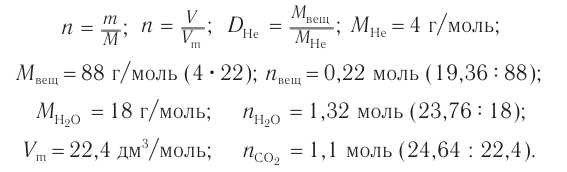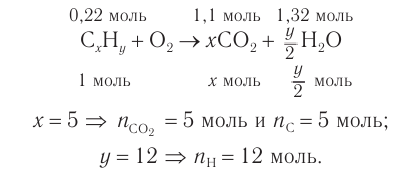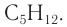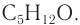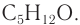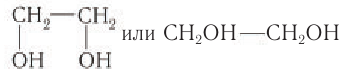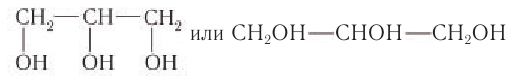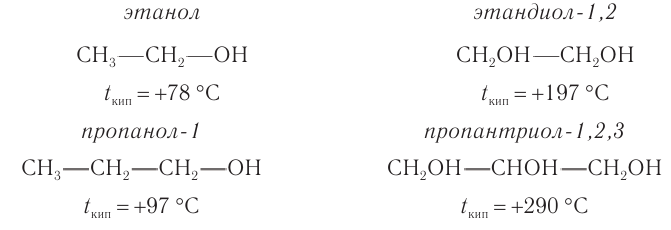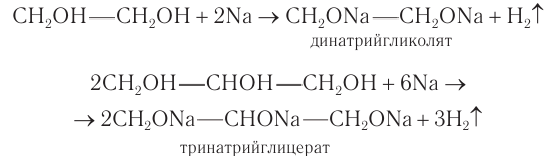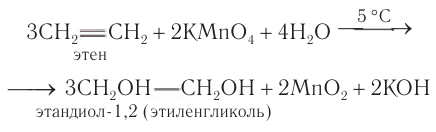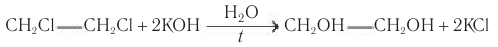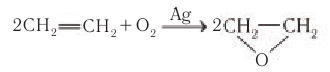Одноатомные предельные спирты
Спиртами называют производные углеводородов общей формулы RОН, где R – углеводородный радикал. Формула спирта получается из формулы соответствующего алкана заменой атома Н на группу ОН: RН RОН.
Вывести химическую формулу спиртов можно иначе, включая атом кислорода О между атомами
С–Н молекулы углеводорода:
RН RОН, СН3–Н
СН3–О–Н.
Гидроксильная группа ОН является функциональной группой спиртов. То есть группа ОН – особенность спиртов, она обусловливает главные физические и химические свойства этих соединений.
Общая формула одноатомных предельных спиртов – СnH2n+1OH.
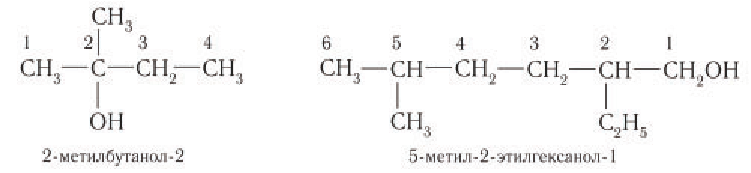
Названия спиртов получают из названий углеводородов с таким же числом атомов С, как в спирте, добавлением суффикса —ол-. Например:
Название спиртов как производных соответствующих алканов характерно для соединений с линейной цепью. Положение группы ОН в них – при крайнем или при внутреннем атоме
С – указывают цифрой после названия:
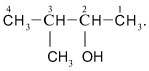
Названия спиртов – производных разветвленных углеводородов – составляют обычным образом. Выбирают главную углеродную цепь, которая должна включать атом С, соединенный с группой ОН. Нумеруют атомы С главной цепи таким образом, чтобы углерод с группой ОН получил меньший номер:
Название cоставляют, начиная с цифры, указывающей положение заместителя в главной углеродной цепи: «3-метил…» Затем называют главную цепь: «3-метилбутан…» Наконец добавляют суффикс —ол-(название группы ОН) и цифрой указывают атом углерода, с которым связана группа ОН: «3-метилбутанол-2».
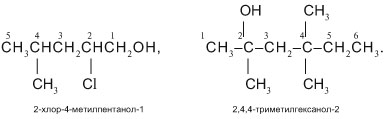
Если заместителей при главной цепи несколько, их перечисляют последовательно, указывая цифрой положение каждого. Повторяющиеся заместители в названии записывают с помощью приставок «ди-», «три-», «тетра-» и т.д. Например:
Изомерия спиртов. Изомеры спиртов имеют одинаковую молекулярную формулу, но разный порядок соединения атомов в молекулах.
Два вида изомерии спиртов:
1) изомерия углеродного скелета;
2) изомерия положения гидроксильной группы в молекуле.
Представим изомеры спирта С5Н11ОН этих двух видов в линейно-уголковой форме записи:
По числу атомов С, связанных со спиртовым (–С–ОН) углеродом, т.е. соседних с ним, спирты называют первичными (один сосед С), вторичными (два С) и третичными (три С-заместителя при углероде –С–ОН). Например:
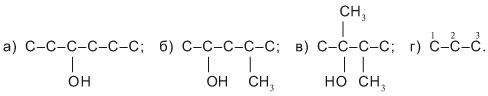
Задача. Составьте по одному изомеру спиртов молекулярной формулы С6Н13ОН с главной углеродной цепью:
а) С6, б) С5, в) С4, г) С3
и назовите их.
Решение
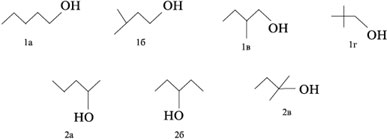
1) Записываем главные углеродные цепи с заданным числом атомов С, оставляя место для атомов Н (их укажем позже):
а) С–С–С–С–С–С; б) С–С–С–С–С; в) С–С–С–С; г) С–С–С.
2) Произвольно выбираем место присоединения группы ОН к главной цепи и при внутренних атомах С указываем углеродные заместители:
В примере г) нет возможности разместить три заместителя СН3– при атоме С-2 главной цепи. У спирта С6Н13ОН нет изомеров с трехуглеродной главной цепью.
3) Расставляем атомы Н при углеродах главной цепи изомеров а)–в), руководствуясь валентностью углерода С(IV), и называем соединения:
УПРАЖНЕНИЯ.
1. Подчеркните химические формулы предельных одноатомных спиртов:
СН3ОН, С2Н5ОН, СН2=СНСН2ОН, СНССН2ОН, С3Н7ОН,
СН3СНО, С6Н5СН2ОН, С4Н9ОН, С2Н5ОС2Н5, НОСН2СН2ОН.
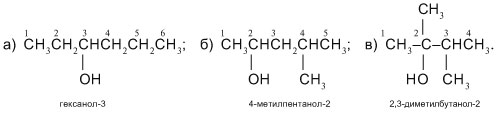
2. Назовите следующие спирты:
3. Составьте структурные формулы по названиям спиртов: а) гексанол-3;
б) 2-метилпентанол-2; в) н-октанол; г) 1-фенилпропанол-1; д) 1-циклогексилэтанол.
4. Составьте структурные формулы изомеров спиртов общей формулы С6Н13ОН:
а) первичного; б) вторичного; в) третичного. Назовите эти спирты.
5. По линейно-уголковым (графическим) формулам соединений запишите их структурные формулы и дайте названия веществам:
Получение спиртов
Низкомолекулярные спирты – метанол СН3ОН, этанол С2Н5ОН, пропанол С3Н7ОН, а также изопропанол (СН3)2СНОН – бесцветные подвижные жидкости со специфическим алкогольным запахом. Высокие температуры кипения: 64,7 °С – СН3ОН, 78 °С – С2Н5ОН, 97 °С – н-С3Н7ОН и 82 °С – (СН3)2СНОН – обусловлены межмолекулярной водородной связью, существующей в спиртах. Спирты С(1)–С(3) смешиваются с водой (растворяются) в любых соотношениях. Эти спирты, особенно метанол и этанол, наиболее широко используются в промышленности.
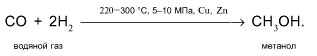
1. Метанол синтезируют из водяного газа:
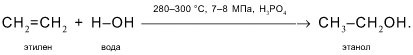
2. Этанол получают гидратацией этилена (присоединением воды к С2Н4):
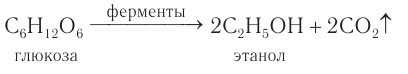
3. Другой способ получения этанола – сбраживание сахаристых веществ под действием дрожжевых ферментов. Процесс спиртового брожения глюкозы (виноградного сахара) имеет вид:
4. Этанол получают из крахмала, а также из древесины (целлюлозы) путем гидролиза до глюкозы ипоследующего сбраживания в спирт:
5. Высшие спирты получают из галогенпроизводных углеводородов гидролизом под действием водных растворов щелочей:
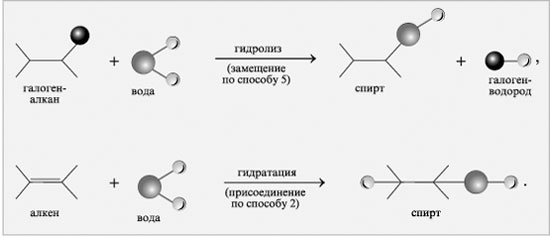 |
Гидролиз и гидратация – способы получения спиртов |
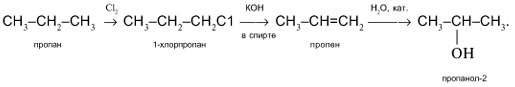
Задача. Как из пропана получить пропанол-1?
Решение
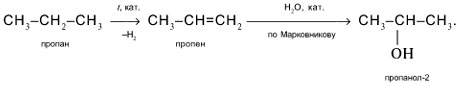
Из пяти предложенных выше способов получения спиртов ни в одном не рассмотрено получение спирта из алкана (пропана и т.п.). Поэтому синтез пропанола-1 из пропана будет включать несколько стадий. По способу 2 спирты получают из алкенов, которые в свою очередь доступны при дегидрировании алканов. Схема процесса следующая:
Другая схема такого же синтеза на одну стадию длиннее, зато ее легче осуществить в лаборатории:
Присоединение воды к пропену на последней стадии протекает по правилу Марковникова и приводит к вторичному спирту – пропанолу-2. В задании требуется получить пропанол-1. Поэтому задача не решена, ищем другой способ.
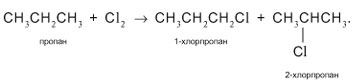
Способ 5 состоит в гидролизе галогеналканов. Необходимый полупродукт для синтеза пропанола-1 – 1-хлорпропан – получают следующим образом. Хлорирование пропана дает смесь 1- и 2-монохлорпропанов:
Из этой смеси выделяют 1-хлорпропан (например, с помощью газовой хроматографии или за счет разных температур кипения: для 1-хлорпропана tкип = 47 °С, для 2-хлорпропана tкип = 36 °С). Действием на 1-хлорпропан водной щелочью КОН или NaOH синтезируют целевой пропанол-1:
Обратите внимание, что взаимодействие одних и тех же веществ: СН3СН2СН2Сl и КОН – в зависимости от растворителя (спирт С2Н5ОН или вода) приводит к разным продуктам – пропилену
(в спирте) или пропанолу-1 (в воде).
УПРАЖНЕНИЯ.
1. Приведите уравнения реакций промышленного синтеза метанола из водяного газа и этанола – гидратацией этилена.
2. Первичные спирты RСН2ОН получают гидролизом первичных алкилгалогенидов RСН2Наl, а вторичные спирты синтезируют гидратацией алкенов. Завершите уравнения реакций:
3. Предложите способы получения спиртов: а) бутанола-1; б) бутанола-2;
в) пентанола-3, исходя из алкенов и алкилгалогенидов.
4. При ферментативном брожении сахаров наряду с этанолом в небольшом количестве образуется смесь первичных спиртов С3–С5 – сивушное масло. Главный компонент в этой смеси – изопентанол (СН3)2СНСН2СН2ОН, минорные компоненты – н-С3Н7ОН, (СН3)2СНСН2ОН и СН3СН2СН(СН3)СН2ОН. Назовите эти «сивушные» спирты по номенклатуре ИЮПАК. Составьте уравнение реакции брожения глюкозы С6Н12О6, в которой бы получались все четыре примесных спирта в мольном соотношении соответственно 2:1:1:1. Введите газ СО2 в правую часть уравнения в количестве 1/3 моль от всех исходных атомов С, а также необходимое количество молекул Н2О.
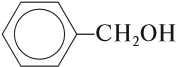
5. Приведите формулы всех ароматических спиртов состава С8Н10О. (В ароматических спиртах группа ОН удалена от бензольного кольца на один или несколько атомов С:
С6Н5– (СН2)n– ОН.)
Содержание
- Определение
- Гомологический ряд, номенклатура, изомерия
- Строение молекул
- Свойства одноатомных спиртов
- Физические свойства
- Химические свойства
- Получение и применение спиртов (на примере этилового спирта)
- Многоатомные спирты
- Понятие о фенолах
- Выводы
Определение
Спирты — это производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на гидроксогруппу ОН.
Если углеводородный радикал обозначить буквой R, то в общем виде формулу молекулы спирта можно изобразить так:
У атома углерода, который соединен с гидроксогруппой, все связи должны быть простыми:
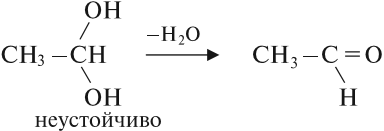
Соединения, у которых гидроксогруппа находится рядом с двойной связью, неустойчивы:
По строению углеводородного радикала спирты делят на:
- предельные
в углеводородном радикале, все связи простые;
- непредельные
в углеводородном радикале, есть кратная связь;
- ароматические
имеется бензольное кольцо, т. е. в углеводородном радикале есть ароматическая связь.
По числу гидроксогрупп спирты делят на:
- одноатомные
в состав молекулы входит одна гидроксогруппа ОН;
- многоатомные
в состав молекул входит две или более (много) гидроксогрупп.
Рассмотрим строение молекул и свойства предельных одноатомных спиртов.
Гомологический ряд, номенклатура, изомерия
Для того чтобы вывести общую формулу гомологического ряда предельных одноатомных спиртов, сравним их состав и состав алканов:
В названиях спиртов гидроксогруппа обозначается суффиксом ОЛ. Этот суффикс прибавляется к названию исходного углеводорода:
Кроме этих названий (по ИЮПАК) для простейших спиртов используют рациональные названия, которые происходят от названия радикала:
Начиная с n = 3, для спиртов возможна изомерия. Она связана с положением группы ОН в молекуле:
Вопрос. Как обозначить положение группы ОН в молекуле?
Как всегда, положение группы ОН обозначают цифрой, которая соответствует номеру атома углерода, соединённому с группой ОН. Нумерацию основной цепи начинают с того конца, к которому ближе группа ОН.
Таким образом: название спирта (1) пропанол-1; название спирта (2) пропанол-2.
Поскольку спирты называют «по радикалам», эти спирты можно назвать и так: пропиловый спирт (1) и изопропиловый спирт (2).
Задание 22.1. Составьте молекулярные формулы этих спиртов и убедитесь, что это — изомеры.
Спирты изомерны простым эфирам, в молекулах которых атом кислорода соединяет два углеродных радикала (это изомерия между разными классами веществ):
Простые эфиры — это вещества, в молекулах которых два радикала соединены атомом кислорода. Поэтому их называют, исходя из названий радикалов. Например, простой эфир (3) — это диметиловый эфир.
Задание 22.2. Составьте графическую формулу изомера пропиловых спиртов, который является простым эфиром. Назовите его.
Строение молекул
Если при помощи графической формулы показать строение молекулы этилового спирта, то легко можно увидеть, что атомы водорода в ней неравноценны:
Действительно, пять атомов водорода соединены с атомами углерода, а один — с атомом кислорода. Теория Бутлерова утверждает, что «атомы в молекуле взаимно влияют друг на друга». Поэтому можно ожидать, что этот атом водорода будет отличаться от остальных пяти. Это отличие заключается в том, что связь О–Н гораздо более полярна, чем связи С–Н. Дело в том, что атом кислорода имеет бОльшую электроотрицательность, чем атом углерода, т. е. способен сильнее смещать к себе общую пару электронов. В результате, на атомах кислорода и водорода связи О–Н появляются значительные заряды (+) и (–).
Вопрос. На каком атоме появляется (+), а на каком (–)?
Величина этих зарядов меньше единицы, но они способны притягивать к себе молекулы других реагирующих веществ, т. е. активнее участвовать в химических реакциях будут наиболее полярные связи.
Вывод. Самыми полярными связями в молекуле спирта являются связи О–Н и О–С. За счёт их разрыва происходят химические реакции (спирт функционирует). Поэтому ОH — функциональная группа спиртов.
Свойства одноатомных спиртов
Физические свойства
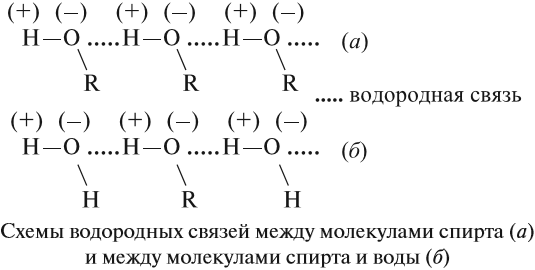
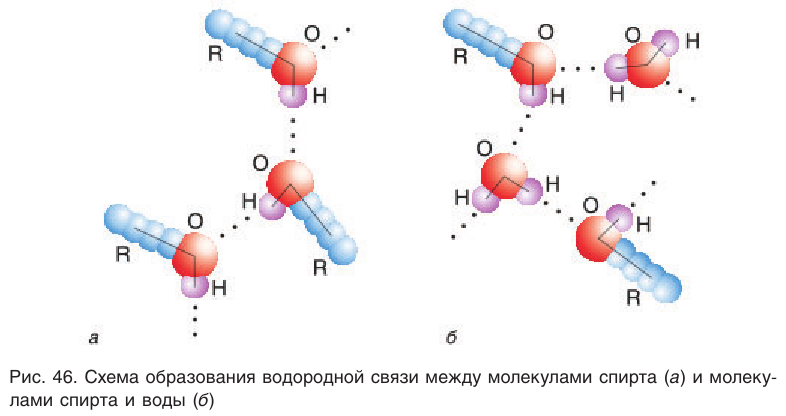
Поскольку в молекуле спирта появились полярные связи, он, в отличие от углеводородов, будет иметь более высокие температуры кипения и плавления (если сравнивать соединения с одинаковым числом атомов углерода). Это связано с тем, что полярные молекулы сильнее притягиваются друг к другу, и для того чтобы оторвать их друг от друга (перевести жидкость в газ), нужно затратить много энергии — дополнительно нагреть. Кроме того, между молекулами спиртов возникают водородные связи (а), которые дополнительно притягивают молекулы друг к другу. Поэтому этиловый спирт — бесцветная жидкость (а этан и диметиловый эфир — газы!) с т. кип. 78 °C. Спирт хорошо растворим в воде, так как и с молекулами воды спирт образует водородные связи (б).
Водородные связи непрочные, поэтому низшие одноатомные спирты (мало атомов углерода в молекуле) — летучие жидкости с характерным запахом.
Химические свойства
Спирты могут реагировать с натрием и другими щелочными металлами. При этом атом водорода ОН-группы замещается на атом металла:
Вопрос. Неорганические вещества какого класса способны вступать в реакции замещения с металлами, в результате чего выделяется водород?
Аналогичную реакцию дают кислоты, поэтому в этой реакции спирт проявляет кислотные свойства. Но это очень слабые свойства, так как растворы спиртов не изменяют окраску индикаторов и не реагируют с растворами щелочей.
Спирты реагируют с неорганическими кислотами:
В этой реакции отщепляется молекула воды, — значит, это реакция дегидратации. При записи таких реакций формулы исходных веществ записывайте так, чтобы функциональные группы были рядом, причём атомы водорода функциональных групп ОН «смотрели» друг на друга. Так, в результате реакции дегидратации, в которой участвуют две молекулы спирта, образуется простой эфир (дегидратация межмолекулярная):
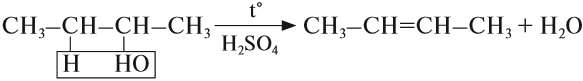
Эта реакция происходит в присутствии концентрированной серной кислоты. Если смесь спирта и концентрированной серной кислоты нагреть сильнее, то молекула воды отщепляется от одной молекулы спирта (дегидратация внутримолекулярная):
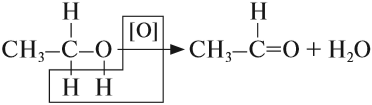
Спирты, у которых ОН-группа соединена с первым (последним) атомом углерода углеродной цепочки (первичные спирты) легко окисляются нагретым оксидом меди CuO, превращаясь в альдегиды:
При составлении этой реакции рекомендуется выделить (подчеркнуть) те атомы, которые образуют воду, и записать новую формулу без этих атомов. Спирты горят, образуя, как и углеводороды, углекислый газ и воду.
Задание 22.3. Составьте уравнение реакции горения этилового спирта.
Таким образом, для спиртов характерны реакции:
- замещения атома водорода ОН-группы;
- дегидратации (отщепления воды);
- окисления.
Все эти реакции идут с участием ОН-группы функциональной группы спиртов.
Задание 22.4. Составьте уравнения таких реакций для пропанола-1 (пропилового спирта). Уравнения реакций составляйте по аналогии с вышеперечисленными.
Получение и применение спиртов (на примере этилового спирта)
Этанол и другие спирты можно получить из алкенов.
Вопрос. При помощи какой реакции можно это осуществить (при затруднении см. урок 19.3)?
Задание 22.5. Составьте уравнение этой реакции.
Полученный таким способом спирт используют в технических целях: в качестве растворителя, для получения каучука, пластмасс и др. Кроме того, спирт используют как горючее.
Пищевой и медицинский спирты получают брожением глюкозы:
В лаборатории этиловый спирт можно получить гидролизом (взаимодействием с водой) хлорэтана:
Для того чтобы эта реакция стала необратимой, используют водный раствор щёлочи.
Задание 22.6. Составьте уравнения реакций:
- пропен + вода;
- 1-хлорпропан + NaOH (водный).
Назовите полученные вещества.
Многоатомные спирты
Многоатомные спирты содержат две и более гидроксогруппы в молекуле. При этом каждый атом углерода в молекулах спиртов может соединяться только с одной гидроксогруппой ОН, в противном случае образуются неустойчивые соединения:
Задание 22.7. Составьте формулы многоатомных спиртов, в молекуле которых:
- два атома углерода и две гидроксогруппы;
- три атома углерода и три гидроксогруппы.
У вас получились формулы простейших многоатомных спиртов:
Вопрос. Как в названии спирта обозначить число гидроксогрупп?
Названия по IUPAC этих спиртов составляют, используя уже известные правила, т. е. к названию углеводорода добавляют суффикс ОЛ, а перед ним указывают число ОН-групп при помощи префиксов ди- или три-. Например, этиленгликоль получит название: этандиол.
Задание 22.8. Назовите по правилам IUPAC глицерин.
Вопрос. Как вы считаете, какой из спиртов будет иметь большую температуру кипения — глицерин или пропанол-1? А растворимость в воде?
Многоатомные спирты за счёт многочисленных ОН-групп образуют многочисленные водородные связи и друг с другом, и с водой. Поэтому они имеют бОльшие температуры кипения и бОльшую растворимость в воде по сравнению с соответствующими одноатомными спиртами. Так, глицерин — бесцветная, густая жидкость, без запаха; он смешивается с водой в любых соотношениях и способен поглощать влагу из воздуха. Более того, безводный глицерин может отнимать воду из живых клеток кожи, вызывая ожоги. Растворы глицерина, наоборот, смягчают кожу.
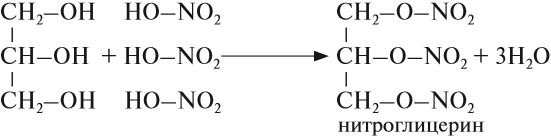
Химические свойства глицерина и других многоатомных спиртов очень похожи на свойства одноатомных спиртов: они реагируют с натрием и НСl, образуют эфиры, могут окисляться. Например, глицерин реагирует с азотной кислотой:
Нитроглицерин входит в состав сильнейшей взрывчатой смеси динамита. Его раствор используется как лекарство.
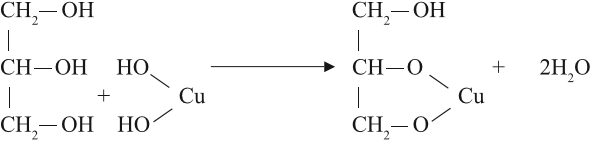
Но в химических свойствах многоатомных спиртов есть и существенные отличия. Так, они могут растворять осадок гидроксида меди II, образуя ярко-синий раствор:
Реакция происходит при обычных условиях, причём полученное соединение очень прочное: не изменяет свой цвет даже при кипячении. Одноатомные спирты такую реакцию не дают.
Вывод. Реакция растворения голубого осадка гидроксида меди II с образованием ярко-синего раствора — это качественная реакция на многоатомные спирты.
Задание 22.9. Составьте уравнения реакций этиленгликоля:
- с азотной кислотой;
- с Сu(ОН)2.
Подсказка. При составлении уравнений этих реакций записывайте формулы многоатомных спиртов так, чтобы цепочки атомов углерода располагались вертикально, а группы ОН были рядом, причём атомы водорода функциональных групп ОН «смотрели» друг на друга.
Глицерин находит широкое применение в кожевенной промышленности (смягчает кожу), используется в медицине, входит в состав невысыхающих красок. Кроме того, глицерин, точнее, остаток его молекулы входит в состав любого жира. Поэтому глицерин часто получают из природных жиров (уравнение реакции в уроке 25).
Понятие о фенолах
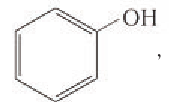
К фенолам относятся вещества, в молекулах которых гидроксогруппа ОН непосредственно связана с бензольным кольцом:
В этой молекуле ОН-группа и бензольное кольцо взаимно влияют друг на друга. Поэтому фенол по свойствам отличается и от спиртов, и от бензола. Рассмотрим примеры такого влияния.
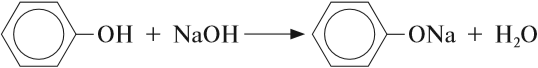
Бензольное кольцо влияет на ОН-группу, делая её более полярной, чем у спиртов. Поэтому фенол, в отличие от спиртов, реагирует с растворами щелочей:
или
В данной реакции фенол проявляет свойства кислоты. Отсюда его второе название — карболовая кислота («карболка»). Растворы фенола изменяют окраску индикатора.
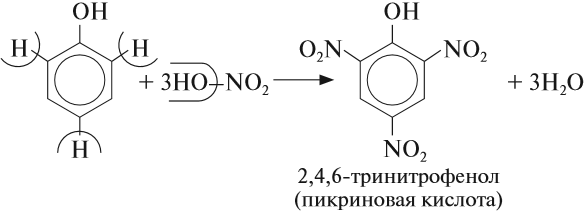
Гидроксогруппа влияет на бензольное кольцо. Фенол очень легко вступает в реакции замещения, причём, как и для толуола, реакция происходит в положениях 2, 4, 6 по отношению к гидроксогруппе:
В отличие от спиртов и бензола фенол обесцвечивает бромную воду даже при нормальных условиях. Реакция протекает аналогично предыдущей.
Задание 22.9. Составьте уравнение реакции фенола с бромом и сравните эту реакцию с реакцией толуола с бромом.
Фенол легко окисляется на воздухе, при этом его белые кристаллы розовеют. Фенол сильно ядовит, так как изменяет структуру и свойства белков — основу всего живого. Кроме того, попадая в воду, он окисляется растворённым в ней кислородом. В результате содержание кислорода в водоёме уменьшается, и обитатели его погибают. Для того чтобы обнаружить фенол в водоёме и любом растворе, используют качественную реакцию с FeCl3: при добавлении этого реактива к смеси, содержащей фенол, появляется фиолетовое окрашивание.
Фенол получают из производных бензола и каменноугольной смолы. В любом случае вначале исходное вещество или смесь превращают в фенолят, а затем выделяют чистый фенол при помощи кислоты:
Фенол применяют для дезинфекции и получения красителей и полимеров.
Выводы
Спирты и фенолы — это производные углеводородов, содержащие функциональную группу ОН. Для таких веществ характерны реакции замещения атома водорода в гидроксогруппе.
Спирты за счёт функциональной группы ОН образуют простые и сложные эфиры (см. урок 25), а фенолы реагируют и за счёт функциональной группы ОН, и за счёт ароматического ядра.
Содержание:
Спирты:
Углеводороды образуют различные функциональные производные при замещении в молекуле одного или нескольких атомов водорода на функциональную группу
Спирты и фенолы относятся к монофункциональным гидроксилпроизвод-ным углеводородов.
Спиртами называют производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на гидроксильную группу —ОН.
Классификация спиртов
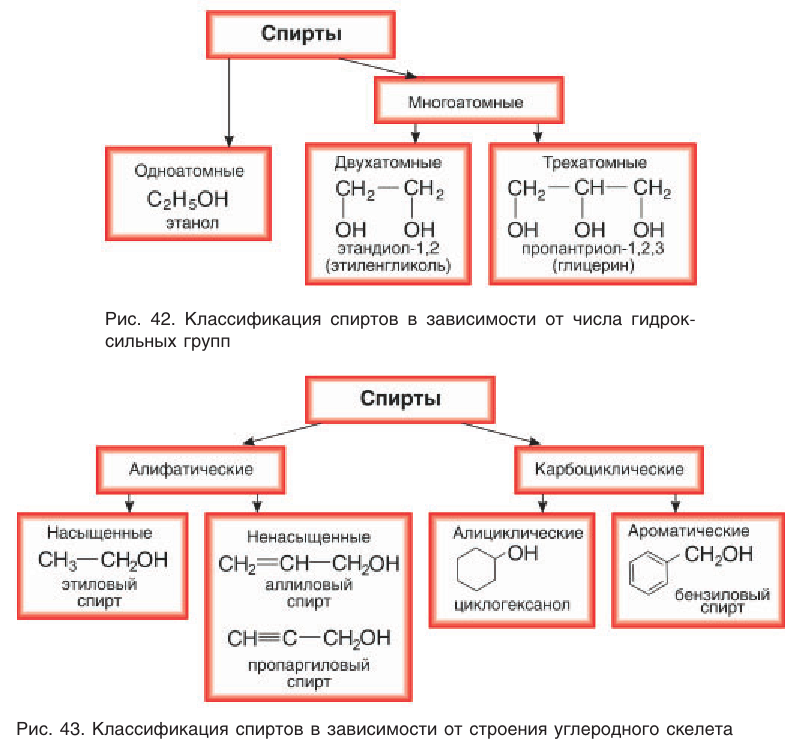
В зависимости от числа гидроксильных групп в молекуле спирты подразделяют на одноатомные, двухатомные, трехатомные, четырехатомные и т. д. (рис. 42). Например:
Спирты, содержащие несколько гидроксильных групп, объединяют общим названием многоатомные спирты.
В зависимости от строения углеродного скелета различают спирты насыщенные, ненасыщенные, ароматические (рис. 43).
Насыщенные спирты — производные алканов, например 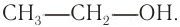
Некоторые одноатомные ненасыщенные спирты, содержащиеся в винограде, из которого производят вина, определяют характерный аромат ряда мускатных вин и рислингов. В процессе старения этих вин одноатомные спирты превращаются в двухатомные. По концентрации образовавшегося двухатомного спирта можно судить о степени старения вина.
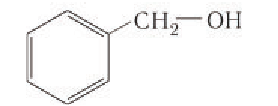
К ароматическим относят спирты, содержащие в молекуле бензольное кольцо и гидроксильную группу, которые связаны друг с другом через атом углерода, например:
Если в молекулах органических соединений гидроксильные группы связаны непосредственно с атомом углерода бензольного кольца, например:
то такие соединения относят к другому классу органических соединений фенолам.
В лепестках розы (рис. 44) содержится ароматический фенилэтиловый спирт, формула которого 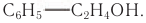
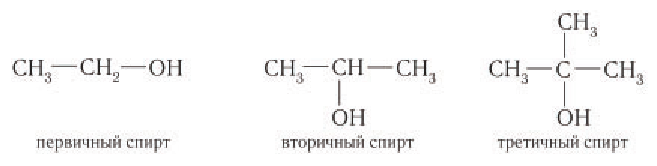
В зависимости от типа атома углерода, с которым связана гидроксильная группа, спирты классифицируют как первичные, вторичные, третичные.
Гидроксильная группа в молекулах первичных спиртов связана с первичным атомом углерода, в молекулах вторичных спиртов — с вторичным атомом углерода и в молекулах третичных спиртов — с третичным атомом углерода. Например:
Спирты — производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на гидроксильную группу —ОН.
Спирты различают по числу гидроксильных групп (атомность спиртов), строению углеродного скелета, типу атома углерода, связанного с гидроксильной группой.
Насыщенные одноатомные спирты
Строение: Насыщенными одноатомными спиртами называют производные алканов, в молекулах которых один атом водорода замещен на гидроксильную группу и содержатся только 
В органической химии известно большое число насыщенных одноатомных спиртов, химический состав и строение которых выражается общей формулой 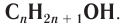
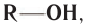
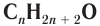
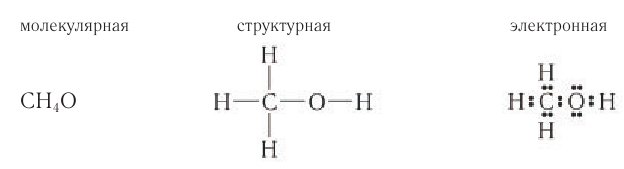
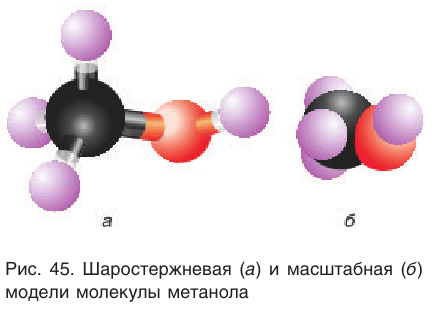
Простейшим представителем данного класса спиртов является метанол 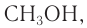
Шаростержневая и масштабная модели молекулы метанола представлены на рисунке 45.
Так как электронное строение алканов и соответствующих им алкильных групп вами уже изучено, то при изучении спиртов — производных алканов — будет рассматриваться только электронное строение функциональной группы спиртов 
В состав функциональной группы спиртов входит атом кислорода, который обладает большой электроотрицательностью и в силу этого оттягивает к себе электронную плотность 
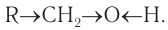
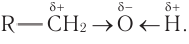
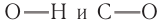
Номенклатура: По правилам номенклатуры ИЮПАК, названия насыщенных одноатомных спиртов образуются от названий соответствующих алканов с добавлением суффикса -ол. Например, 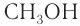
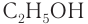
Систематическая номенклатура допускает употребление названий, связанных с названием алкильных групп, для низших членов ряда. Например,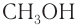
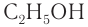
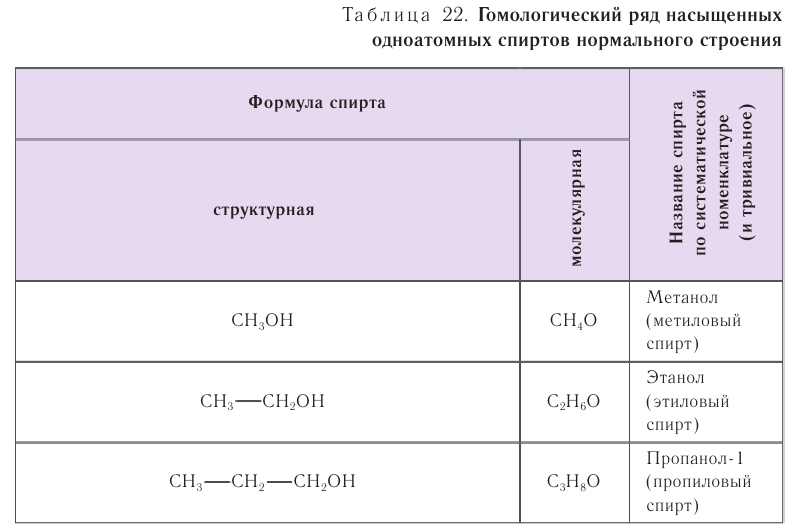
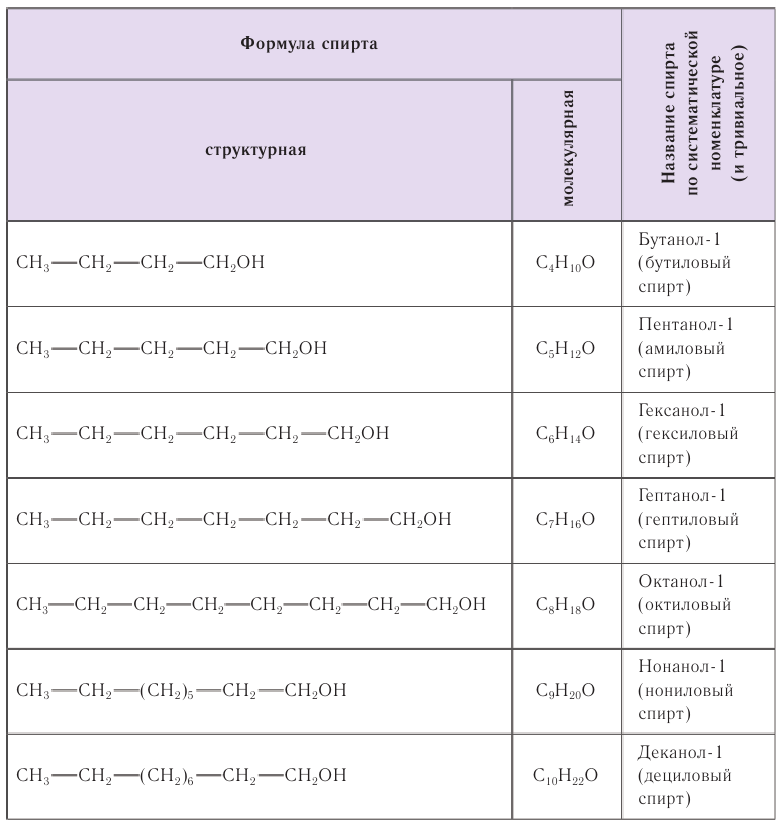
В таблице 22 приведены названия первых десяти представителей гомологического ряда спиртов, у которых функциональная группа —ОН находится у первичного атома углерода, по номенклатуре ИЮПАК и тривиальные.
При названии спиртов с неразветвленной углеродной цепью, начиная с пропанола, цифрой указывается атом углерода, с которым связана гидроксильная группа. Нумерация углеродных атомов начинается с того конца, ближе к которому расположена гидроксильная группа. Названия спиртов образуют, добавляя суффикс -ол к названию соответствующего алкана, цифрой указывается положение гидроксильной группы в цепи. Например:
Для названий спиртов с разветвленной углеродной цепью выбирают самую длинную цепь, содержащую функциональную гидроксильную группу, и нумеруют с того конца, ближе к которому расположена гидроксильная группа. Названия спиртов образуют, добавляя суффикс -ол к назанию алкана, соответствующего самой длинной цепи, цифрой указываются атомы углерода, с которыми связана гидроксильная группа и заместители. Названия заместителей перечисляются в алфавитном порядке. Например:
Изомерия: Для насыщенных одноатомных спиртов характерна структурная изомерия. Структурная изомерия спиртов обусловлена изомерией углеродного скелета и изомерией положения гидроксильной группы. Первые два члена гомологического ряда — метанол 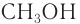
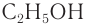
Рассмотрим примеры изомеров спиртов состава 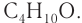
В зависимости от положения гидроксильной группы при том и другом углеродном скелете возможны еще два изомерных спирта:
Общее число структурных изомеров спиртов состава 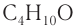
Физические свойства: Первые представители класса насыщенных одноатомных спиртов 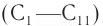
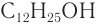
Низшие спирты обладают характерным алкогольным запахом, запах спиртов, стоящих в середине гомологического ряда, сильный и часто неприятный, а высшие спирты (более 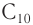
Низшие спирты (
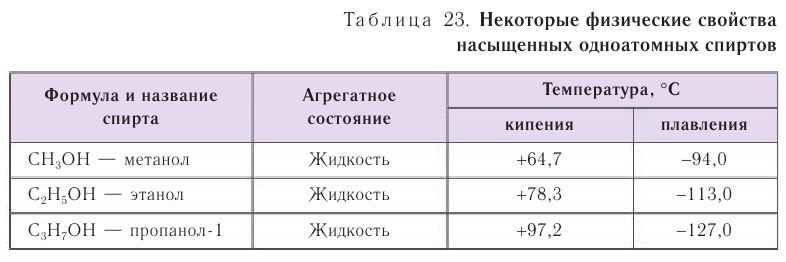
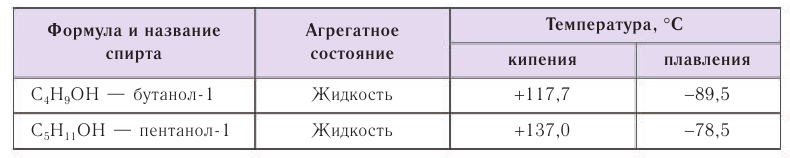
Спирты обладают аномально высокими температурами кипения по сравнению с представителями алканов с приблизительно такой же относительной молекулярной массой. Например, температура кипения этанола 78,3 °С, а пропана -42,2 °С. В таблице 23 приводятся температуры кипения, плавления и агрегатное состояние некоторых спиртов.
Причиной отсутствия газообразных спиртов при нормальных условиях, а также более высоких температур кипения спиртов по сравнению с алканами с одинаковой относительной молекулярной массой являются межмолекулярные водородные связи, характерные для спиртов. Как отмечалось, связь 
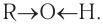
Образованием межмолекулярных водородных связей между молекулами спиртов и полярными молекулами воды (рис. 46, б) объясняется хорошая растворимость низших спиртов, в отличие от углеводородов, которые из-за малой полярности связей С—Н не образуют с водой водородных связей. С увеличением длины цепи алкильных групп растворимость спиртов понижается, и октанол уже не смешивается с водой.
Насыщенными одноатомными спиртами называют производные алканов, в молекулах которых один атом водорода замещен на гидроксильную группу.
Общая формула насыщенных одноатомных спиртов
Структурная изомерия спиртов обусловлена строением углеродного скелета и различным положением гидроксильной группы при одинаковой углеродной цепи.
На физические свойства спиртов большое влияние оказывает водородная связь между молекулами спиртов или молекулами спиртов и воды в их растворах.
Химические свойства спиртов
Характерные реакции спиртов определяются наличием в составе их молекул гидроксильиой группы, атом кислорода которой смещает электронную плотность как от атома водорода, так и от атома углерода. Такая поляризация может способствовать разрыву связей 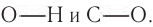
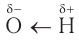
Рассмотрим важнейшие химические свойства спиртов на примере алифатических насыщенных одноатомных спиртов.
Взаимодействие со щелочными металлами: При взаимодействии щелочных металлов 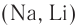

Спирты — очень слабые электролиты, слабее даже, чем вода. Поэтому алкокеиды (алкоголяты) легко разлагаются водой:
При взаимодействии с металлами у спиртов проявляются кислотные свойства, но к классу кислот спирты не относят, так как степень их диссоциации незначительна. Поэтому спирты с водными растворами щелочей взаимодействуют обратимо.
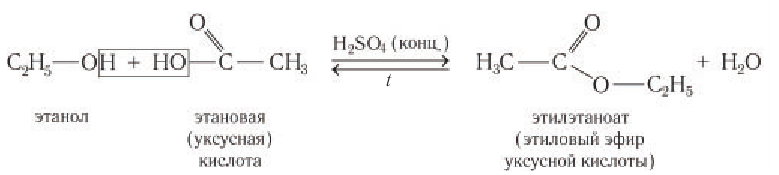
Взаимодействие с карбоновыми и кислородсодержащими минеральными кислотами с образованием сложных эфиров.
В реакции с карбоновыми кислотами от молекулы спирта отщепляется атом водорода, а от молекулы карбоновой кислоты — гидроксильная группа с образованием молекулы воды. Реакция обратима, но равновесие смещается вправо в присутствии концентрированной серной кислоты и при выводе воды из зоны реакции:
В реакциях с кислородсодержащими минеральными кислотами спирты образуют сложные эфиры этих кислот:
Взаимодействие с галогеноводородами с образованием галогеналканов
В реакции с галогеноводородами в молекуле спирта происходит разрыв связи 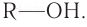
Данная реакция обратима. В этой реакции проявляются слабые основные свойства спирта.
При взаимодействии этанола с бромоводородом образуется бромэтан — тяжелая жидкость:
Внутримолекулярная дегидратация с образованием алкена
Первичные спирты дегидратируются под действием катализатора — концентрированной серной кислоты — при высоких температурах (выше 140 °С) с образованием алкена:
Реакция дегидратации обусловлена отщеплением водорода в виде протона и гидроксильной группы от соседних атомов углерода.
Например, в результате внутримолекулярного отщепления молекулы воды от молекулы этанола (под действием катализатора — концентрированной серной кислоты) образуется этен:
Реакции окисления
Спирты горят на воздухе или в кислороде некоптящим пламенем с выделением большого количества теплоты (рис. 48):
С более слабым, чем кислород, окислителем, например с оксидом меди(II), происходит частичное окисление спиртов, при этом первичные спирты окисляются до альдегидов.
Если в пробирку с этанолом опустить раскаленную скрученную в спираль медную проволоку, покрытую черным налетом оксида меди(II), то черный налет на проволоке исчезает. Спираль приобретает розово-красный цвет, при этом чувствуется неприятный запах образовавшегося альдегида:
Под действием таких окислителей, как подкисленный раствор перманганата калия или дихромата калия, первичные спирты окисляются до карбоновых кислот.
Кислотно-основные свойства насыщенных одноатомных спиртов обусловлены наличием в их молекулах функциональной гидроксильной группы.
Спирты взаимодействуют со щелочными металлами, галогеноводородами, карбоновыми и минеральными кислотами; вступают в реакции дегидратации и окисления.
Получение и применение спиртов
Получение: Для промышленного получения спиртов используют ненасыщенные углеводороды, извлекаемые из нефтепродуктов, или галогеналканы.
Познакомимся с основными общими промышленными и лабораторными способами получения насыщенных одноатомных спиртов и специфическими способами получения этанола и метанола.
1) Одним из наиболее важных общих промышленных способов получения спиртов является гидратация алкенов.
Этанол получают гидратацией этена водяными парами при повышенной температуре (280—300 °С), повышенном давлении (7—8 мПа) и в присутствии катализатора
Спирт, полученный из этена, называют синтетическим.
2) В пищевой промышленности этанол получают характерным только для него способом при спиртовом брожении глюкозы под действием ферментов, выделяемых некоторыми видами дрожжевых грибков:
Брожению подвергают виноградный сок, содержащий глюкозу, а также картофельный крахмал, который превращается в глюкозу под действием особого фермента. Этанол, полученный при ферментативном расщеплении различных пищевых продуктов, используют в основном для изготовления спиртных напитков.
В промышленности этанол производят гидролизным способом из древесных опилок, отходов целлюлозно-бумажной промышленности и т. д. Содержащуюся в древесине целлюлозу подвергают гидролизу с образованием глюкозы, которую далее подвергают брожению, и получают этанол, называемый гидролизным спиртом.
3) В промышленности метанол получают характерным только для него способом при взаимодействии водорода с угарным газом (СО) при повышенном давлении и высокой температуре в присутствии катализатора:
Смесь угарного газа и водорода, взятых в количественном соотношении 1 : 2, называют синтез-газом.
Историческое название метанола — древесный спирт. Оно указывает на старый способ получения спирта — сухую перегонку древесины твердых пород дерева (нагревание древесины без доступа воздуха).
Для получения спиртов в лаборатории используют галогеналканы.
При гидролизе моногалогеналканов с галогеном при первичном атоме углерода в водных растворах щелочей при нагревании образуются первичные спирты:
Гидролиз галогеналканов, проводимый в присутствии щелочи, является практически необратимым процессом и используется как общий метод получения первичных насыщенных спиртов в лаборатории.
Применение: Спирты находят широкое применение. В химической промышленности спирты — исходные вещества для разнообразных синтезов. Во многих производствах спирты применяют в качестве растворителей. Рассмотрим несколько примеров промышленного использования важнейших насыщенных одноатомных спиртов.
Метанол (метиловый спирт) 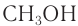
Метанол — прекрасный растворитель для многих органических и неорганических веществ.
Необходимо знать, что метанол — сильнейший яд. Употребление даже нескольких граммов метанола приводит к слепоте, а затем и смерти. Вот поэтому на банках, в которых хранится этот спирт, используемый для технических нужд, имеется надпись: «Метанол — яд». Это должно служить серьезным предостережением при работе с ним.
Этанол (этиловый спирт) 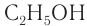
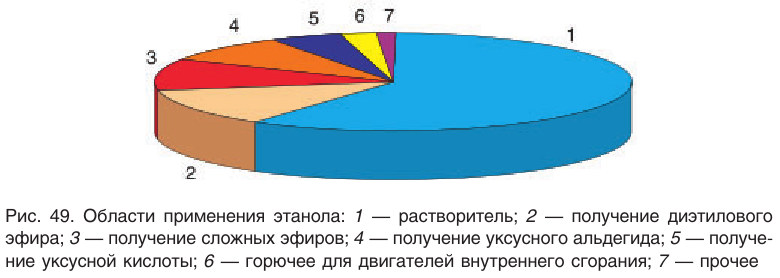
Этанол является исходным веществом в промышленном органическом синтезе (диэтиловый эфир, этилацетат и другие эфиры и т. д.), окислением этанола получают пищевую уксусную кислоту.
Спирт-ректификат, получаемый в промышленности, представляет собой смесь этанола (массовая доля 95,6 %) и воды (массовая доля 4,4 %). Безводный спирт называют абсолютным спиртом.
Следует помнить, что этанол — своего рода наркотик, возбуждающе действующий на организм человека. Даже небольшие дозы снижают остроту зрения, замедляют реакции и уменьшают способность здраво рассуждать. Длительное употребление спирта вызывает тяжелые заболевания нервной и сердечно-сосудистой систем, разрушение печени и приводит к преждевременной смерти.
В этанол, применяемый для технических целей, специально добавляют небольшие количества трудноотделяемых ядовитых, плохо пахнущих и имеющих отвратительный вкус веществ и подкрашивают. Содержащий такие добавки спирт называют денатуратом. Употребление денатурата смертельно опасно.
Другие (низшие) спирты используются в качестве растворителей при изготовлении различных лаков и красок на предприятиях лакокрасочной промышленности, одним из которых является ОАО «Лакокраска» в Лиде.
Высшие спирты (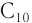
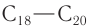


Ненасыщенный аллиловый спирт 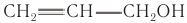
В промышленном масштабе этанол получают гидратацией этена, гидролизным способом, в процессе спиртового брожения глюкозы.
Метанол в промышленных масштабах в основном получают из синтез-газа.
В лаборатории первичные насыщенные одноатомные спирты получают в процессе щелочного гидролиза моногалогеналканов.
Спирты используют для синтеза многих органических веществ.
Решение расчетных задач
В параграфе рассмотрены образцы решения задач таких типов, как расчеты по химическим уравнениям, если одно из реагирующих веществ взято в избытке, и определение молекулярных формул органических веществ на основании качественного и количественного состава.
Пример 1.
Определите массу бромэтана, полученного в реакции, для которой был взят этанол массой 5,98 г и бромоводород объемом (н. у.)
Решение
1. Общие формулы, используемые при расчетах:
2. Значения молярных масс веществ, молярный объем:
3. Определяем химические количества спирта и бромоводорода, взятых для реакции:
4. На основе анализа уравнения реакции определяем, какое из веществ взято в избытке, а затем рассчитываем химическое количество и массу продукта реакции:
Следовательно, спирт взят в избытке. Расчеты продукта реакции проводятся исходя из данных о химическом количестве хлороводорода:
Ответ:
Пример 2.
Массовая доля углерода в насыщенном одноатомном спирте равна 0,6. Определите молекулярную формулу спирта. Составьте структурные формулы возможных изомеров и назовите их по номенклатуре ИЮПАК.
Решение
1. Для решения задачи используем общую формулу 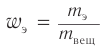
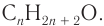
2. Определяем формулу искомого спирта.
Общая формула 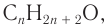
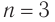
Изомеры:
Ответ:
Пример 3.
В результате ряда последовательных реакций из алкана массой 69,6 г получен первичный насыщенный одноатомный спирт массой 88,8 г с тем же числом атомов углерода в молекуле, что и у алкана (алкан 

Решение
1. Из алкана химическим количеством 1 моль получают спирт химическим количеством 1 моль:
2. Разница масс взятого и полученного веществ равна 19,2 г (88,8 — 69,6). Разница молярных масс спирта и алкана равна 16, что хорошо видно при анализе общих формул алканов и насыщенных одноатомных спиртов:
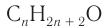
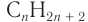
3. Используя общую формулу 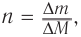
4. Зная химическое количество и массу спирта, определяем его молярную массу и молекулярную формулу:
Решая уравнение
Следовательно, молекулярная формула спирта — 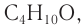
Ответ:
Пример 4.
При гидратации алкена массой 22,68 г получили вторичный насыщенный одноатомный спирт массой 32,40 г. Определите молекулярную формулу спирта, составьте структурную формулу и назовите спирт по номенклатуре ИЮПАК.
Решение
1. Анализ уравнения реакции гидратации, записанного в общем виде, показывает, что для гидратации алкена химическим количеством 1 моль требуется вода химическим количеством 1 моль. Следовательно, разница масс алкена и спирта и есть масса присоединенной воды:
2. Определяем химическое количество воды и спирта, далее молярную массу и молекулярную формулу спирта:
Следовательно,
Решая уравнение 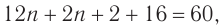
Молекулярная формула спирта — 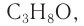
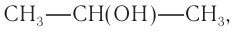
Ответ:
Пример 5.
Определите молекулярную формулу органического вещества, относительная плотность паров которого по гелию равна 22, если при сгорании его массой 19,36 г образовались углекислый газ объемом (н. у.) 2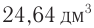
Решение
1. Определяем молярную массу неизвестного вещества, его химическое количество, а также химические количества образовавшихся оксида углерода (IV) и воды:
2. Проанализируем схему реакции горения вещества, предположив, что сожгли углеводород химическим количеством 1 моль. На основе данных о продуктах реакции рассчитаем количественный состав вещества:
Формула вещества —
3. Молярная масса вещества 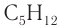
Ответ:
Многоатомные спирты
Строение: Производные углеводородов, в молекулах которых два и более атомов водорода у соседних атомов углерода замещены на гидроксильные группы, называют многоатомными спиртами.
Гидроксильные группы во всех устойчивых многоатомных спиртах связаны с соседними атомами углерода.
Простейшим представителем двухатомных спиртов (гликолей) является этиленгликоль, структурная формула которого:
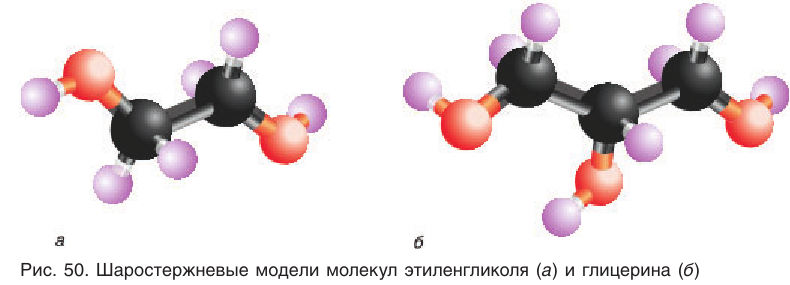
Шаростержневая модель молекулы этиленгликоля приведена на рисунке 50, а.
Простейшим представителем трехатомных спиртов (глицеринов) является глицерин (от греч. glykeros — сладкий), структурная формула которого:
Шаростержневая модель молекулы глицерина приведена на рисунке 50, б.
На примере этих двух спиртов вы познакомитесь с основными характеристиками многоатомных спиртов.
Номенклатура: По номенклатуре ИЮНАК двухатомный спирт 
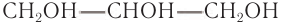
Физические свойства: Этиленгликоль и глицерин — бесцветные вязкие жидкости, тяжелее воды, неограниченно растворимы в воде, хорошо растворяются в этаноле. Эти свойства присущи и другим многоатомным спиртам.
Этиленгликоль ядовит, его водные растворы не кристаллизуются при низких температурах, что позволяет применять его как компонент незамерзающих жидкостей — антифризов. Глицерин имеет сладковатый вкус, гигроскопичен, нелетуч.
Впервые глицерин был получен из оливкового масла шведским химиком и фармацевтом К. Шееле в 1783 г.
Хорошая растворимость этиленгликоля и глицерина в воде объясняется наличием межмолекулярных водородных связей между молекулами спиртов и воды. Число таких связей больше, чем у одноатомных спиртов, из-за большего числа гидроксильных групп в молекулах.
Температуры кипения этих спиртов по сравнению с одноатомными спиртами с таким же числом атомов угелерода в молекуле намного выше:
Причиной более высоких температур кипения многоатомных спиртов является большее число межмолекулярных водородных связей между молекулами спиртов за счет большего числа гидроксильных групп в составе молекул.
Химические свойства: Для этиленгликоля и глицерина характерны все реакции одноатомных спиртов, обусловленные наличием функциональной группы —ОН, и особые свойства, обусловленные одновременным присутствием в молекуле нескольких гидроксильных групп.
1) Взаимодействие со щелочными металлами. Многоатомные спирты реагируют с активными металлами с образованием соединений, которые по аналогии с алкоголятами называют гликолятами и глицератами. Названия «гликоляты» и «глицераты» допускаются в номенклатуре ИЮНАК.
В реакциях могут участвовать одна или более гидроксильных групп. Многоатомные спирты, как и одноатомные, проявляют кислотные свойства в реакциях со щелочными металлами.
2) Взаимодействие с основаниями. В отличие от одноатомных спиртов, этиленгликоль и глицерин реагируют не только со щелочными металлами, но и с нерастворимыми гидроксидами тяжелых металлов. Такие реакции возможны для многоатомных спиртов, потому что из-за взаимного влияния гидроксильных групп в молекуле их кислотность выше, чем у одноатомных спиртов.
Если в стакан с раствором щелочи добавить несколько капель раствора сульфата меди(II) и к образовавшемуся гидроксиду меди(II) прилить многоатомный спирт, например глицерин, то образуется прозрачный раствор ярко-синего цвета (рис. 51). Цвет раствора обусловлен образованием комплексного соединения меди.
Реакция со свежеприготовленным гидроксидом меди(II) является качественной реакцией на многоатомные спирты с гидроксильными группами, находящимися у соседних атомов углерода. Из-за сложности строения образовавшегося глицерата меди уравнение реакции не приводится.
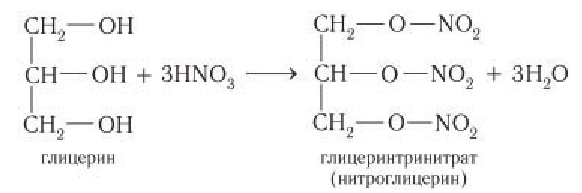
3) Образование сложных эфиров. Для многоатомных спиртов, как и для одноатомных, характерно образование сложных эфиров при взаимодействии с кислородсодержащими минеральными кислотами и карбоновыми кислотами. В частности, в реакции глицерина с избытком азотной кислоты в присутствии каталитических количеств серной кислоты образуется глицеринтринитрат, известный под названием нитроглицерин:
Название «нитроглицерин» относится к тривиальным названиям, оно не отражает строение вещества. Известно, что в химии к нитросоединениям относят вещества, в которых группа —
Реакцию глицерина с карбоновыми кислотами е образованием сложных эфиров вы будете рассматривать при изучении темы «Жиры».
Получение: Двухатомные и трехатомные спирты можно получать теми же способами, что и одноатомные спирты. В качестве исходных веществ используются алкены и галогеналканы.
Лабораторные способы: Общим способом получения гликолей является окисление алкенов раствором перманганата калия в слабощелочной или нейтральной среде:
Этиленмиколь также получают гидролизом соответствующего дигалогеналкана:
Промышленные способы. Глицерин получают в процессе гидролиза жиров и синтетическим способом из пропена, образующегося при крекинге нефтепродуктов.
Этиленгликоль в промышленных масштабах получают гидратацией эпоксида 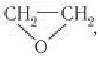
Применение: Этиленгликоль используют для синтеза полимерных материалов, синтетических волокон, например лавсана; в качестве антифризов (от анти — против и англ. freeze — морозить, замерзать) — жидкостей, добавляемых в воду, чтобы понизить температуру замерзания. Антифризы заливаются в системы охлаждения, в частности автомобильных двигателей. Температура замерзания антифриза с объемной долей этиленгликоля 52,5 % равна -40 °С. Этиленгликоль применяют для получения пластификаторов (смягчителей), используемых в лакокрасочной промышленности.
Применение глицерина основано на его гигроскопичности. Его используют для приготовления мазей, в кожевенном производстве — для предохранения кож от высыхания, в текстильной промышленности — для отделки тканей с целью придания им мягкости и эластичности и др. Глицерин применяют при изготовлении косметики, где он играет роль смягчающего и успокаивающего средства; как добавку к зубной пасте, клеям, чтобы предохранить их от быстрого высыхания; для приготовления антифризов.
Незамерзание клеточной жидкости иногда объясняют усиленной выработкой глицерина в растительных клетках.
Большое количество глицерина идет на получение нитроглицерина, который служит сырьем при производстве бездымных порохов и динамита.
Нитроглицерин токсичен, но в малых дозах используется как лечебное средство, так как расширяет кровеносные сосуды сердечной мышцы и тем самым улучшает кровоснабжение сердца.
Многоатомными спиртами называют производные углеводородов, в молекулах которых содержится несколько гидроксильных групп, связанных с соседними атомами углерода.
Многоатомные спирты взаимодействуют с активными металлами, щелочами, гидроксидами тяжелых металлов, кислородсодержащими неорганическими кислотами и карбоновыми кислотами.
Реакция с гидроксидом меди(II) используется для качественного обнаружения многоатомных спиртов.
Этиленгликоль применяют для получения синтетического волокна лавсан, в качестве антифриза; глицерин используется во многих отраслях промышленности.
- Фенолы в химии
- Альдегиды в химии
- Карбоновые кислоты в химии
- Сложные эфиры в химии
- Теория химического строения органических соединений А. М. Бутлерова
- Насыщенные углеводороды
- Ненасыщенные углеводороды
- Ароматические углеводороды
CharChem
:
Система описания химических формул для WEB.
Химические формулы для «чайников»
Научно-популярная статья о химических формулах.
Изначально сайт был задуман, как ресурс для профессиональных химиков. Содержание Структурные формулы — это просто!
Я думаю, что знакомство с формулами лучше всего начать со структурных формул органических веществ. Перед нами структурная формула метана — самого простого органического вещества. H-C-H;H|#2|H
Что мы видим? В центре латинская буква C, а от неё четыре палочки, на концах которых четыре латинских буквы H.
Структурные формулы могут слегка менять свой внешний вид.
H-C-H; H|#2|H = Все эти картинки означают одно и то же. И считаются одинаковыми формулами.
В общем, структурные формулы не являются какими-то жесткими конструкциями.
Но в химии приняты не только структурные формулы. И здесь мы познакомимся с некоторыми из них. CH4
Палочки исчезли, а вместо четырёх букв H осталась одна, но с маленькой цифрой 4, которая указывает количество атомов.
Стоит упомянуть, что метан — это природный газ, который знаком всем, у кого есть газовая плита. Углеводороды
Прежде, чем мы начнём знакомство с многочисленными органическими соединениями, хочу напомнить —
Здесь представлены органические вещества, называемые углеводородами.
Теперь посмотрим на колонку, где представлены упрощённые структурные формулы.
Некоторые функциональные группы получают собственные названия и даже специальные обозначения. Двойные и тройные связи
Итак, за короткое время мы уже разобрались, что такое структурные формулы и выяснили, что они бывают развёрнутые и упрощённые.
Представленные здесь вещества тоже относятся к углеводородам.
Кроме того, появились дополнительные названия. Тут тоже нет ничего страшного. Циклические углеводороды
Продолжим знакомство с формулами углеводородов. Они ещё не раскрыли нам всех своих секретов.
Изомеры
До сих пор мы не особенно обращали внимания на последнюю колонку, где выведены брутто-формулы.
В химии существует такое понятие как изомеры. Классическими изомерами среди углеводородов можно назвать бутан и изобутан. Посмотрим на их формулы:
Изобутан является изомером бутана. Обратите внимание, что брутто-формулы одинаковы.
Как видно, разнообразие углеводородов не перестаёт удивлять.
А у вещества декан, имеющего формулу C10H22, существует 75 изомеров.
Обратите внимание, что научное название зависит от числа звеньев в прямой цепочке, Бензол и скелетные формулы
Думаю, что пора познакомиться ещё с одним весьма примечательным представителем углеводородов.
Чем же этот бензол так примечателен? Дело в том, что это шестиугольное колечко входит в состав огромного
Конечно, скелетные формулы не так просты, как развёрнутые, но зато их гораздо легче записывать. Давайте посмотрим, как выглядят формулы других веществ, производных от бензола.
Как видите, появился ещё и смешанный вариант. Опять какой-то новый вид формул? На этот раз уже нет. А вот скелетная формула углеводорода, который называется коронен. Причём, другие варианты здесь уже использовать нет смысла. |/`/|«/|`|«|/`/«||/\/\|||`/|`//«/`\`|/`/«||/
Впечатляет? Но это далеко не самая сложная структура для органического вещества.
Скелетные формулы существуют не только для циклических молекул.
Трехмерные изображения
Иногда плоского изображения становится недостаточно.
В качестве примера посмотрим на формулы уже известных нам углеводородов:
Конечно, здесь потребуется включать воображение, чтобы представить трёхмерную структуру. Формулы с окружностью
Думаю, что стоит упомянуть ещё одну интересную конструкцию, которая нередко встречается при изображении циклических структур. /\|`//«|| <-> /=`//`-`\ <-> //||`/`\`| <-> /|`/«|_o <-> H|</H>|<H>`/<|H>`<`/H>`|<`H>/_o
Само собой, все они означают одно и то же. Но первые три отличаются только поворотом вокруг собственного центра.
Формулы бензола, где используется чередование одинарных и двойных связей называются формулами Кекуле в честь немецкого учёного,
На самом деле, среди химиков нет единого мнения по поводу того, насколько правильно использование формул с кружком. Вот пара примеров записи уже для уже знакомых нам веществ:
Знакомство с кислородом. Спирты
До сих пор мы знакомились со структурными формулами углеводородов, которые состоят только из углерода и водорода.
Кислород — очень распространённый элемент на нашей планете.
Не правда ли, что в этом есть что-то знакомое? Метан — метанол, этан — этанол, пропан — пропанол.
Все спирты можно описать в виде обобщённой формулы {R}-OH,
Конечно же стоит упомянуть, что этанол — это тот самый спирт, который входит в состав алкогольных напитков.
Ещё здесь из четырёх спиртов есть два изомера: 1-пропанол и 2-пропанол.
CH3-CH2-CH2-OH = $slope(45)CH3CH2CH2OH = CH3|CH2|CH2|OH = HO/CH2/CH2/CH3 = Поэтому первый номер — тот, который ближе к гидроксильной группе.
Все спирты, с которыми мы уже успели познакомиться, имеют в своём составе одну гидроксильную группу.
Ну и чтобы завершить знакомство со спиртами, приведу ещё формулу другого известного вещества — холестерина.
|`/`\`|<`|w>«/|<`/w$color(red)HO$color()>/`|0/`|/<`|w>|_q_q_q<-dH>:a_q|0<|dH>`/<`|wH>`|dH; Гидроксильную группу в нём я обозначил красным цветом. Карбоновые кислоты
Любой винодел знает, что вино должно храниться без доступа воздуха. Иначе оно скиснет.
Отличительной особенностью органических кислот является наличие карбоксильной группы (COOH),
Все, кто пробовал уксус, знают что он весьма кислый. Причиной этого является наличие в нём уксусной кислоты.
Карбоновые кислоты могут иметь несколько карбоксильных групп. В пищевых продуктах содержится немало других органических кислот. Вот только некоторые из них:
Название этих кислот соответствует тем пищевым продуктам, в которых они содержатся. Радикалы
Радикалы — это ещё одно понятие, которое оказало влияние на химические формулы.
Выше по тексту уже несколько раз упоминались обобщённые формулы: спирты — {R}-OH и
Если выражаться более определённо, то одновалентным радикалом называется часть молекулы, лишённая одного атома водорода.
Радикалы в химии получили собственные названия.
Думаю, что здесь всё понятно. Хочу только обратить внимание на колонку, где приводятся примеры спиртов.
Существует ещё такое явление, как свободные радикалы. Знакомство с азотом. Амины
Предлагаю познакомиться с ещё одним элементом, который входит в состав многих органических соединений. Это азот. Посмотрим, какие вещества получаются, если к знакомым нам углеводородам присоединить азот:
Как Вы уже наверное догадались из названий, все эти вещества объединяются под общим названием амины.
В общем, никаких особых новшеств здесь нет. Рациональные формулы
Не следует делать вывод о том, что неорганическая химия проще, чем органическая.
Так вот, ничего этого я рассказывать не буду. Тема моей статьи — химические формулы.
Для начала, познакомимся с ещё одним элементом — кальцием. Это тоже весьма распространённый элемент.
При первом взгляде можно заметить, что рациональная формула является чем то средним между структурной и брутто-формулой.
Кальций в чистом виде — это мягкий белый металл. В природе он не встречается. 2Ca + O2 -> 2CaO
Цифра 2 перед формулой вещества означает, что в реакции участвуют 2 молекулы. CaO + H2O -> Ca(OH2)
Получается гидроксид кальция. Если присмотреться к его структурной формуле (в предыдущей таблице), то видно,
Но и гидроксид кальция не встречается в природе из-за наличия в воздухе углекислого газа. CO2 + H2O <=> H2CO3 Знак <=> говорит о том, что реакция может проходить в обе стороны при одинаковых условиях.
Таким образом, гидроксид кальция, растворённый в воде, вступает в реакцию с угольной кислотой Ca(OH)2 + H2CO3 -> CaCO3″|v» + 2H2O
Стрелка вниз означает, что в результате реакции вещество выпадает в осадок. CaCO3 + CO2 + H2O <=> Ca(HCO3)2
Этот процесс влияет на жесткость воды.
Из карбоната кальция в значительной степени состоят мел, известняк, мрамор, туф и многие другие минералы.
Этот небольшой рассказ о круговороте кальция в природе должен пояснить, для чего нужны рациональные формулы.
Кроме того, отдельные элементы — Ca, H, O(в оксидах) — тоже являются самостоятельными группами. Ионы
Думаю, что пора знакомиться с ионами. Это слово наверняка всем знакомо.
В общем, природа химических связей обычно заключается в том, что одни элементы отдают электроны, а другие их получают. H2O <=> H^+ + OH^-
Здесь мы видим, что в результате электролитической диссоциации вода распадается на положительно заряженный H2CO3 = H^+ + HCO3^- <=> 2H^+ + CO3^2- Карбонат-ион имеет заряд 2-. Это означает, что к нему присоединились два электрона.
Отрицательно заряженные ионы называются анионы. Обычно к ним относятся кислотные остатки.
И вот здесь наверное можно полностью понять смысл рациональных формул. В них сначала записывается катион, а за ним — анион.
Вы наверное уже догадываетесь, что ионы можно описывать не только рациональными формулами. O^-|O`|/OH
Здесь заряд указан непосредственно возле атома кислорода, который получил лишний электрон, и поэтому лишился одной чёрточки. NH3 + H2O <=> NH4^+ + OH^- То же самое, но с использованием структурных формул: H|N<`/H>H + H-O-H <=> H|N^+<_(A75,w+)H><_(A15,d+)H>`/H + O`^-# -H
В правой части мы видим два иона.
2H|N^+<`/H><_(A75,w+)H>_(A15,d+)H + O^-C|O`|/O^- <=>
Но в таком виде уравнение реакции дано в демонстрационных целях. 2NH4^+ + CO3^2- <=> (NH4)2CO3 Система Хилла
Итак, можно считать, что мы уже изучили структурные и рациональные формулы.
В принципе, рациональная формула угольной кислоты вполне может считаться истинной формулой,
Вместо заключения мне хотелось бы рассказать о системе CharChem.
Зачем вообще нужна какая-то система для вывода формул?
Рациональные и брутто-формулы вполне можно изобразить при помощи текста. H H
| |
H-C-C-O-H
| |
H H
Выглядит конечно не очень красиво, но тоже осуществимо.
Настоящая проблема возникает при попытке изобразить бензольные кольца и при использовании скелетных формул.
Система CharChem позволяет хранить все формулы прямо в HTML-документе в текстовом виде. По-моему, это очень удобно.
Таким образом, для подготовки этой статьи я пользовался только текстовым редактором. Вот несколько примеров, раскрывающих секрет подготовки текста статьи:
Описания из левого столбца автоматически превращаются в формулы во втором столбце. Здесь есть гораздо более подробная документация по использованию системы CharChem. На этом разрешите закончить статью и пожелать удачи в изучении химии. Краткий толковый словарь использованных в статье терминов
|
План урока:
Формула и строение спиртов
Классификация спиртов
Номенклатура спиртов
Изомерия спиртов
Методы получения спиртов
Физические свойства
Химические свойства
Применение спиртов
Формула и строение спиртов
Спирты из-за наличия функциональной группы -ОН можно рассматривать как производное воды Н-О-Н. Геометрическое строение воды и спиртов схоже. Угол связи R-O-H равен 109˚, при этом гидроксильный кислород находится в состоянии sp3-гибридизации.
Строение молекулы спирта
У спиртов особенное электронное строение. Алкоголи – дипольные молекулы, которые содержат связи C-H, C-O, O-H. Атом кислорода имеет частично отрицательный заряд, а атомы углерода и водорода – частично положительный. Связь О-Н имеет большую полярность, по сравнению со связью С-О. Это явление связано с разностью электроотрицательности кислорода и водорода. Но полярность связей недостаточна для диссоциации и образования ионов Н+. Поэтому можно сделать вывод, что спирты – неэлектролиты.
Формула спиртов: CnH2n+1OH
Классификация спиртов
В классификации спиртов заключены особенности строения молекул. По числу гидроксильных групп различают одноатомные, двухатомные, трехатомные и многоатомные спирты.
Также спирты классифицируют в зависимости от положения гидроксильной группы на первичные, вторичные и третичные.
Номенклатура спиртов
Для спиртов свойственно несколько типов номенклатуры.
- Тривиальная (историческая) номенклатура. Для простых спиртовых соединений свойственны упрощенные названия. В этом случае название радикала переводят в прилагательное с помощью окончания «овый» и добавляют слово «спирт». Например, CH3-CH2-CH2-OH – пропановый спирт.
У первых двух представителей гомологического ряда есть особенные исторические названия. Метанол – древесный спирт, а этанол – винный. Такие названия обусловлены историческим методом получения. Опьяняющие свойства этанола были известны не менее чем за 8000 лет до н.э.
- Систематическая номенклатура спиртов. Как правило, в химии используют именно этот вид номенклатуры. В одноатомных спиртах к названию радикала добавляется суффикс «ол», в двухатомных – «диол», в трехатомных – «триол». Положение гидроксигруппы обозначается наименьшим значением, если в составе спирта отсутствует карбонильная и/или карбоксильная группа.
Алгоритм названия спиртов
Систематическая номенклатура подчиняется определенному алгоритму.
- Выбор главной цепи в соединении.
- Нумерация начинается с того конца, к которому ближе функциональная группа.
- Название углеводородного радикала.
- Прибавление окончания «ол» и указание номера атома углерода, с которым связана гидроксогруппа.
Изомерия спиртов
Для спиртов свойственно несколько видов изомерии – изомерия углеродного скелета, положения заместителя и межклассовая (с простыми эфирами). Изомерия углеродного скелета начинается с бутанола.
Типы изомерии спиртов
Способы получения спиртов
Существует несколько реакций получения спиртов.
Реакция проходит по правилу Марковникова, т.е. атом водорода присоединяется к более гидрированному атому углерода, а гидроксильная группа – к менее. Например, в молекуле CH3-CH2-CH=CH2 атом водорода Н+ примыкает к атому углерода, стоящему в СН2 у кратной связи, а гидроксильная группа ОН— – к СН.
Физические свойства
Физические свойства определяются особенностями строения молекулы спирта. Алкоголи – бесцветные жидкости с характерным запахом. Температуры плавления и кипения спиртов выше, чем у соответствующих представителей других классов веществ. По гомологическому ряду они увеличиваются.
Все алкоголи имеют плотность ниже единицы, т.е. они плавают на поверхности воды. Спирты растворимы в большинстве органических растворителях.
Особенность алкоголей заключается в том, что в гомологическом ряде нет газов. Агрегатное состояние спиртов – жидкое или твердое. Это связано с тем, что атом кислорода в гидроксильной группе обладает частично отрицательным зарядом, а атом водорода – частично положительным. Кислород притягивает положительно заряженные атомы и образует с ними водородные связи. Большое количество таких связей обеспечивает «прилипание» молекул спирта между собой и обуславливает особенное строение.
Из этилового спирта изготавливают алкогольные напитки. Несмотря на относительную безопасность употребления этанола, его систематическое употребление пагубно влияет на организм:
- 100 мл пива – гибель 3000 клеток головного мозга,
- 100 мл вина – гибель 5000 клеток головного мозга,
- 100 мл водки – гибель 7500 клеток головного мозга.
В алкогольные напитки вместо этанола могут добавлять метанол, который опасен для жизни. Эти два спирта отличаются по характеру пламени:
- метиловый горит зеленым пламенем,
- этиловый – синим.
Но при наличии примесей в метаноле, зеленое пламя может и не появиться.
Химические свойства
Реакции замещения
- Замещение водорода в гидроксильной группе
- Взаимодействие с активными металлами (например, с натрием)
Реакция проводится в безводной среде. В воде алкоголяты металлов полностью гидролизуются.
2CH3-CH2-O[H] + 2Na → 2CH3-CH2-ONa + H2
- Взаимодействие с кислотами (этерификация)
CH3-O[H + HO]-NO2→ CH3-O-NO2 + H2O
- Замещение гидроксигруппы
- Взаимодействие с галогеноводородами при нагревании
CH3-CH2-[OH + H]Br→ CH3-CH2-Br + H2O
- Взаимодействие с аммиаком
Реакция идет при пропускании смеси паров спирта с аммиаком при 300˚С над оксидом алюминия.
CH3-CH2-[OH +H]-NH2→CH3-CH2-NH2 + H2O
При избытке в спирте алкильных радикалов в молекуле аммиака могут замещаться два или три атома водорода.
2CH3-CH2-[OH + H]-NH2 → C2H5-NH-C2H5 + 2H2O
Реакции отщепления
- Дегидратация
- Межмолекулярная дегидратация в присутствии концентрированной серной кислоты и при 140˚С
CH3-CH2-O[H + НО]-СН2-СН3→С2Н5-О-С2Н5 + Н2О
CH3-O[H + HO]-CH2-CH3→ CH3-O-C2H5 + H2O
- Внутримолекулярная дегидратация в присутствии концентрированной серной кислоты и при 170˚С
OH]-CH2-CH2-[H →CH2=CH2 + H2O
Для метанола не характерна внутримолекулярная дегидратация. Реакция вторичных и третичных спиртов проходит по правилу Зайцева. Т.е. при отщеплении воды от спирта атом водорода отрывается от соседнего менее гидрированного атома углерода. Например, в молекуле CH3-CH2-CH(OH)-CH3 атом водорода Н+ отщепляется от атома углерода в СН3, находящегося вблизи гидроксильной группы.
CH3-CH(OH)-CH2-CH3→CH3-CH=CH-CH3 + H2O
- Дегидрирование в присутствии катализатора меди и под действием нагревания
Реакции окисления
- Полное окисление (горение)
CH3-CH2-OH + 3О2→ 2СО2 + 3Н2О
Неполное окисление
Качественная реакция на многоатомные спирты
Качественная реакция – химическое превращение, которое сопровождается характерными признаками. С ее помощью можно распознать определенное вещество.Строение многоатомных спиртов, т.е. присутствие в молекуле нескольких гидроксильных групп, обуславливает образование при взаимодействии со свежеполученным осадком гидроксида меди (II) растворимых в воде комплексов василькового цвета.
Строение одноатомных спиртов такая качественная реакция не подтверждает.
Применение спиртов
Метанол, или древесный спирт, опасен для употребления. Он был получен путем перегонки твердых древесных пород. Этот одноатомный спирт недобросовестные производители алкогольных напитков применяют вместо этанола, что провоцирует гибель потребителей. Древесный спирт в организме под влиянием фермента алкогольдегидрогеназы преобразуется в формальдегид и муравьиную кислоту, которые провоцируют слепоту. 50 мл метанола – смертельная доза. Метанол непросто отличить от этанола, т.к. они имеют схожий запах и вид.
Применение метилового спирта
Области применения этилового спирта разнообразны. Этиловый спирт используют в получении синтетического каучука, лекарственных препаратов и применяют как растворитель. Этанол используется в изготовлении алкоголя. При попадании в организм он снижает болевые ощущения, уменьшает торможения в коре головного мозга, ускоряет мочеобразование, провоцирует расширение кровеносных сосудов. При больших количествах этанола происходит его окисление до ацетальдегида, что вызывает тяжелые отравления.
При систематическом употреблении алкоголя снижается работоспособность головного мозга, а клетки печени погибают. Дети и подростки, употребляющие алкоголь, подвержены инфекционным заболеваниям. Продолжительность жизни пьющих людей меньше на 10-12 лет по сравнению с людьми, ведущих здоровый образ жизни.
Применение этилового спирта.
Практическое применение трехатомный спирт глицерин нашел в косметической, медицинской и пищевой промышленности. Он смягчает и успокаивает кожу. Также глицерин входит в состав зубной пасты, что предотвращает ее высыхание.
Применение глицерина
Многоатомный спирт глицерин также применяют в промышленной отрасли для предотвращения кристаллизации продуктов. Его используют как увлажнитель для табака. Он входит в состав клеев и предохраняет их от слишком быстрого высыхания.