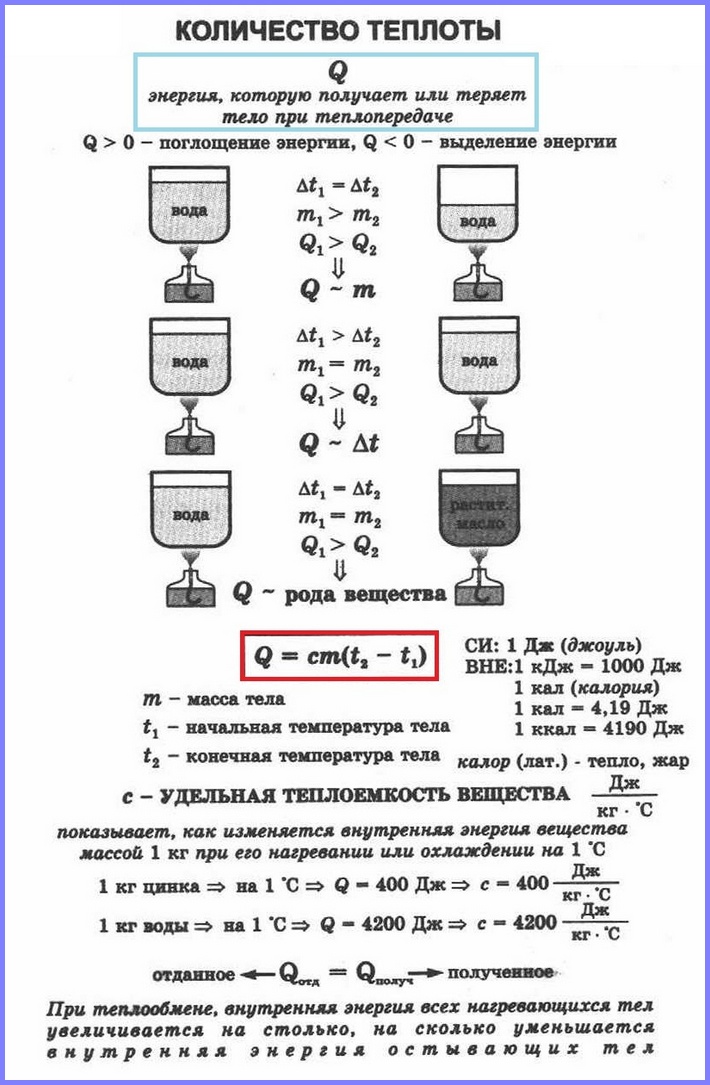
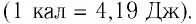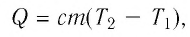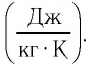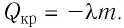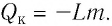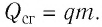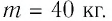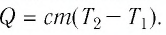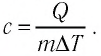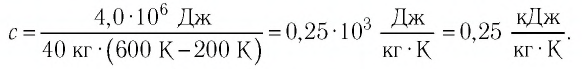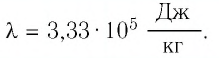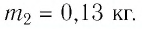Для того чтобы нагреть на определённую величину тела, взятые при одинаковой температуре, изготовленные из различных веществ, но имеющие одинаковую массу, требуется разное количество теплоты.
Пример:
для нагревания (1) кг воды на (1°C) требуется количество теплоты, равное (4200) Дж. А если нагревать (1) кг цинка на (1°C), то потребуется всего (400) Дж.
Удельная теплоёмкость вещества — физическая величина, численно равная количеству теплоты, которое необходимо передать веществу массой (1) кг для того, чтобы его температура изменилась на (1~°C).
([c]=1frac{Дж}{кг cdot °C}).
Пример:
по таблице удельной теплоёмкости твёрдых веществ находим, что удельная теплоёмкость алюминия составляет (c(Al)=920 frac{Дж}{кг cdot °C}). Поэтому при охлаждении (1) килограмма алюминия на (1) градус Цельсия ((°C)) выделяется (920) джоулей энергии. Столько же необходимо для нагревания (1) килограмма на алюминия на (1) градус Цельсия ((°C)).
Ниже представлены значения удельной теплоёмкости для некоторых веществ.
Твёрдые вещества
|
Вещество |
(c), Дж/(кг·°C) |
| Алюминий |
(920) |
| Бетон |
(880) |
| Дерево |
(2700) |
|
Железо, сталь |
(460) |
| Золото |
(130) |
| Кирпич |
(750) |
| Латунь |
(380) |
| Лёд |
(2100) |
| Медь |
(380) |
| Нафталин |
(1300) |
| Олово |
(230) |
| Парафин |
(3200) |
| Песок |
(970) |
| Платина |
(130) |
| Свинец |
(120) |
| Серебро |
(240) |
| Стекло |
(840) |
| Цемент |
(800) |
| Цинк |
(400) |
| Чугун |
(550) |
| Сера |
(710) |
Жидкости
|
Вещество |
(c), Дж/(кг·°C) |
| Вода |
(4200) |
| Глицерин |
(2400) |
| Керосин |
(2140) |
|
Масло подсолнечное |
(1700) |
|
Масло трансформаторное |
(2000) |
| Ртуть |
(120) |
|
Спирт этиловый |
(2400) |
|
Эфир серный |
(2300) |
Газы (при постоянном давлении и температуре (20°C))
|
Вещество |
(c), Дж/(кг·°C) |
| Азот |
(1000) |
| Аммиак |
(2100) |
| Водород |
(14300) |
|
Водяной пар |
(2200) |
| Воздух |
(1000) |
| Гелий |
(5200) |
| Кислород |
(920) |
|
Углекислый газ |
(830) |
Удельная теплоёмкость реальных газов, в отличие от идеальных газов, зависит от давления и температуры. И если зависимостью удельной теплоёмкости реальных газов от давления в практических задачах можно пренебречь, то зависимость удельной теплоёмкости газов от температуры необходимо учитывать, поскольку она очень существенна.
Обрати внимание!
Удельная теплоёмкость вещества, находящегося в различных агрегатных состояниях, различна.
Пример:
вода в жидком состоянии имеет удельную теплоёмкость, равную (4200) Дж/(кг·°C), в твёрдом состоянии (лёд) — (2100) Дж/(кг·°C), в газообразном состоянии (водяной пар) — (2200) Дж/(кг·°C).
Вода — вещество особенное, обладающее самой высокой среди жидкостей удельной теплоёмкостью. Но самое интересное, что теплоёмкость воды снижается при температуре от (0°C) до (37°C) и снова растёт при дальнейшем нагревании (рис. (1)).
Рис. (1). График удельной теплоёмкости воды
В связи с этим вода в морях и океанах, нагреваясь летом, поглощает из окружающей среды огромное количество теплоты. А зимой вода остывает и отдаёт в окружающую среду большое количество теплоты. Это явление оказывает влияние на климат данного региона. Летом здесь нет изнуряющей жары, а зимой — лютых морозов.
Высокая удельная теплоёмкость воды нашла широкое применение в различных областях: от медицинских грелок до систем отопления и охлаждения.
Задумывались ли вы, почему воду используют при тушении пожаров? Из-за большой теплоёмкости. При соприкосновении с горящим предметом вода забирает у него большое количество теплоты. Оно значительно больше, чем при использовании такого же количества любой другой жидкости.
Помимо непосредственного отвода тепла, вода гасит пламя ещё и косвенным образом. Водяной пар, образующийся при контакте с огнём, окутывает горящее тело, предотвращая поступление кислорода, без которого горение невозможно.
Какой водой эффективнее тушить огонь: горячей или холодной? Горячая вода тушит огонь быстрее, чем холодная. Дело в том, что нагретая вода скорее превратится в пар, а значит, и отсечёт поступление воздуха к горящему объекту.
Источники:
Рис. 1. Автор: Epop — собственная работа. Общественное достояние, https://commons.wikimedia.org/w/index.php?curid=10750129.
Удельная теплоёмкость — это энергия, которая требуется для увеличения температуры 1 грамма чистого вещества на 1°. Параметр зависит от его химического состава и агрегатного состояния: газообразное, жидкое или твёрдое тело. После его открытия начался новый виток развития термодинамики, науки о переходных процессах энергии, которые касаются теплоты и функционирования системы.
Как правило, удельная теплоёмкость и основы термодинамики используются при изготовлении радиаторов и систем, предназначенных для охлаждения автомобилей, а также в химии, ядерной инженерии и аэродинамике. Если вы хотите узнать, как рассчитывается удельная теплоёмкость, то ознакомьтесь с предложенной статьёй.
Содержание:
- Формула
- Инструкция по расчёту параметра
- Расчёт
- Как рассчитать теплоемкость продуктов питания
- Полезные советы
- Видео
Формула
Перед тем, как приступить к непосредственному расчёту параметра следует ознакомиться с формулой и её компонентами.
Формула для расчёта удельной теплоёмкости имеет следующий вид:
- с = Q/(m*∆T)
Знание величин и их символических обозначений, использующихся при расчёте, крайне важно. Однако необходимо не только знать их визуальный вид, но и чётко представлять значение каждого из них. Расчёт удельной теплоёмкости вещества представлен следующими компонентами:
ΔT – символ, означающий постепенное изменение температуры вещества. Символ «Δ» произносится как дельта.
ΔT можно рассчитать по формуле:
ΔT = t2–t1, где
- t1 – первичная температура;
- t2 – конечная температура после изменения.
m – масса вещества используемого при нагреве (гр).
Q – количество теплоты (Дж/J)
На основании Цр можно вывести и другие уравнения:
- Q = m*цp*ΔT – количество теплоты ;
- m = Q/цр*(t2 — t1) – массы вещества;
- t1 = t2–(Q/цp*m) – первичной температуры;
- t2 = t1+(Q/цp*m) – конечной температуры.
Инструкция по расчёту параметра
Рассчитать с вещества достаточно просто и чтобы это сделать нужно, выполнить следующие шаги:
- Взять расчётную формулу: Теплоемкость = Q/(m*∆T)
- Выписать исходные данные.
- Подставить их в формулу.
- Провести расчёт и получим результат.
В качестве примера произведём расчёт неизвестного вещества массой 480 грамм обладающего температурой 15ºC, которая в результате нагрева (подвода 35 тыс. Дж) увеличилась до 250º.
Согласно инструкции приведённой выше производим следующие действия:
Выписываем исходные данные:
- Q = 35 тыс. Дж;
- m = 480 г;
- ΔT = t2–t1 =250–15 = 235 ºC.
Берём формулу, подставляем значения и решаем:
с=Q/(m*∆T)=35тыс.Дж/(480 г*235º)=35тыс.Дж/(112800 г*º)=0,31 Дж/г*º.
Расчёт
Выполним расчёт CP воды и олова при следующих условиях:
- m = 500 грамм;
- t1 =24ºC и t2 = 80ºC – для воды;
- t1 =20ºC и t2 =180ºC – для олова;
- Q = 28 тыс. Дж.
Для начала определяем ΔT для воды и олова соответственно:
- ΔТв = t2–t1 = 80–24 = 56ºC
- ΔТо = t2–t1 = 180–20 =160ºC
Затем находим удельную теплоёмкость:
- с=Q/(m*ΔТв)= 28 тыс. Дж/(500 г *56ºC) = 28 тыс.Дж/(28 тыс.г*ºC) = 1 Дж/г*ºC.
- с=Q/(m*ΔТо)=28тыс.Дж/(500 гр*160ºC)=28 тыс.Дж/(80 тыс.г*ºC)=0,35 Дж/г*ºC.
Таким образом, удельная теплоемкость воды составила 1 Дж/г *ºC, а олова 0,35 Дж/г*ºC. Отсюда можно сделать вывод о том, что при равном значении подводимого тепла в 28 тыс. Дж олово нагрется быстрее воды, поскольку его теплоёмкость меньше.
Теплоёмкостью обладают не только газы, жидкости и твёрдые тела, но и продукты питания.
Как рассчитать теплоемкость продуктов питания
При расчёте емкости питания уравнение примет следующий вид:
с=(4.180*w)+(1.711*p)+(1.928*f)+(1.547*c)+(0.908 *a), где:
- w – количество воды в продукте;
- p – количество белков в продукте;
- f – процентное содержание жиров;
- c – процентное содержание углеводов;
- a – процентное содержание неорганических компонентов.
Определим теплоемкость плавленого сливочного сыра Viola. Для этого выписываем нужные значения из состава продукта (масса 140 грамм):
- вода – 35 г;
- белки – 12,9 г;
- жиры – 25,8 г;
- углеводы – 6,96 г;
- неорганические компоненты – 21 г.
Затем находим с:
- с=(4.180*w)+(1.711*p)+(1.928*f)+(1.547*c)+(0.908*a)=(4.180*35)+(1.711*12,9)+(1.928*25,8) + (1.547*6,96)+(0.908*21)=146,3+22,1+49,7+10,8+19,1=248 кДж /кг*ºC.
Полезные советы
Всегда помните, что:
- процесс нагревания металла проходит быстрее, чем у воды, так как он обладает CP в 2,5 раза меньше;
- по возможности преобразуйте полученные результаты в более высокий порядок, если позволяют условия;
- в целях проверки результатов можно воспользоваться интернетом и посмотреть с для расчётного вещества;
- при равных экспериментальных условиях более значительные температурные изменения будут наблюдаться у материалов с низкой удельной теплоёмкостью.
Видео
Разобраться в этой теме вам поможет видео урок.
Загрузить PDF
Загрузить PDF
Удельная теплоемкость — это энергия, необходимая для того, чтобы поднять температуру одного грамма чистого вещества на один градус Цельсия. Удельная теплоемкость вещества зависит от его химического состава и агрегатного состояния. Открытие удельной теплоемкости подстегнуло развитие термодинамики, науки о переходах энергии, касающейся теплоты и работы системы. Удельная теплоемкость и термодинамика широко используются в химии, ядерной инженерии и аэродинамики, а также в повседневной жизни для радиаторов и систем охлаждения автомобилей. Если вы хотите узнать, как вычислить удельную теплоемкость, следуйте приведенной ниже инструкции.
-
1
Ознакомьтесь с величинами, которые используются для расчета удельной теплоемкости. Очень важно знать величины, которые используются для расчета удельной теплоемкости. Вы должны знать, как выглядит символ каждой величины, и понимать, что он означает. Далее приведены величины, которые обычно используются в выражении для расчета удельной теплоемкости вещества:
- Дельта, или символ «Δ», подразумевает изменение величины.
- Например, если ваша первая температура (T1) составляет 150 ºC, а вторая (T2) составляет 20 ºC, тогда ΔT, или изменение температуры, составит 150 ºC — 20 ºC = 130 ºC.
- Масса образца обозначается буквой «m».
- Количество теплоты обозначается буквой «Q». Единица измерения количества теплоты — «Дж», или Джоуль.
- «T» — это температура вещества.
- Удельная теплоемкость обозначается буквой «Cp».
- Дельта, или символ «Δ», подразумевает изменение величины.
-
2
Освойте выражение для определения удельной теплоемкости. Ознакомившись с величинами, которые используются для вычисления удельной теплоемкости, вы должны выучить уравнение для определения удельной теплоемкости вещества. Формула имеет вид: Cp = Q/mΔT.
- Вы можете оперировать этой формулой, если хотите узнать изменение количества теплоты вместо удельной теплоемкости. Вот как это будет выглядеть:
- ΔQ = mCpΔT
Реклама
- Вы можете оперировать этой формулой, если хотите узнать изменение количества теплоты вместо удельной теплоемкости. Вот как это будет выглядеть:
-
1
Изучите формулу. Сначала вам нужно изучить выражение для того, чтобы понять, что вам нужно сделать, чтобы найти удельную теплоемкость. Давайте рассмотрим следующую задачу: Определите удельную теплоемкость 350 г неизвестного вещества, если при сообщении ему 34 700 дж теплоты его температура поднялась с 22 до 173 ºC без фазовых переходов.
-
2
Запишите известные и неизвестные факторы. Разобравшись с задачей, вы можете записать все известные и неизвестные переменные, чтобы лучше понять, с чем вы имеете дело. Вот как это делается:
- m = 350 г
- Q = 34 700 Дж
- ΔT = 173 ºC — 22 ºC = 151 ºC
- Cp = неизвестно
-
3
Подставьте неизвестные факторы в уравнение. Известны все значения за исключением «Cpc», поэтому необходимо подставить в исходное уравнение все остальные факторы и найти «Cp». Делать это нужно так:
- Исходное уравнение: Cp = Q/mΔT
- c = 34 700 Дж/(350 г x 151 ºC)
-
4
Найдите ответ. Теперь, после того как вы подставили известные величины в выражение, вам осталось выполнить несколько простейших арифметических действий, чтобы узнать ответ. Удельная теплоемкость — окончательный ответ — составляет 0,65657521286 Дж/(г x ºC).
- Cp = 34,700 Дж/(350 г x 151 ºC)
- Cp = 34,700 Дж/(52850 г x ºC)
- Cp = 0,65657521286 Дж/(г x ºC)
Реклама
Советы
- Металл нагревается быстрее воды из-за низкой удельной теплоемкости.
- При нахождении удельной теплоемкости сокращайте единицы измерения тогда, когда это возможно.
- Удельную теплоемкость многих материалов можно найти в интернете для проверки вашего ответа.
- Иногда для изучения процессе теплопередачи в процессе физических или химических превращений может использоваться калориметр.
- Изменение температуры при прочих равных условиях значительнее для материалов с низкой удельной теплоемкостью.
- Системная единица СИ (Международная система единиц измерения) удельной теплоемкости — джоуль на градус Цельсия на грамм. В странах с британской системой мер она измеряется в калориях на градус Фаренгейта на фунт.
- Изучите формулу расчета удельной теплоемкости пищевых продуктов Cp = 4,180 x w + 1,711 x p + 1,928 x f + 1,547 x c + 0,908 x a — это уравнение для нахождения удельной теплоемкости, где «w» — процентное содержание воды в продукте, «p» — процентное содержание белков, «f» — процентное содержание жиров, «c» — процентное содержание углеводов и «a» — процентное содержание неорганических компонентов. Уравнение учитывает массовую долю (x) всех твердых веществ, которые составляют пищу. Расчет удельной теплоемкости приведен в кДж/(кг х K).
Реклама
Об этой статье
Эту страницу просматривали 112 744 раза.
Была ли эта статья полезной?
Содержание:
Количество теплоты:
В чём причина изменения внутренней энергии макроскопического тела при теплообмене?
Теплообмен
Другим способом изменения внутренней энергии термодинамической системы является теплообмен.
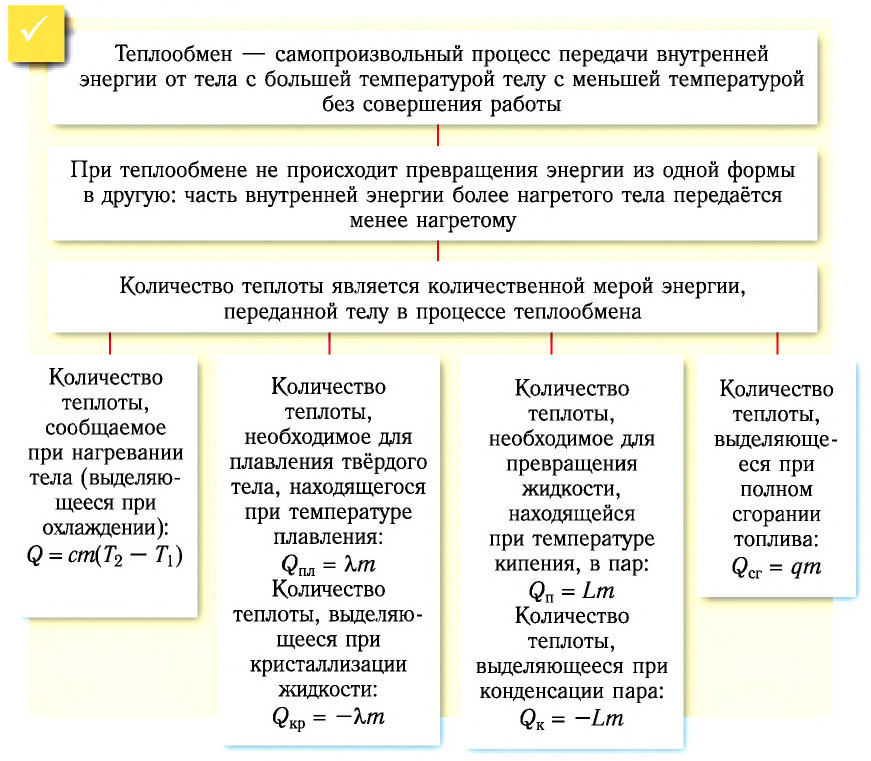
Теплообмен — самопроизвольный процесс передачи внутренней энергии от тела с большей температурой телу с меньшей температурой без совершения работы.
Теплообмен между контактирующими телами называют теплопередачей. За счёт переданной при этом энергии увеличивается внутренняя энергия одного тела и уменьшается внутренняя энергия другого. Если, например, привести в соприкосновение два тела с разными температурами, то частицы более нагретого тела будут передавать часть своей кинетической энергии частицам менее нагретого тела. В результате внутренняя энергия одного тела уменьшается, а другого увеличивается.
Таким образом, при теплопередаче не происходит превращения энергии из одной формы в другую: часть внутренней энергии более нагретого тела передаётся менее нагретому.
Количество теплоты и удельная теплоёмкость
Количественной мерой энергии, сообщённой телу (или отданной им) в процессе теплообмена, является количество теплоты.
В СИ единицей количества теплоты Q является джоуль (Дж). Иногда для измерения количества теплоты используют внесистемную единицу — калорию
Если процесс теплообмена не сопровождается изменением агрегатного состояния вещества, то
где 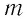
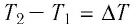
Удельная теплоёмкость зависит от свойств данного вещества и, как показывает опыт, в достаточно большом интервале температур практически не изменяется. Однако удельная теплоёмкость газа зависит от того, при каком процессе (изобарном или изохорном) осуществляется теплообмен.
Интересно знать:
Физическая величина, равная произведению массы тела на удельную теплоёмкость вещества, носит название теплоёмкость тела. Обозначают теплоёмкость С и измеряют в джоулях, деленных на кельвин 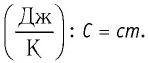
Удельная теплота плавления
Физическую величину, численно равную количеству теплоты, необходимому для превращения кристаллического вещества массой 1 кг, взятого при температуре плавления, в жидкость той же температуры, называют удельной теплотой плавления 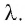
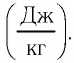
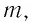
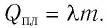
Удельная теплота парообразования
Физическую величину, численно равную количеству теплоты, которое необходимо передать жидкости массой 1 кг, находящейся при температуре кипения, для превращения её при постоянной температуре в пар, называют удельной теплотой парообразования L. Единицей измерения этой величины является джоуль, делённый на килограмм 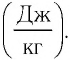
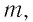
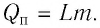
Удельная теплота сгорания топлива
Физическую величину, численно равную количеству теплоты, выделяющемуся при полном сгорании топлива массой 1 кг, называют удельной теплотой сгорания 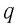
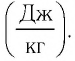
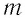
Это количество теплоты передаётся телам, образующим термодинамическую систему, и по отношению к ним является положительной величиной.
- Заказать решение задач по физике
Примеры решения задач
Пример №1
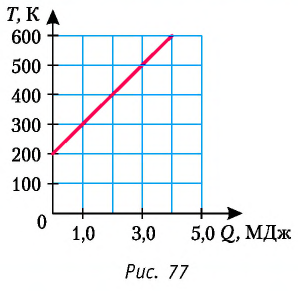
На рисунке 77 представлен график зависимости абсолютной температуры нагреваемого тела от переданного ему количества теплоты. Воспользовавшись таблицей на с. 84, определите вещество, из которого изготовлено тело, если его масса
Решение:
Для того чтобы определить вещество, из которого изготовлено тело, найдём его удельную теплоёмкость с. Анализируя график, делаем вывод, что при нагревании тела от температуры 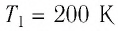
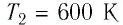
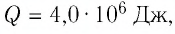
Следовательно, удельная теплоёмкость вещества
Полученное значение удельной теплоёмкости соответствует олову.
Ответ: 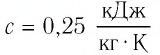
Пример №2
В налитую в сосуд воду, масса которой 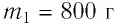
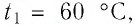
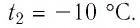
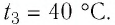
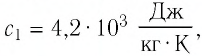
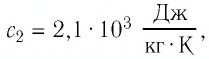
Решение:
Ответ:
- Расчет количества теплоты при нагревании и охлаждении
- Удельная теплота сгорания топлива
- Плавление и кристаллизация в физике
- Испарение жидкостей в физике
- Конвекция в физике
- Излучение тепла в физике
- Виды излучений в физике
- Инфракрасные излучения
«Количество теплоты. Удельная теплоёмкость»
Количество теплоты
Изменение внутренней энергии путём совершения работы характеризуется величиной работы, т.е. работа является мерой изменения внутренней энергии в данном процессе. Изменение внутренней энергии тела при теплопередаче характеризуется величиной, называемой количествоv теплоты.
Количество теплоты – это изменение внутренней энергии тела в процессе теплопередачи без совершения работы. Количество теплоты обозначают буквой Q.
Работа, внутренняя энергия и количество теплоты измеряются в одних и тех же единицах — джоулях (Дж), как и всякий вид энергии.
В тепловых измерениях в качестве единицы количества теплоты раньше использовалась особая единица энергии — калория (кал), равная количеству теплоты, необходимому для нагревания 1 грамма воды на 1 градус Цельсия (точнее, от 19,5 до 20,5 °С). Данную единицу, в частности, используют в настоящее время при расчетах потребления тепла (тепловой энергии) в многоквартирных домах. Опытным путем установлен механический эквивалент теплоты — соотношение между калорией и джоулем: 1 кал = 4,2 Дж.
При передаче телу некоторого количества теплоты без совершения работы его внутренняя энергия увеличивается, если тело отдаёт какое-то количество теплоты, то его внутренняя энергия уменьшается.
Если в два одинаковых сосуда налить в один 100 г воды, а в другой 400 г при одной и той же температуре и поставить их на одинаковые горелки, то раньше закипит вода в первом сосуде. Таким образом, чем больше масса тела, тем большее количество тепла требуется ему для нагревания. То же самое и с охлаждением.
Количество теплоты, необходимое для нагревания тела зависит еще и от рода вещества, из которого это тело сделано. Эта зависимость количества теплоты, необходимого для нагревания тела, от рода вещества характеризуется физической величиной, называемой удельной теплоёмкостью вещества.
Удельная теплоёмкость
Удельная теплоёмкость – это физическая величина, равная количеству теплоты, которое необходимо сообщить 1 кг вещества для нагревания его на 1 °С (или на 1 К). Такое же количество теплоты 1 кг вещества отдаёт при охлаждении на 1 °С.
Удельная теплоёмкость обозначается буквой с. Единицей удельной теплоёмкости является 1 Дж/кг °С или 1 Дж/кг °К.
Значения удельной теплоёмкости веществ определяют экспериментально. Жидкости имеют большую удельную теплоёмкость, чем металлы; самую большую удельную теплоёмкость имеет вода, очень маленькую удельную теплоёмкость имеет золото.
Поскольку кол-во теплоты равно изменению внутренней энергии тела, то можно сказать, что удельная теплоёмкость показывает, на сколько изменяется внутренняя энергия 1 кг вещества при изменении его температуры на 1 °С. В частности, внутренняя энергия 1 кг свинца при его нагревании на 1 °С увеличивается на 140 Дж, а при охлаждении уменьшается на 140 Дж.
Количество теплоты Q, необходимое для нагревания тела массой m от температуры t1°С до температуры t2°С, равно произведению удельной теплоёмкости вещества, массы тела и разности конечной и начальной температур, т.е.
Q = c ∙ m (t2 — t1)
По этой же формуле вычисляется и количество теплоты, которое тело отдаёт при охлаждении. Только в этом случае от начальной температуры следует отнять конечную, т.е. от большего значения температуры отнять меньшее.
Это конспект по теме «Количество теплоты. Удельная теплоёмкость». Выберите дальнейшие действия:
- Перейти к следующему конспекту: «Уравнение теплового баланса»
- Вернуться к списку конспектов по Физике
- Посмотреть решение типовых задач на количество теплоты