Теплота сгорания газов
Теплота сгорания, или теплотворная
способность газа как топлива, — это
количество теплоты, выделяемой при
полном сгорании единицы количества
вещества (кг или м),
измеренного при нормальных стандартных
условиях (давление, температура).
Различают высшую
и низшую
теплоту сгорания. Высшей теплотой
сгорания называется количество теплоты
(кДж), выделяющееся при полном сгорании
единицы количества вещества (кг или
м),
с учетом конденсации водяных паров,
образующихся при окислении водорода.
Низшей теплотой сгорания называется
количество теплоты (кДж), выделяющееся
при полном сгорании единицы количества
вещества при нормальных или стандартных
условиях без учета теплоты, выделяющейся
при конденсации водяных паров. На основе
численного значения теплоты сгорания
топлива определяют потребность в
газообразном топливе, а также КПД
газоперекачивающих агрегатов и других
газоиспользующих установок.
В расчетах обычно используют понятие
низшей теплоты сгорания топлива в силу
того, что отходящие из газоиспользующих
установок продукты сгорания имеют
относительно высокую температуру,
значительно выше, чем температура точки
росы, при которой и происходит конденсация
водяных паров, содержащихся в продуктах
сгорания.
Численные значения низшей теплоты
сгорания ряда компонентов газообразного
топлива приведены в табл. 1.3.
Следует заметить, что приводимые в
литературе данные о теплоте сгорания
отдельных компонентов газообразного
топлива часто разнятся между собой. Это
в определенной степени обусловлено
различием в подсчете основных характеристик
самого топлива.
Таблица 1.3
Низшая теплота сгорания некоторых компонентов природного газа
|
#G0Компонент |
Метан СН |
Этан С |
Пропан С |
Бутан С |
Пентан С |
Гексан С |
|
Низшая |
35880 |
64450 |
92940 |
118680 |
146130 |
173760 |
Пример 1.2. Определить низшую теплоту
сгорания природного газа, имеющего
следующее процентное содержание
компонентов: метана СН=
94%; этана СН
=
3%; пропана СН
= 1,5%; бутана С
Н
= 1%; пентана С
Н
=
0,5%.
Решение. Расчет низшей теплоты сгорания
топлива проводится по формуле:
,
где
—
теплота сгорания компонентов смеси;
—
процентное содержание компонентов
смеси.
Применительно к данному случаю получим:
=
35880·0,94 + 64450·0,03 + 92949·0,015 + 118680·0,01 +146130·0,005
= 38672 кДж/м.
Переход к определению массовой теплоты
сгорания топлива (кДж/кг) осуществляется
с использованием плотности газа в данных
условиях [,кДж/кг
= (
кДж/м
)
/,
кг/м].
Пересчет теплоты сгорания газа от
нормальных условий к стандартным
проводится по формуле:
(20°С)
=(0°С)
.
Согласно существующим требованиям,
номинальная низшая теплота сгорания
топлива при проведении теплотехнических
расчетов в системе газовой промышленности
принимается равной 34541 кДж/м.
Страница содержит калькуляторы:
-
- расчет низшей теплотворной способности (теплоты сгорания) природного газа при стандартных условиях;
- расчет числа Воббе природного газа при стандартных условиях.
Расчет низшей теплотворной способности (теплоты сгорания) природного газа при стандартных условиях.
Расчет числа Воббе природного газа при стандартных условиях.
Общие данные.
При известном составе природного газа рассчитать низшую теплотворную способность и число Воббе при различных стандартных условиях (при 0 или 20 град. Цельсия) можно на калькуляторах, приведенных выше.
Данным калькулятором рекомендуется пользоваться только в случае отсутствия данных о низшей теплотворной способности и числе Воббе от газораспределительной организации. Как правило значение теплотворной способности и числе Воббе можно получить из паспорта качества природного газа, получаемого (оформляемого) газораспределительной организацией.
Примеры паспортов качества газа:
-
- ООО «Газпром трансгаз Нижний Новгород», ООО «Газпром трансгаз Ухта», ООО «Газпром трансгаз Москва» (Московское ЛПУМГ), ООО «Газпром трансгаз Москва» (Гавриловское ЛПУМГ);
- Газпром Межрегионгаз Омск.
Низшая теплотворную способность используется:
-
- для расчета расходов газа на оборудование (котлы, технологическое оборудование);
- при выполнении теплотехнического расчета газоиспользующего оборудования.
Число Воббе газообразного топлива (низшее или высшее) — это отношение объемной (соответственно, низшей или высшей) теплоты сгорания к корню квадратному из относительной плотности газообразного топлива.
Это число характеризует постоянство теплового потока, получаемого при сжигании газа. Газы c одинаковым числом Воббе при равном давлении истечения обычно могут использоваться один вместо другого без замены горелки или форсунки.
Примечание: При этом число Воббе не охватывает таких характеристик, как возможность отрыва или проскока пламени. Требуется дополнительная проверка на устойчивость пламени газогорелочного устройства.
При подводе газов с разными числами Воббе к одной горелке газ с меньшим числом Воббе должен подводиться при большем давлении. Давление газа при новом значении числа Воббе определяется по формуле:
P2=(ρ2/ρ1)*P1*(QH1/QH2)2
где P2 — избыточное давление газа на новом газе с плотность ρ2 и низшей теплотворной способность природного газа QH2;
P1 — избыточное давление газа на первоначального газа с плотность ρ1 и низшей теплотворной способность природного газа QH1.
При невозможности изменения давления газа требуется изменение конструкции горелки (например изменение диаметра сопла горелки). Методы расчета изменений конструктивных размеров элементов горелки зависит от типа горелки (например: инжекционные горелки низкого давления, инжекционные горелки среднего давления, горелки с принудительной подачей воздуха и т.д. ).
Примечание.
В комментарии приветствуются пожелания, замечания и рекомендации по улучшению программы.
Поделиться ссылкой:
Дата актуализации статьи: 06.04.2022 16:21:00
06.04.2022
Фото:
Ранее мы уже рассказывали нашим читателям о составе природного газа, теперь пришло время поговорить о его основных теплотехнических характеристиках. Эти знания нам также будут весьма полезны для дальнейшего понимания взрывопожароопасности природного газа и о способах ее снижения.
Свойства природного газа зависят от его компонентного состава, который различается от месторождения к месторождению. По этой причине существует широкий разброс основных параметров газообразного топлива, добываемого в разных залежах.
Теплота сгорания природного газа
Основной теплотехнической характеристикой, интересующей потребителя топлива, является теплота сгорания. Это количество теплоты, выделяющееся при сжигании 1 кг твердого топлива или 1 м3
горючего газа. Для газообразного топлива измеряется в мегаджоулях на кубический метр (МДж/м3). На практике часто применяется другая единица измерения — килокалория на кубический метр (ккал/м3). Возможно определение теплоты сгорания горючих газов в мегаджоулях на килограмм (МДж/кг), что необходимо для сопоставления различных видов топлива: твердого, жидкого и газообразного.
Рис. 1. Низшая и высшая теплота сгорания природного газа
Источник: https://eco-kotly.ru/wp-content/uploads/b/2/6/b265ef32d6a26b09c862ddaceaf637f5.jpeg.
Высшая и низшая теплота сгорания природного газа
При сжигании всех видов топлива, в составе компонентов которого содержится водород, в продуктах сгорания образуются пары воды. Если эти пары уйдут в атмосферу, они унесут часть тепла. Если вода сконденсируется в оборудовании, она отдаст это тепло.
Низшая теплота сгорания QН
не учитывает теплоту конденсации водяных паров из продуктов сгорания. В качестве примера рассмотрим использование тепла в водонагревательном оборудовании (рис. 1 а). Коэффициент полезного действия современных не конденсационных газовых котлов, определенный по низшей теплоте сгорания, составляет около 91 %. Из выделившейся при горении газового топлива 100%-й теплоты 91 % переходит в полезное тепло, то есть поступает потребителю в виде нагретой воды. Потери тепла из-за излучения наружных поверхностей котла составляют 3 %, потери с дымовыми газами — 6 %. Химического недожога современные газогорелочные устройства не допускают. Если из 100 % тепла, полученных при сгорании газа, вычесть потери (3 + 6 = 9 %), то получается КПД, равный 91 %.
Высшая теплота сгорания QВ
учитывает всю теплоту, выделяющуюся при сгорании топлива. У конденсационных котлов коэффициент полезного действия, если его определять по низшей теплоте сгорания, может достигать 107 %. Для человека, не прогуливавшего в школе физику, такое невозможно. Вечного двигателя не существует.
Но здесь надо разобраться в расчетах. Получение тепла при сгорании и конденсации паров воды в продуктах сгорания составляет 111 %, опять же по низшей теплоте сгорания. Это 100 %, полученных при горении, и 11 %, полученных при конденсации (рис.1 б). Потери на излучение в окружающую среду — 1 %, потери с дымовыми газами — 3 %. Уменьшение потерь на излучение достигается за счет лучшей тепловой изоляции котла. Уменьшение потерь с отходящими дымовыми газами — результат более низкой их температуры. Если из 111 % вычесть потери (1 + 3 = 4 %), то получается КПД, равный 107 %. КПД конденсационных котлов, рассчитанный по высшей теплоте сгорания, превышает 98 %.
Исторически сложилось так, что в России для практических расчетов используется низшая теплота сгорания. В некоторых странах (США, Великобритания) теплотехнические расчеты выполняют с учетом высшей теплоты сгорания.
Теплота сгорания углеводородных компонентов природного газа приведена в таблице 1.
Таблица 1
|
Компонент |
Теплота сгорания, МДж/м3 |
|
|
Высшая |
Низшая |
|
|
Метан |
39,82 |
35,88 |
|
Этан |
70,31 |
64,36 |
|
Пропан |
101,21 |
93,18 |
|
н-Бутан |
133,80 |
123,57 |
|
u-Бутан |
132,96 |
122,78 |
Необходимо отметить, что наличие негорючих компонентов уменьшает теплотворную способность газового топлива. Например, в уренгойском газе содержится более 1 % азота и иных примесей, поэтому его низшая теплота сгорания — 34,95 МДж/м3. Особенно велико содержание негорючих компонентов в попутных нефтяных газах, где оно может составлять более четверти от общего объема. В соответствии с ГОСТ 5542-2014 «Газы горючие природные промышленного и коммунально-бытового назначения. Технические условия» низшая теплота сгорания природного газа при стандартных условиях должна быть не менее 31,8 МДж/м3.

Немного про конденсационные котлы
Создание энергосберегающих аппаратов является приоритетным направлением развития техники. Конденсационные котлы имеют более сложный теплообменник, позволяющий отобрать у продуктов сгорания больше тепла (рис. 2). В нем больше поверхностей теплообмена, расположенных в камере, где дымовые газы остывают до температуры точки росы. В конденсационных котлах используются горелки с принудительной подачей воздуха. Такие особенности приводят к усложнению конструкции и удорожанию аппарата.
Несмотря на высокий КПД, конденсационные котлы в России не находят широкого применения. Тому есть несколько причин. Во-первых, высокая стоимость, в разы превышающая цену обычных аппаратов. Конечно, увеличение коэффициента полезного действия позволяет экономить газ. Но стоимость газа в нашей стране невелика. Полученная экономия не позволяет в обозримом времени окупить приобретение газового аппарата. Вторая причина — относительно низкая температура теплоносителя на выходе котла, около 60 °С. При использовании конденсационных котлов требуются специальные отопительные системы. Приходится увеличивать количество отопительных приборов (радиаторов) либо применять более дорогие радиаторы с увеличенной площадью поверхности. Другое решение — система отопления типа «теплый пол».
Рис. 2. Принцип работы конденсационного котла
Источник: https://prostroymaterialy.com/wp-content/uploads/2021/06/img_16226812587093-1.jpg.
Кроме того, при работе конденсационного котла образуется конденсат, который необходимо утилизировать. В котлах малой и средней мощности в час образуется 4–7 л конденсата с растворенными продуктами сгорания. Эта жидкость является опасным отходом: в канализацию ее можно сливать в случае, если она соотносится с общим объемом канализационного стока в отношении 1 к 25.
Число Воббе природного газа
Взаимозаменяемость горючих газов характеризуется числом Воббе — это отношение объемной теплоты сгорания газообразного топлива к корню квадратному из его относительной плотности. В свою очередь, относительная плотность — отношение плотности газа к плотности воздуха при стандартных условиях. Физический смысл этого показателя: при одинаковом давлении газы с одинаковым числом Воббе дадут равное количество теплоты. Число Воббе одновременно учитывает изменение состава газа и перепад давления на горелочном устройстве. Это позволяет использовать одни и те же горелки при переходе с одного газа на другой, не изменяя давление газа.
Измеряется число Воббе так же, как и теплота сгорания — в мегаджоулях на кубический метр (МДж/м3). В соответствии с ГОСТ 5542-2014 область значений числа Воббе для природного газа при стандартных условиях — от 41,20 до 54,50 МДж/м3.
Температура самовоспламенения природного газа
Подготовительным этапом горения газового топлива является воспламенение, когда идет медленное окисление без видимого пламени. В результате накопления теплоты происходит воспламенение других объемов газовоздушной смеси. В свою очередь, дальнейшее повышение температуры приводит к ускорению реакции и интенсивному горению. При самовоспламенении газовоздушная смесь равномерно нагревается до такой температуры, при которой весь объем самостоятельно, без введения источника теплоты, воспламеняется. Иной характер реакции происходит при зажигании: холодная смесь воспламеняется в одной точке источником с высокой температурой (нагретое тело, искра, пламя), затем горение распространяется по всему объему.
Температура самовоспламенения — это температура топливовоздушной смеси, при которой смесь начинает гореть без источника воспламенения. Для метана она составляет 537 °С. Именно такую цифру дает ГОСТ 5542-2014. Температура самовоспламенения зависит от состава природного газа. С увеличением доли более тяжелых углеводородов (этана, пропана, бутана) она понижается.
Жаропроизводительность
Жаропроизводительность — это максимальная температура, которая может быть достигнута при полном сгорании газа, если количество воздуха, необходимого для горения, точно отвечает формуле горения, а начальная температура воздуха и газа равны нулю. Для метана она составляет 2043 °С. Интересно, что наибольшей жаропроизводительностью среди горючих газов обладает ацетилен — 2620 °С.
В разделе:
Читай также
В данной статье мы расскажем о взрывопожароопасности природного газа и его удушающем действии.
Стабилизация пламени в газовых горелках очень важна, поскольку ее нарушение может привести к пожару. В данной статье мы рассказываем, какими способами достигается стабилизация пламени, а также как предотвратить ее отрыв и проскок.
По запасам природного газа в традиционных месторождениях Российская Федерация занимает первое место в мире — около 50 трлн м3. В топливно-энергетическом балансе нашей страны он занимает ведущее место, обеспечивая более 55 % от общей потребности в энергоресурсах. В данной статье подробно расскажем о том, где именно находятся указанные месторождения.
S-2098 (А018)

Правообладатель: Портал про пожарную безопасность propb.ru.
1.1. Элементарный состав твердого, газообразного и жидкого топлива
В базовой и промышленной энергетике для получения электрической и тепловой энергии используется в основном топливо органического происхождения.
Все виды органического топлива (горючие) представляют собой углеводородные соединения, в которые входят небольшие количества других веществ.
К твердому топливу относят: антрацит, каменный и бурый уголь, торф, дрова, сланцы, отходы лесопильных заводов и деревообделочных цехов, а также растительные отходы сельскохозяйственного производства — солому, костру, лузгу и др.
К жидкому топливу относят нефть, а также различные продукты ее переработки: бензин, керосин, лигроин, разнообразные масла и остаточный продукт нефтепереработки нефти — мазут.
До 70 % и более видов жидкого топлива используется на транспорте — авиационном, автомобильном, специальном водном, железнодорожном (тепловозы), около 30 % сжигается в виде мазута на тепловых электростанциях и в промышленных котельных.
К газообразному топливу относят природный газ, добываемый из недр земли, попутный нефтяной газ, газообразные отходы металлургического производства (коксовый и доменный газ), крекинговый газ, а также генераторный газ, получаемый искусственным путем из твердого топлива в особых газогенераторных установках.
Топливо в том виде, в каком оно поступает для сжигания в топки котлов или в двигатели внутреннего сгорания, называется рабочим.
В общем случае в состав рабочего (твердого или жидкого) топлива входят углерод С, водород Н, кислород О, азот N и летучая сера S, а также негорючие минеральные примеси — зола А и влага W.
Для рабочей массы топлива имеет место равенство:
Cp+ Hp+ Op+ Np+ Sp+ Ap+ Wp= 100 %, (1.1)
где СР, НР, ОР и т. д. — элементы рабочего топлива, % общей массы топлива.
Влага, содержащаяся в топливе совместно с золой, называется балластом топлива.
В естественных видах ископаемого твердого топлива встречается сера трех разновидностей:
1) органическая Sо, связанная с другими элементами топлива С, Н, N и О в виде сложных органических соединений;
2) колчеданная Sк в виде пирита, колчедана FeS2;
3) сульфатная Sсульф в виде солей серной кислоты (гипс, FeSО4и др.). Сульфаты представляют собой высокие окислы серы, поэтому находящаяся в них сера гореть не может. Присутствующие в топливе органическая и колчеданная серы сгорают, образуя токсичный сернистый ангидрид SO2и (в небольших количествах) еще более токсичный серный ангидрид SO3. Выброс их с продуктами сгорания вызывает загрязнение воздушного бассейна.
Органическая и колчеданная сера образуют вместе летучую горючую серу Sл. Общее содержание серы в топливе
Sобщ = Sо + Sк + Sсульф = Sл + Sсульф. (1.2)
В горючую часть топлива входит только летучая сера, остальная сера в горении участия не принимает и может быть отнесена к балласту топлива.
Для правильного представления тепловых свойств топлива вводится понятие горючей массы, для которой
Сг+ Нг+ Ог+ Nг+ Sгл= 100 %, (1.3)
где индекс вверху показывает, что процентный состав отдельных элементов отнесен к горючей массе.
Название «горючая масса» носит условный характер, так как действительно горючими ее элементами являются только углерод, водород и сера. Углерод — преобладающий компонент твердых и жидких топлив, в топливах его обычно содержится от 50 до 95 %, тогда как содержание водорода Нг колеблется в пределах от 1 до 11 %, а серы Sг — от 0 до 8 %. Горючую массу можно характеризовать как топливо, не содержащее золы и в абсолютно сухом состоянии. Содержание азота в горючей массе твердых топлив обычно составляет 1—2 % по массе. Несмотря на столь малое количество, азот является весьма вредным компонентом, поскольку при сгорании азотсодержащих соединений в высокотемпературных топках образуются сильнотоксичные оксиды NО и NO2(они образуются также и из атмосферного азота, но в
меньшей степени).
Для топлива, содержащего большое количество влаги (бурый уголь, торф, дрова, некоторые растительные отходы), в некоторых случаях удобно использовать понятие сухой массы, т. е. характеризовать состав абсолютно сухого топлива суммой элементов Сс, Нс, Ос, Nс, Sс и Ас. При этом
Сс + Нс + Ос + Nс + Sс + Ас = 100 %, (1.4)
где индекс показывает, что процентный состав отдельных элементов отнесен к сухой массе.
Для взаимного пересчета массы топлива в соответствии с понятием о массах топлива служат формулы, объединенные в табл. 1.1.
Таблица 1.1. Формулы для пересчета состава топлива с одной массы на другую
|
Заданная масса топлива |
Искомая масса топлива, % |
||
|
рабочая |
сухая |
горючая |
|
|
Рабочая |
1 |
|
|
|
Сухая |
|
1 |
|
|
Горючая |
|
|
1 |
Зольность топлива. Золой называют твердый негорючий остаток, остающийся после сжигания топлива в атмосфере воздуха. Зола может быть в виде сыпучей массы с плотностью в среднем 600 кг/м3 и в виде сплавленных пластин и кусков, называемых шлаками, с плотностью до 800 кг/м3.
В состав золы большинства видов твердого топлива входят: глинозем Al2O3, кремниевая кислота SiO2, известь СаО, магнезия MgO, щелочи Na2O, окислы железа FeO и Fe2О3.
Влажность твердого топлива. Влажность твердого топлива Wрдоходит
до 50 % и более и определяет экономическую целесообразность использования данного горючего материала и возможность его сжигания. Влага снижает температуру в топке и увеличивает объем дымовых газов. Увеличенный объем дымовых газов требует дополнительной энергии на их удаление.
Очевидно, что влага является балластной примесью, так как уменьшает тепловую ценность исходного топлива. Кроме того, часть теплоты, выделяемой топливом при его сгорании, расходуется на испарение влаги.
Летучие вещества. При нагревании твердого топлива без доступа воздуха его органическая масса разлагается, в результате чего образуются газы, водяные и смоляные пары и углесодержащий остаток. Суммарное количество выделяющихся летучих веществ увеличивается с увеличением температуры и времени выдержки, этот процесс в основном заканчивается при 700—800 оС. Выход летучих веществ Vг, в процентах на горючую массу, является важнейшей характеристикой горючей массы твердого топлива и уменьшается по мере увеличения его возраста. Чем больше выход летучих веществ, т.е. чем больше топлива превращается при нагревании в горючий газ, тем проще зажечь это топливо и легче поддерживать устойчивое горение. Органическая часть древесины и горючих сланцев при нагревании без доступа воздуха почти целиком переходит в летучие вещества
(Vг= 85÷90%), в то время как у антрацитов Vг= 3÷4 %. Именно большой выход летучих веществ определяет хорошую горючесть древесины.
Состав некоторых видов твердого топлива представлен в табл. 1.2.
Таблица 1.2. Примерный состав и теплотехнические характеристики горючей массы основных видов твердого топлива
|
Топливо |
Состав горючей массы, % |
Выход летучих веществ, Vг, % |
Низшая теплота сгорания, МДж/кг |
||||
|
Сг |
Sг |
Нг |
Oг |
Nг |
|||
|
Дрова |
51 |
— |
6,1 |
42,2 |
0,6 |
85 |
19 |
|
Торф |
58 |
0,3 |
6 |
33,6 |
2,5 |
70 |
8,12 |
|
Горючий сланец |
60—75 |
4—13 |
7—10 |
12—17 |
0,3—1,2 |
80—90 |
7,66 |
|
Бурый уголь |
64—78 |
0,3—6 |
3,8—6,3 |
15,26 |
0,6—1,6 |
40—60 |
27 |
|
Каменный уголь |
75—90 |
0,5—6 |
4—6 |
2—13 |
1—2,7 |
9—50 |
33 |
|
Полуантрацит |
90—94 |
0,5—3 |
3—4 |
2—5 |
1 |
6—9 |
34 |
|
Антрацит |
93—94 |
2—3 |
2 |
1—2 |
1 |
3—4 |
33 |
Жидкое топливо. Практически все виды жидкого топлива получают путем переработки нефти (бензин, керосин, дизельное топливо и мазут). Мазут представляет собой сложную смесь жидких углеводородов, в состав которых входят в основном углерод (Ср= 84÷86 %) и водород (Нр= 10÷12 %); Ор + Nр= 1÷2 %, содержание воды и зольность не превышают 0,2—1,5%.
Мазуты, полученные из нефти ряда месторождений, могут содержать много серы (до 4,5—5%), что резко усложняет защиту окружающей среды при их сжигании.
Характеристики основных видов жидкого топлива приведены в табл. 1.3. Из указанных выше видов жидкого топлива в промышленных и котельных печах сжигаются только топочные мазуты, которые классифицируются по степени их вязкости: М20, М40, М60, М80, М100 и М120 (цифры в указанных марках мазута означают условную вязкость в градусах Энглера).
Для транспортных установок применяют так называемый мазут флотский марок Ф5 и Ф12.
В табл. 1.4 приведены характеристики топочных и флотских мазутов.
Газообразное топливо. Газообразное топливо по сравнению с другими видами топлива имеет ряд существенных преимуществ: сгорает при небольшом избытке воздуха, образуя продукты полного горения без дыма и копоти; не дает твердых остатков; удобно для транспортировки по газопроводам на большие расстояния и позволяет простейшими средствами осуществлять сжигание в установках самых различных конструкций и мощностей. Газообразное топливо делится на естественное и искусственное. Естественное топливо в свою очередь делится на природное и нефтепромысловое.
Таблица 1.3. Характеристики некоторых видов жидкого топлива, получаемого из нефти
|
Топливо |
Состав горючей массы, % |
Зольность сухого топлива Ас, % |
Влага рабочего топлива Wр, % |
Низшая теплота сгорания рабочего топлива, МДж/кг |
|||
|
углерод Сг |
водород Нг |
сера Sг |
кислород и азот Oг + Nг |
||||
|
Бензин |
85 |
14,9 |
0,05 |
0,05 |
0 |
0 |
43,8 |
|
Керосин |
86 |
13,7 |
0,2 |
0,1 |
0 |
0 |
43 |
|
Дизельное |
86,3 |
13,3 |
0,3 |
0,1 |
Следы |
Следы |
42,4 |
|
Солярное |
86,5 |
12,8 |
0,3 |
0,4 |
0,02 |
Следы |
42 |
|
Моторное |
86,5 |
12,6 |
0,4 |
0,5 |
0,05 |
1,5 |
41,5 |
|
Мазут: |
|||||||
|
малосернистый |
86,5 |
12,5 |
0,5 |
0,5 |
0,1 |
1 |
41,3 |
|
сернистый |
85 |
11,8 |
2,5 |
0,7 |
0,15 |
1 |
40,2 |
|
многосернистый |
84 |
11,5 |
3,5 |
0,5 |
0,1 |
1 |
40 |
Таблица 1.4. Основные характеристики котельных мазутов
|
Показатель |
Нормы по маркам мазута |
||||
|
флотского |
топочного |
||||
|
Ф5 |
Ф12 |
40 |
100 |
200 |
|
|
Вязкость (условная), оВУ, не более: |
|||||
|
при 50 °С |
5 |
12 |
— |
— |
— |
|
при 80 °С |
— |
— |
8 |
15,5 |
|
|
при 100 °С |
— |
— |
— |
— |
6,5—9,5 |
|
Температура застывания °С, не выше |
|||||
|
мазута |
–5 |
–8 |
+10 |
+25 |
+ 36 |
|
мазута из высокопарафиновых нефтей |
— |
— |
+25 |
+42 |
+42 |
|
Температура вспышки, °С, не ниже, при |
|||||
|
определении в тигле: |
|||||
|
закрытом |
80 |
90 |
— |
— |
— |
|
открытом |
— |
— |
90 |
110 |
140 |
Природный газ получают из чисто газовых месторождений, где он выбрасывается из недр земли под давлением, доходящим иногда до 100 атм и более. Основным его компонентом является метан СН4, кроме того, в газе разных месторождений содержатся небольшие количества водорода Н2, азота N2, высших углеводородов СnНm, оксида (СО) и диоксида (СO2) углерода. В табл. 1.5 представлены характеристики горючих газов, входящих в состав газообразного топлива.
Таблица 1.5. Характеристика горючих газов, входящих в состав газообразного топлива
|
Газ |
Химическая формула |
Низшая теплота сгорания 1 м3 газа Qнс |
Плотность газа r, кг/м3, при нормальных условиях |
Удельный объем, м3/кг |
Теоретическая температура горения, °С |
|
|
МДж/м3 |
ккал/м3 |
|||||
|
Водород |
Н2 |
10,8 |
2 580 |
0,09 |
11,112 |
— |
|
Метан |
СН4 |
35,82 |
8 555 |
0,717 |
1,4 |
1 980 |
|
Этан |
С2Н6 |
63,75 |
15 226 |
1,342 |
0,746 |
2 150 |
|
Пропан |
С3Н8 |
91,25 |
21 795 |
1,967 |
1,51 |
— |
|
Бутан |
С4Н10 |
118,65 |
28 338 |
2,593 |
0,385 |
2 080 |
|
Пентан |
C5H12 |
146,08 |
34 890 |
3,218 |
0,321 |
2 090 |
|
Этилен |
С2Н4 |
59,06 |
14 107 |
1,261 |
— |
2 200 |
|
Пропилен |
С3Н6 |
86,00 |
20 541 |
1,915 |
— |
2 270 |
|
Бутилен |
C4H8 |
113,51 |
27 111 |
2,372 |
— |
2 100 |
|
Оксид углерода |
СО |
12,64 |
3 018 |
1,25 |
0,8 |
— |
|
Сероводород |
H2S |
23,38 |
5 585 |
1,5392 |
0,650 |
1900 |
При добыче нефти выделяется так называемый попутный газ, содержащий меньше метана, чем природный, но больше высших углеводородов и поэтому выделяющий при сгорании больше теплоты. Проблема полного его использования сейчас весьма актуальна.
К искусственным газам относят доменный газ, являющийся продуктом при выплавке чугуна на металлургических заводах; коксовый, образующийся при получении кокса в коксовых батареях; светильный, получаемый при сухой перегонке угля; генераторный, получаемый в газогенераторах.
Коксовый и доменный газ используют главным образом на месте в доменном и других цехах металлургического завода.
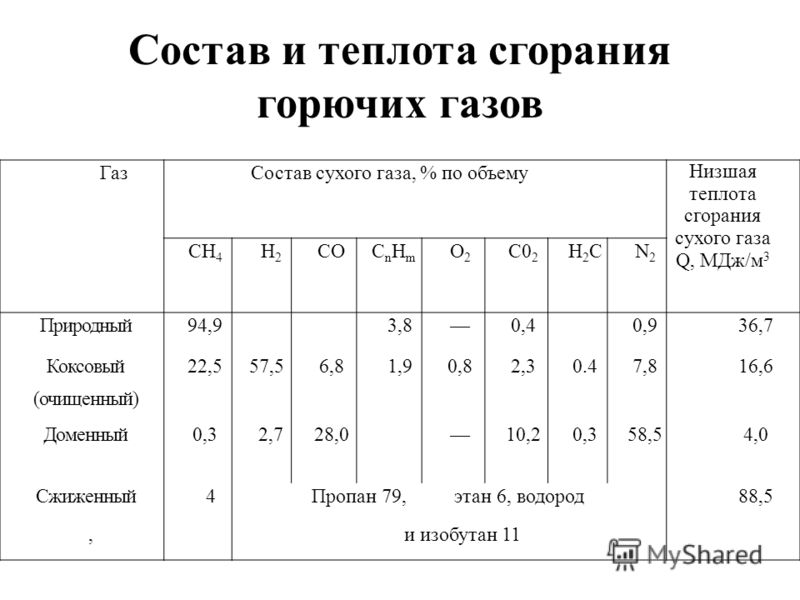
В табл. 1.6 представлены состав и теплота сгорания некоторых видов газообразного топлива.
Теплота сгорания топлива. Основной характеристикой топлива является так называемая теплота сгорания. Теплотой сгорания твердого и жидкого топлива называется количество тепла, кДж, выделяемое 1 кг топлива при полном его сгорании. Теплоту сгорания обозначают буквой Q и измеряют в килоджоулях на килограмм (кДж/кг) [в системе МКГСС в килокаллориях на килограмм (ккал/кг)].
Теплоту сгорания газообразного топлива относят обычно к 1 м3, взятому при нормальных условиях (0 °С, 760 мм рт.ст.), и измеряют в килоджоулях на метр кубический (кДж/м3).
Таблица 1.6. Состав и теплота сгорания основных горючих газов
|
Газы |
Состав сухого газа, % по объему |
Низшая теплота сгорания газа Qнс , МДж/м3 |
|||||||
|
СН4 |
Н2 |
СО |
СmHn |
O2 |
СО2 |
S |
N2 |
||
|
Природный Коксовый (очищенный) Доменный Сжиженный (ориентировочно) |
94,9 22,5 0,3 4 |
— 57,5 2,7 |
— 6,8 28 |
3,8 1,9 — |
— 0,8 — |
0,4 2,3 10,2 |
— 0,4 0,3 |
0,9 7,8 58,5 |
36,7 16,6 4,0 88,5 |
|
Пропан 79, этан 6, Н — изобутан 11 |
Теплота сгорания зависит от химического состава топлива и условий его сжигания.
В соответствии с понятием органической, горючей и других масс топлива она может быть отнесена к той или другой из этих масс. Наибольший практический интерес представляет теплота сгорания рабочей массы топлива Qнр.
Низшей теплотой сгорания Qнр рабочего топлива называют тепло, выделяемое при полном сгорании 1 кг топлива, за вычетом тепла, затраченного на испарение как влаги, содержащейся в топливе, так и влаги, образующейся от сгорания водорода.
Теплоту сгорания топлива определяют по формулам, учитывающим, что углерод С, водород Н и сера S, участвующие в горении, выделяют определенное количество тепла.
Для определения Qнр используют формулу Д.И. Менделеева, которая дает достаточно точные результаты для самых разнообразных видов топлива.
Формула для определения Qнр, кДж/кг, твердого и жидкого топлива имеет вид
Qнр = 338 Ср+ 1025 Нр– 108,5 (Ор– Sр)– 25 Wр, (1.5)
где коэффициенты выражают теплоту сгорания отдельных горючих элементов, деленную на 100.
Низшую теплоту сгорания сухого газообразного топлива определяют как сумму произведений теплот сгорания горючих газов на их объемное содержание в смеси, кДж/м3:
Qнр = 127 СО + 10 Н2 + 358 СН4 + 591С2Н6 + 911 С3Н8 + 234 Н2S. (1.6)
Условное топливо. Большая разница в теплоте сгорания различных видов топлива затрудняет в некоторых случаях проведение сравнительных расчетов, например, при выявлении запасов топлива, при оценке целесообразности применения разных сортов топлива и пр. Поэтому принято понятие условного топлива. Условным называется такое топливо, теплота сгорания 1 кг или 1 м3 которого равна 29330 кДж (Qусл).
Для перевода действительного топлива в условное пользуются соотношением (безразмерным коэффициентом):
Эк= Qнр /29330 (в системе МКГСС —Эк= Qнр/7000), (1.7)
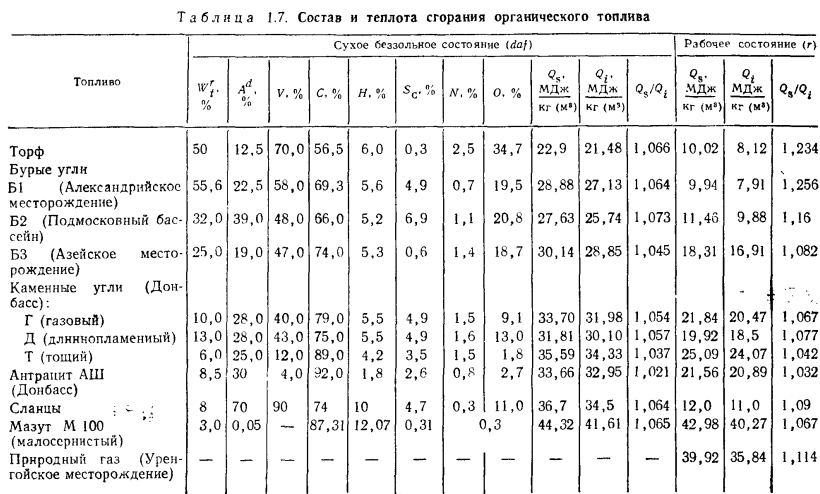
где Эк — калорийный эквивалент, указывающий какая часть теплоты сгорания условного топлива соответствует низшей теплоте сгорания рассматриваемого топлива (табл. 1.7).
Таблица 1.7. Калорийные эквиваленты различных видов топлива
|
Вид топлива |
Низшая теплота сгорания Qнр, кДж/кг |
Калорийный эквивалент Эк=Qнр/Qусл |
|
Твердое топливо |
||
|
Дрова смешанные |
12 580 |
0,43 |
|
Торф фрезерный |
8460 |
0,29 |
|
Бурый уголь (Подмосковный бассейн) |
10760 |
0,37 |
|
Бурый уголь (Назаровское месторождение) |
13020 |
0,44 |
|
Антрацит АШ (Донецкий бассейн) |
24240 |
0,83 |
|
Сланцы эстонские |
10340 |
0,35 |
|
Жидкое топливо |
||
|
Нефть сырая |
43000 |
1,47 |
|
Мазут М-100 (многосернистый) |
40030 |
1,37 |
|
Мазут М-100 (малосернистый) |
40820 |
1,39 |
|
Газообразное топливо * |
||
|
Природный газ |
34860 |
1,65 |
|
Доменный газ |
3770 |
0,1 |
|
Коксовый газ |
18000 |
1,21 |
|
Генераторный водяной |
10030 |
0,3 |
|
Сжиженный газ (технический пропан) |
93750 |
3,2 |
* Теплота сгорания газообразного топлива, кДж/м3, при нормальных условиях.
Расход условного топлива
Вусл= B Qнр /Qусл , (1.8)
где В — расход рассматриваемого топлива; Qнр — теплота сгорания топлива.
1.2. Расчеты горения топлива
При тепловом расчете топливосжигающих установок (паровых и водогрейных котлов, промышленных огневых печей, двигателей внутреннего
сгорания), а также при обработке результатов их испытаний определяют следующие характеристики и величины:
• теоретический и действительный расходы воздуха V0 и Vд, необходимые для сгорания 1 кг твердого и жидкого топлива или 1 м3 газообразного топлива;
• состав и объем продуктов сгорания Vг (дымовых газов);
• энтальпию дымовых газов при требующихся температурах и коэффициентах избытка воздуха Тг.
Для полного сгорания топлива требуется некоторый избыток воздуха против теоретического расхода. Избыток воздуха характеризуется так называемым коэффициентом избытка aт (иногда называемым коэффициентом расхода воздуха). Он зависит от способа сжигания топлива, качества смесеобразования топлива с воздухом и ряда других факторов.
Коэффициент избытка воздуха представляет собой отношение действительного расхода воздуха к теоретическому, т. е.
aт= Vд/V0. (1.9)
При полном сгорании дымовые газы (продукты сгорания) состоят из СО2 и SО2, получившихся при сгорании углерода и летучей серы, водяного пара, образующегося при испарении влаги топлива и сгорании его водорода, азота, подводимого в топку (камеру сгорания) с воздухом, и, наконец, кислорода, не использованного при горении.
Объем продуктов сгорания определяется по формуле
Vг= VCO2 + VSO2+ VH2O+ VN2+ VO2. (1.10)
При проведении химического анализа дымовых газов содержание СО2 и SO2 определяется совместно, поэтому в расчетные формулы вводится сумма количества СО2 и SO2, обозначаемая символом RO2, тогда
Vг= VRO2+ VN2+ VO2+ VH2O= Vс. г+ VH2O. (1.11)
где Vс. г — объем сухих дымовых газов:
Vс. г= VRO2+ VN2+ VO2. (1.12)
В табл. 1.8 приведены расчетные формулы для определения объемов воздуха и продуктов полного сгорания для твердых, жидких и газообразных видов топлива. В этих формулах Ср, Нр, …; СО, Н2, СН4, … — содержание соответствующих элементов и компонентов в рабочем топливе, %; aт— коэффициент избытка воздуха; dв— влагосодержание сухого воздуха, г/м3 (обычно принимается 10 г/м3).
В случае отсутствия элементарного состава сжигаемого топлива при известном значении Qнр и Wр можно пользоваться эмпирическими формулами
табл. 1.9.
Основой тепловых расчетов топливоиспользующих устройств является энтальпия продуктов сгорания, которую принято рассчитывать на единицу количества топлива, из которого получились эти продукты.
Таблица 1.8. Расчетные формулы для определения объемов воздуха и продуктов полного сгорания при нормальных условиях
|
Определяемые величины |
Для твердого и жидкого топлива, м3/кг |
Для газообразного топлива, м3/м3 |
|
Теоретически необходимое количество воздуха |
V0=[0,0889(Ср+ 0,375Sр)+ 0,2665HP – 0,033Ор]*(1 + 0,00124dв) |
V0= 0,0476[0,5СО+ 0,5Н2+1,5H2S + 2CH4+ ∑(m + n/4)CmHn— O2](1 + 0,00124dв) |
|
Действительное количество воздуха |
Vд= aтV0 |
|
|
Количество продуктов полного сгорания |
VCO2= 0,0187 + Cp; VH2O= 0,112Hp+ 0,00124WP+ 0,0124Vдdв; VSO2= 0,07 Sp ; VO2= 0,21(aт— 1)V0; VN2= 0,008Np + 0,79Vд |
VCO2=(СО + CО2+ СН4+ ∑mCmHn)0,01; VH2O=(H2+ H2S + 2CH4+ CmHn+ 0,124Vдdв)0,01; VSO2= 0,01 H2S; VO2= 0,21 (aт+ l) VO; VN2=(N2+ 79Vд)0,01 |
|
Состав продуктов сгорания, % |
Vг= VCO2+ VH2O+ VSO2+ VO2+ VN2 СО2=(VCO2/ Vг)100 и т.д. |
Таблица 1.9. Эмпирические формулы для определения V0и Vг, м3/кг или м3/м3 при нормальных условиях
|
Топливо |
Теоретически необходимое количество воздуха |
Действительное количество продуктов сгорания |
|
Дрова Уголь Жидкое топливо Газообразное топливо с Qнр< 12 МДж/м3 То же с Qнр> 12 МДж/м3 Коксодоменная печь |
V0= 4,66 (1 – Wp/1000) V0 = 0,24 Qнр+ 0,5 V0= 0,2 Qнр+ 2 V0= 0,21 Qнр V0 = 0,26 Qнр— 0,25 V0 = 0,24 Qнр— 0,2 |
Vг= 5,3 — 4,055Wp/1000 +(a — 1)V0 Vг= 0,21Qнр+ 1,65 +(a — 1)V0 Vг= 0,265 Qнр+(-1)V0 Vг= 0,17 Qнр+ 1 +(a — 1)V0 Vг= 0,27 Qнр+ 0,25 +(- 1)V0 Vг= 0,225 ×+ 0,765 + (a — 1)V0 |
Примечание: Qнр — в МДж/кг или МДж/м3 при нормальных условиях (1 ккал = 4,187 кДж).
Энтальпия продуктов сгорания вычисляется как произведение их объема при нормальных условиях на объемную теплоемкость при постоянном давлении и на температуру, кДж/кг или кДж/м3:
Iг = Vгсгt, (1.13)
где t — температура, оС; Vг —полный объем продуктов сгорания, м3/кг или м3/м3, на единицу топлива; сг — средняя в диапазоне температур 0 — t оС теплоемкость продуктов сгорания, кДж/(кг× оС) или кДж/(м3× оС).
Расчет энтальпии продуктов сгорания, кДж/кг или кДж/м3, производится по формуле
Iг= VCO2(cϑ)CO2+ VSO2(cϑ)SO2+VH2O(cϑ)H2O+VN2(cϑ)N2+VO2, (1.14)
где VCO2, VSO2, VH2O, VN2, VO2— объемы продуктов полного сгорания, определяемые по табл. 1.8; (cϑ)CO2, (cϑ)SO2, (cϑ)H2O,(cϑ) — энтальпии газов, определяемые по температуре (табл. 1.10).
Таблица 1.10. Энтальпия газов и воздуха при различных температурах и постоянном давлении 101 кН/м2 (760 мм рт. ст.), кДж/м3
|
Температура,°С |
(cϑ)CO2 |
(cϑ)H2O |
Сухой воздух |
(cϑ)N2 |
(cϑ)O2 |
(cϑ)H2 |
(cϑ)CO |
(cϑ)SO2 |
|
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
100 |
171 |
150 |
130 |
130 |
132,3 |
129,2 |
130,2 |
182 |
|
200 |
360,6 |
302,4 |
261,9 |
261,6 |
267,2 |
259,6 |
261,5 |
379,4 |
|
300 |
563,9 |
418,7 |
395,7 |
394,6 |
409,4 |
390,6 |
395,7 |
589,5 |
|
400 |
777,1 |
623,4 |
533 |
530,1 |
551,4 |
521,7 |
532,2 |
810,2 |
|
500 |
1001,1 |
600,2 |
672,4 |
667,8 |
699,6 |
654 |
671 |
1037,9 |
|
600 |
1236,4 |
964,3 |
814,7 |
389,4 |
850,8 |
785,9 |
802,2 |
1272,4 |
|
700 |
1475,1 |
1143 |
959 |
950,9 |
1004,5 |
919,5 |
960,7 |
1510,7 |
|
800 |
1718,8 |
1328,9 |
1106,9 |
1098,7 |
1160,5 |
1086,9 |
1110,3 |
1751,8 |
|
900 |
1967,5 |
1526,8 |
1259,4 |
1247,7 |
1320,2 |
1245,3 |
1261,1 |
1997,6 |
|
1000 |
2219,5 |
1721 |
1412,3 |
1399,3 |
1479,7 |
1330,2 |
1414,4 |
2243,8 |
Энтальпию Iгопределяют для нескольких значений ϑ и a. На основании этих подсчетов строят кривые зависимости Iгот ϑ для нескольких a, по которым можно определить объемную энтальпию дымовых газов при заданных температуре и коэффициенте избытка воздуха.
Большая Энциклопедия Нефти и Газа
Cтраница 1
Теплота сгорания природного газа достаточно точно определяется расчетом по его фракционному составу. [1]
Теплота сгорания природных газов колеблется в широких пределах от 7100 — 7500 к / сал / нж3 для некоторых месторождений Куйбышевско-Бугурусланского района и Восточной Украины, до 15000 ккал / нм3 для попутных газов Грозненского и Туймазинского районов. [2]
Теплота сгорания природного газа, преимущественно в зависимости от содержания инертных газов, изменяется очень сильно, и здесь очень трудно быть точным. [3]
Обратите внимание
Теплота сгорания природного газа ( газовой смеси) определяется экспериментально путем его сжигания в калориметрах. [4]
Теплотой сгорания природного газа называется тепло, выделенное при сгорании единицы объема ( или массы) газа в определенных условиях. Теплота сгорания определяется количеством тепла, выделившегося при охлаждении продуктов сгорания до 0 С и при конденсации образовавшейся влаги. Она известца как общая или полная теплота сгорания. [5]
Так, например, теплота сгорания природного газа, равная 8500 ккал / кг составит 8500 X 4 19 35 615 кдж / кг, или 35 615 Мдж / кг. [6]
Теплота сгорания попутных и газоконденсатных газов значительно вышетеплоты сгорания природных газов и колеблется от 9300 до 14000 ккал на 1 м3 углеводородной части газа. Изучение попутного и газоконден-сатного газов показало, что их состав изменяется не только по годам ( для одного и того же месторождения), но и в различные периоды года. [7]
Теплота сгорания смеси пропан-бутан приблизительно в два раза большетеплоты сгорания природного газа. Температура пламени газа зависит от его состава и полноты сгорания. [8]
Специальные исследования и практика работы в промышленных условиях показывают, что определениетеплоты сгорания природного газа в проточном калориметре характеризуется значительными ошибками даже при очень тщательном выполнении всех требований методики. [9]
Присутствие балластных компонентов, например азота, нежелательно, так как они снижаюттеплоту сгорания природного газа и удорожают его транспорт. [10]
Газ, полученный по методу Холла, имеет самую высокую теплоту сгорания, почти равнуютеплоте сгорания природного газа, поэтому в европейских странах его не применяют в качестве городского газа без смешения с газами, имеющими более низкую теплоту сгорания. [11]
Важно
Общий газовый поток от всех аппаратов из смесителя / вентилятором 2 подается в топку-подогреватель 3, где за счеттеплоты сгорания природного газа подогревается до температуры реакции. Нагретые газы поступают в контактный аппарат 4 и, проходя через слой катализатора 5, окисляются. [13]
Необходимо работать над улучшением конструкций газо-горелочных устройств приборов для сжигания сжиженных газов, теплота сгорания которых почти в три раза превышаеттеплоту сгорания природных газов. [14]
При использовании в качестве топлива производственного газа с преимущественным составом пропан-бутановой смеси следует иметь в виду, что его теплота сгорания примерно втрое вышетеплоты сгорания природного газа. [15]
Страницы: 1 2
Источник: https://www.ngpedia.ru/id509561p1.html
Состав и характеристики топлив
Топливом может быть названо любое вещество, способное при горении (окислении) выделять значительное количество теплоты. По определению, данному Д. И. Менделеевым, «топливом называется горючее вещество, умышленно сжигаемое для получения тепла».
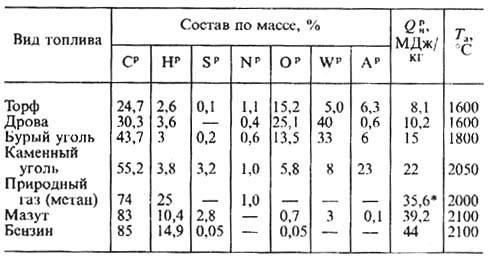
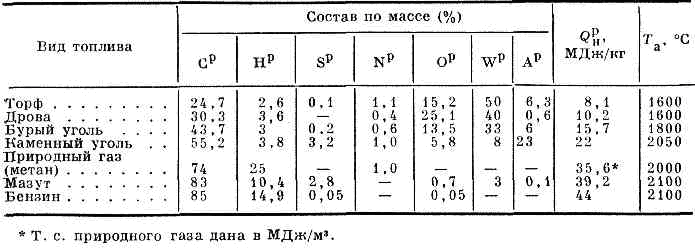
В таблицах ниже представлены основные характеристики различных видов топлив: состав, низшая теплота сгорания, зольность, влажность и т. д.
Примерный состав и теплотехнические характеристики горючей массы твердого топлива
| Топливо | Состав горючей массы, % | Выход летучих веществ,VГ, % | Низшая теплота сгорания,МДж/кг | Жаро- производи- тельность,tmax, °С | RO2 max* продуктовсгорания, % | ||||
| CГ | SГ | HГ | OГ | NГ | |||||
| Дрова | 51 | — | 6,1 | 42,2 | 0,6 | 85 | 19 | 1980 | 20,5 |
| Торф | 58 | 0,3 | 6 | 33,6 | 2,5 | 70 | 8,12 | 2050 | 19,5 |
| Горючий сланец | 60—75 | 4—13 | 7—10 | 12—17 | 0,3—1,2 | 80—90 | 7,66 | 2120 | 16,7 |
| Бурый уголь | 64—78 | 0,3—6 | 3,8—6,3 | 15,26 | 0,6—1,6 | 40—60 | 27 | — | 19,5 |
| Каменный уголь | 75—90 | 0,5—6 | 4—6 | 2—13 | 1-2,7 | 9—50 | 33 | 2130 | 18,72 |
| Полуантрацит | 90—94 | 0,5—3 | 3—4 | 2—5 | 1 | 6—9 | 34 | 2130 | 19,32 |
| Антрацит | 93—94 | 2—3 | 2 | 1—2 | 1 | 3—4 | 33 | 2130 | 20,2 |
* — RO2 = CO2 + SO2
Характеристики жидких топлив, получаемых из нефти
| Топливо | Состав горючей массы, % | Зольностьсухоготоплива,AС, % | Влагарабочеготоплива,WР, % | Низшаятеплотасгораниярабочеготоплива,МДж/кг | |||
| Углерод CГ | Водород HГ | Сера SГ | Кислород и азотOГ + NГ | ||||
| Бензин | 85 | 14,9 | 0,05 | 0,05 | 43,8 | ||
| Керосин | 86 | 13,7 | 0,2 | 0,1 | 43,0 | ||
| Дизельное | 86,3 | 13,3 | 0,3 | 0,1 | Следы | Следы | 42,4 |
| Солярное | 86,5 | 12,8 | 0,3 | 0,4 | 0,02 | Следы | 42,0 |
| Моторное | 86,5 | 12,6 | 0,4 | 0,5 | 0,05 | 1,5 | 41,5 |
| Мазут малосернистый | 86,5 | 12,5 | 0,5 | 0,5 | 0,1 | 1,0 | 41,3 |
| Мазут сернистый | 85 | 11,8 | 2,5 | 0,7 | 0,15 | 1,0 | 40,2 |
| Мазут многосернистый | 84 | 11,5 | 3,5 | 0,5 | 0,1 | 1,0 | 40,0 |
Топливо в том виде, в каком оно поступает для сжигания в топки или в двигатели внутреннего сгорания, называется рабочим.
Название «горючей массы» носит условный характер, т. к. действительно горючими ее элементами являются только углерод, водород и сера. Горючую массу можно характеризовать как топливо, не содержащее золы и в абсолютно сухом состоянии.
Зольность топлива. Золой называют твердый негорючий остаток, остающийся после сжигания топлива в атмосфере воздуха. Зола может быть в виде сыпучей масы с плотностью в среднем 600 кг/м3 и в виде сплавленный пластин и кусков, называемых шлаками, с плотностью до 800 кг/м3.
Влажность топлива определяется по ГОСТ 11014-2001 высушиванием навески при 105 — 110 °С. Максимальная влажность достигает 50% и более и определяет экономическую целесообразность использования данного топлива. Влага снижает температуру в топке и увеличивает обхем дымовых газов.
Состав и теплота сгорания горючих газов
| Наименование газа | Состав сухого газа, % по объему | Низшаятеплотасгораниясухого газаQнс, МДж/м3 | |||||||
| CH4 | H2 | CO | CnHm | O2 | CO2 | H2C | N2 | ||
| Природный | 94,9 | — | — | 3,8 | — | 0,4 | — | 0,9 | 36,7 |
| Коксовый (очищенный) | 22,5 | 57,5 | 6,8 | 1,9 | 0,8 | 2,3 | 0,4 | 7,8 | 16,6 |
| Доменный | 0,3 | 2,7 | 28 | — | — | 10,2 | 0,3 | 58,5 | 4,0 |
| Сжиженный (ориентировочно) | 4 | Пропан 79, этан 6, изобутан 11 | 88,5 |
Низшей теплотой сгорания рабочего топлива называют теплоту, выделяемую при полном сгорании 1 кг топлива, за вычетом теплоты, затраченной на испарение как влаги, содержащейся в топливе, так и влаги, образующейся от сгорания водорода.
Высшей теплотой сгорания рабочего топлива называю теплоту, выделяемую при полном сгорании 1 кг топлива, считая, что образующиеся при сгорании водяные пары конденсируются.
Источник: Основы энергетики : учебник / Г. Ф. Быстрицкий. — 2-е изд., испр. и доп. — М. :КНОРУС, 2011. — 352 с.
Источник: https://energoworld.ru/library/sostav-i-harakteristiki-topliv/
Теплота сгорания газов — Сайт о нефти, газе и нефть сопутствующих продуктах
Для определения состава природного газа лабораториями газовой промышленности используется хроматографический метод анализа. Хроматографы имеют детектор по теплопроводности и аналогичные параметры: чувствительность, точность, время анализа.
С помощью этих приборов определяют углеводородные и неуглеводородные компоненты природного газа. Они служат для непрерывного контроля за химическим составом потоков газа. Результаты анализов записываются регистратором прибора в виде следующих одна за другой хроматограмм.
Такая информация о составе контролируемой газовой смеси дает возможность своевременно обнаружить изменения в ее составе и в случае необходимости принять соответствующие меры.
Ввиду того, что качественный состав, как правило, известен, то необходимо следить лишь за количественным изменением характерных компонентов, показателем чего служат высоты их пиков на хроматограммах.
Теплота сгорания, теплотворная способность, калорийность — понятия равнозначные, характеризующие качество газа при использовании его как топлива.
Высшей теплотой сгорания называется количество теплоты (в кДж), выделяющееся при полном сгорании единицы объема сухого газа, измеренного при нормальных или стандартных условиях, сюда входит и теплота конденсации водяных паров.
Низшей теплотой сгорания называется количество теплоты (в кДж), выделяющееся при полном сгорании единицы объема сухого газа, измеренного при нормальных или стандартных условиях, за вычетом теплоты конденсации водяных паров.
Газы, не содержащие в своем составе водород, имеют только одну теплоту сгорания.
Совет
Оптовые цены промышленности установлены при расчетной калорийности, равной 34333.4 ± 418,7 кДж/м. Пересчет на фактическую калорийность выполняют по формуле, где- цена по прейскуранту;- фактическая низшая калорийность, кДж/м.
При анализах, не связанных с коммерческими расчетами допускается устанавливать теплоту сгорания газа расчетным путем по химическому составу, определенному с помощью хроматографов разных марок.
Расчет по составу газа проводится по формуле
,
где — теплота сгорания чистых компонентов; — процентный объем компонентов смеси.
Пример 1.1. Определить низшую теплоту сгорания смеси газов при нормальных условиях, имеющих определенное процентное содержание (см. табл. 1.2, 1.3).
Решение
где буквенные формулы — компоненты смеси газов, %.
Пересчет теплоты сгорания газа от нормальных условий к стандартным проводится по формуле
Согласно требованиям ОНТП-51-85 Мингазпрома СССР номинальная низшая теплота сгорания топливного газа принимается равной 34 541 Дж/м.
Источник: http://neftyaga.ru/spravochnik-rabotnika-gazovoy-promishlennosti/teplota-sgoraniya-gazov
ПОИСК
Иногда бывает, что при работе иа газах с невысокой теплотой сгорания, например, па природном газе, проще и экономичнее поддерживать более высокие температуры в печах, чем при работе на газе с более высокой теплотой сгорания.
Максимальная температура горения газа, как видно из формулы, зависит не только от его теплоты сгорания, но н от количества образующихся топочных газов н их теплоемкости, т. е. [c.110]
Экспериментально высшую и низшую теплоты сгорания топлив определяют при помощи различных калориметров.
Для измерения теплоты сгорания газов в газопроводах применяются регистрирующие калориметры непрерывного действия. Их калибруют с помощью так называемого водяного калориметра.
Обратите внимание
Принцип действия его состоит в том, что газ, подаваемый с определенной скоростью, сжигается в камере сгорания и выделяющееся тепло затрачивается на повышение температуры проходящей через калориметр воды. [c.76]
Величина Q»p — низшая теплота сгорания газа, отнесенная к 1 м сухих топочных газов, образующихся при сжигании топлива в стехиометрическом объеме воздуха (берется из табл. 1У-2). Приведенные в формулах величины (С02) ух, (СО) [c.134]
В течение ряда лет неоднократно изучалась и в отдельных случаях находила практическое воплощение идея использования продуктов предварительной газификации топлива в тепловых двигателях. Так, в 20—30-е годы широко использовали на автомобилях продукты газификации твердого топлива — древесные чурки, древесный и каменный уголь, торфяные и соломенные брикеты и др.
Газификация осуществлялась в специальном газогенераторе, установленном на автомобиле (такие автомобили называли газогенераторными). Газогенераторная установка включала агрегаты очистки и охлаждения получаемого газа и приспособления для розжига топлива и обеспечения пуска двигателя. Основной топливный газ, получаемый при газификации, — оксид углерода.
Кроме того, в продуктах газификации содержались водород, метан и другие горючие газы. Например, средний состав газа, получаемого из древесных чурок с абсолютной влажностью 20%, таков 20,9% (об.) СО, 16,1% (об.) На, 2,3% (об.) СН4, 0,2% -(об.) С Н , 9,2% (об.) СО2, 1,6% (об.) О2 и 49,7% (об.) N2.
Теплота сгорания газа — около 5 МДж/м а горючей смеси с воздухом — 2,39 МДж/м . [c.182]
Теплота сгорания газа — это количество тепла, выделяющегося при сгорании единицы объема газа с воздухом в стандартных условиях, с учетом конденсации водяного пара, образовавшегося в процессе горения (высшая теплота сгорания), или с учетом сохранения воды в парообразном состоянии (низшая, теплота сгорания). [c.35]
Содержание двуокиси углерода в газе при его транспортировке не вызывает особых проблем, если ие считать, что она снижает теплоту сгорания газа. Обычно СОз извлекают из газа в коммерческих целях или для того, чтобы повысить теплоту сгорания газа.
Поэтому иногда выгодно применять для очистки реагенты, селективные по отношению к H2S или СО,- Селективность во многих процессах контролируется поддержанием параметров процесса, однако при регенерации из раствора реагента удаляется как HjS, так и СОо. [c.
267]
Важно
Теплота сгорания газа, кДж/м 15 500 16 470 27200 32 200 [c.47]
Например, при замедленном коксовании гудрона (р = = 0,975 г/см ) получили 6,2% газа, 12,1% бензина (р = = 0,74 г/см ), 39,4% легкого газойля (р = 0,86 г/см ), 22,7% тяжелого газойля (р = 0,91 г/см ), 19,6% кокса.
Определим теплоту процесса по теплотам сгорания сырья и продуктов. Использование уравнения, связывающего ДЯс с плотностью для жидких нефтепродуктов, а также табличных данных о теплотах сгорания газа и кокса дает [c.
132]
Низшая теплота сгорания газа [c.22]
Среднее отношение Иг СО в газе Теплота сгорания газа (высшая), МДж/м Термический к. п. д. газогенератора, °/ [c.94]
Диапазон производительности горелок, разработанных различными проектными институтами, примерно один и тот же.
Однако по конструкции и размерам отдельных деталей инжекционные горелки отличаются друг от друга, поскольку расчет производится не по единой общепринятой методике, а с различными допущениями.
Некоторые исходные данные (теплота сгорания газа, плотность) также различаются. [c.341]
Для предотвращения выгорания катализатора (платина или рений) максимальную температуру процесса каталитического сжигания ограничивают 815 °С.
Совет
Каталитическое сжигание применяют для отходящих газов, содержание углеводородов в которых на 25% ниже минимального взрывоопасного предела. Если теплота сгорания газов достаточна для достижения температур, приводящих к выгоранию катализатора, их разбавляют атмосферным воздухом.
Однако обычно отходящий газ содержит значительно меньше горючих материалов, чем требуется для поддержания устойчивого горения, и поэтому его предварительно нагревают до температуры проведения каталитической реакции.
При использовании систем каталитического сжигания часто получают чистый нагретый газ, который затем можно использовать в установках утилизации тепла отходящих газов, значи- [c.143]
Теплота сгорания газа [c.51]
Отходяш,ие газы содержат 80—85% оксида углерода, 8— 10% азота, 2—3% воды, а также -водород, фосфин, диоксид углерода, фосфор.
Теплота сгорания газов около 11 МДж/м Наиболее приемлемым решением проблемы использования тепла отходящих газов является их применение в качестве топлива для технологических аппаратов или для выработки пара.
Одно из условий использования тепла отходящих газов — создание специального теплообменного оборудования, устойчивого в агрессивной среде. [c.226]
Определяют теплоту сгорания сырья и продуктов любым доступным методом. Теплоту сгорания газа можно рассчитать по его составу, либо подобрать в литературе. Данные о теплоте сгорания бутана, жидких нефтепродуктов и кокса представлены в табл. И. [c.204]
ТЕПЛОТА СГОРАНИЯ ГАЗА И ЕЕ ОПРЕДЕЛЕНИЕ Понятие о теплоте сгорания газов [c.64]
Обратите внимание
Теплота сгорания газа вычисляется по компонентному составу и теплоте сгорания отдельных компонентов относительная плотность вычисляется по компонентному составу и плотности отдельных компонентов число Воббе представляет собой отношение теплоты сгорания и корня квадратного из плотности [c.62]
Очистка газа от двуокиси углерода необходима лишь при высоком содержании ее, т. е. в случаях резкого снижения теплоты сгорания газа или опасности коррозии газопровода вследствие взаимодействия его с влажным перекачиваемым газом. В этих условиях снижение содержания СОг ДО 3 об.
% считается вполне нормальным. Если природный газ подлежит сжижению, необходима полная очистка его как от НаЗ, так и от СОг, поскольку температура замерзания СОг и НгЗ выше, чем других компонентов, и затвердевшие вещества будут мешать нормальной работе установки. [c.
32]
Рассмотрим работу бытовой установки, оборудование которой рассчитано на природный газ, и предприятия, на котором до подачи природного газа было необходимо иметь газовое топливо. В обоих случаях газы должны быть взаимозаменяемы, т. е. иметь. одинаковые числа Воббе. Так как относительные плотности природного газа и СНГ различны (для природного газа р
Смотреть страницы где упоминается термин Теплота сгорания газов: [c.230] [c.365] [c.155] [c.53] [c.516] [c.24] [c.9] [c.45] [c.103] [c.135] [c.101] Смотреть главы в:
Природный газ -> Теплота сгорания газов
Справочник по основной химической промышленности Издание 2 Часть1 -> Теплота сгорания газов
Сжигание природного газа -> Теплота сгорания газов
Инструментальные методы химического анализа (1960) — [ c.368 ]
Инструментальные методы химического анализа (1960) — [ c.368 ]
Справочник по физико-техническим основам криогенетики Издание 3 (1985) — [ c.196 ]
Справочник по физико-техническим основам глубокого охлаждения (1963) — [ c.151 ]
Теплота сгорания
© 2019 chem21.info Реклама на сайте
Источник: https://www.chem21.info/info/647608/
Теплота сгорания сжиженного газа
Доброе утро дорогие друзья. За маленький период времени , нам довольно много раз задавали один и тот же вопрос. Мы решили ответить на него в этой статье.
Какова теплота сгарания сжиженного газа?
Начнем с главного, что такое теплота сгорания (она же – теплотворная способность) – это количество теплоты, выделяемое в результате полного сгорания данного вида топлива объемом 1 м3 или массой 1 кг (теплота сгорания сжиженного газа может рассчитываться и по массе, и по объему и измеряется в МДж/кг и МДж/л, соответственно).
Чем больше теплотворная способность сжиженного газа (а сжиженный газ бывает углеводородным – СУГ – или природным), тем меньшее количество топлива необходимо для получения одного и того же количества теплоты.
Теплотворная способность сжиженного газа (пропан-бутана) находится на уровне 46,8 МДж/к или 25,3 МДж/л. При переводе показателей сжиженного углеводородного газа из мегаджоулей (МДж) в киловатт-часы (кВТ*ч) получаем удельную теплоту сгорания газа, равную 13,0 кВт*ч/кг или 7,0 кВт*ч/л.
Важно
Теплота сгорания сжиженного углеводородного газа делает этот вид топлива наиболее дешевым среди альтернатив (электричества, дизельного топлива, угля, дров), за исключением, возможно, природного газа метана. Однако не стоит забывать, что сжиженный газ пропан-бутан гораздо дешевле при подключении (при автономной газификации), чем метан из централизованного газопровода.
Цена магистрального газа растет стремительными темпами, в то время, как цена сжиженного углеводородного топлива (газа пропан-бутан) остается стабильной в регионе Санкт-Петербурга и Ленинградской области. А растущая популярность автономного газа делает отрасль еще более конкурентоспособной за счет увеличения потребления сжиженного топлива.
Стоимость 1кВт*ч за счет использования газа намного ниже, чем у альтернативных видов топлива: при удельной теплоте сгорания в 46,8 МДж на 1 кг и плотности (приблизительной) в 0,555 кг/л, имеющихся КПД газгольдеров на уровне 95% и стоимости газа 18,50 руб. за 1 литр, мы получим 2,7 руб. за 1 кВт*ч (похожая цифра получается и для газа метана). Тогда как для дизельного топлива стоимость 1 кВт*ч превысит 4,5 руб.
Теплотворная способность зависит от точного состава газа – пропан-бутан делится на «летний» и «зимний». В первом случае процентное соотношение пропана и бутана примерно одинаково – по 50% каждого газа. В случае «зимнего» СУГ в составе преобладает пропан – до 90% объема.
Теплота сгорания «летнего» и «зимнего» пропан-бутана будет незначительно отличаться, но такое деление необходимо для соблюдения безопасности эксплуатации системы автономного газоснабжения и недопущения ситуации, когда емкость для хранении пропан-бутана получает повреждения или взрывается из-за слишком сильного расширения газов.
Вот как то так, дорогие друзья . Надеюсь мы смогли в очередной раз ответить на интересующий вас вопрос. Если у вас возник какой либо вопрос по нашей теме , пишите нам мы будем рады написать статью или проконсультировать вас онлайн.
Источник: https://gazekoset.ru/stati/raznoe/139-teplota-sgoraniya-szhizhennogo-gaza
Газовое топливо
Котлы типа ДЕ потребляют от 71 до 75 м3 природного газа на получение одной тонны пара. Стоимость газа в России на сентябрь 2008г. составляет 2,44 рубля за кубометр. Следовательно, тонна пара будет стоить 71 × 2,44 = 173 руб 24 коп. Реальная стоимость тонны пара на заводах составляет для котлов ДЕ составляет не менее 189 рублей за тонну пара.
Котлы типа ДКВР потребляют от 103 до 118 м3 природного газа на получение одной тонны пара. Минимальная расчетная стоимость тонны пара для этих котлов составляет 103 × 2,44 = 251 руб 32 коп. Реальная же стоимость пара по заводам составляет не менее 290 рублей за тонну.
Как рассчитать максимальный расход природного газа на паровой котел ДЕ-25? Это техническая характеристика котла. 1840 кубиков в час. Но можно и расчитать. 25 тонн (25 тыс кг) надо умножить на разность энтальпий пара и воды (666,9-105) и всё это разделить на к.п.д котла 92,8% и теплоту сгорания газа. 8300. и все
Совет
Искуственные горючие газы являются топливом местного значения, поскольку имеют значительно меньшую теплоту сгорания. Основными горючими элементами их являются окись углерода СО и водород Н2. Эти газы используют в пределах того производства, где они получаются в качестве топлива технологических и энергетических установок.
Все природные и искусственные горючие газы являются взрывоопасными, способны воспламеняться на открытом огне или искре. Различают нижний и верхний предел взрываемости газа, т.е. наибольшую и наименьшую процентную его концентрацию в воздухе.
Нижний предел взрываемости природных газов колеблется от 3% до 6%, а верхний — от 12% до 16%. Все горючие газы способны вызывать отравление организма человека.
Основными отравляющими веществами горючих газов являются: окись углерода СО, сероводород H2S, аммиак NH3.
Природные горючие газы, так и искусственные бесцветны (невидимы), не имеют запаха, что делает их опасными при проникновении во внутреннее помещение котельной через неплотности газопроводной арматуры. Во избежание отравления горючие газы следует обрабатывать одорантом — веществом с неприятным запахом.
Для промышленных целей окись углерода получают путём газификации твёрдого топлива, т. е. превращения его в газообразное топливо. Так можно получить окись углерода из любого твёрдого топлива — ископаемых углей, торфа, дров и т. д.
Процесс газификации твердого топлива показан на лабораторном опыте (рис.1). Заполнив тугоплавкую трубку кусочками древесного угля, сильно нагреем её и будем пропускать кислород из газометра.
Выходящие из трубки газы пропустим через промывалку с известковой водой и затем подожжём. Известковая вода мутится, газ горит синеватым пламенем.
Это указывает на наличие двуокиси СО2 и окиси углерода СО в продуктах реакции.
Обратите внимание
Образование этих веществ можно объяснить тем, что при соприкосновении кислорода с раскалённым углем последний сначала окисляется в двуокись углерода: С + О2 = СО2
Затем, проходя через раскалённый уголь, углекислый газ частично восстанавливается им до окиси углерода: СО2 + С = 2СО
Рис. 1. Получение окиси углерода (лабораторный опыт).
В промышленных условиях газификацию твёрдого топлива осуществляют в печах, называемых газогенераторами.
Образующаяся смесь газов называется генераторным газом.
Устройство генератора газа показано на рисунке. Он представляет собой стальной цилиндр высотой около 5 м и диаметром примерно 3,5 м, футерованный внутри огнеупорным кирпичом. Сверху газогенератор загружается топливом; снизу через колосниковую решётку вентилятором подаётся воздух или водяной пар.
Кислород воздуха реагирует с углеродом топлива, образуя углекислый газ, который, поднимаясь вверх через слой раскалённого топлива, восстанавливается углеродом до окиси углерода.
Если в генератор вдувать только воздух, то получается газ, который в своём составе содержит окись углерода и азот воздуха (а также некоторое количество СО2 и других примесей) . Такой генераторный газ называется воздушным газом.
Если же в генератор с раскалённым углем вдувать водяной пар, то в результате реакции образуются окись углерода и водород: С + Н2О = СO + Н2
Эта смесь газов называется водяным газом. Водяной газ обладает более высокой теплотворной способностью, чем воздушный, так как в его состав наряду с окисью углерода входит и второй горючий газ — водород. Водяной газ (синтез газ), один из продуктов газификациии топлив.
Важно
Водяной газ состоит главным образом из СО (40%) и Н2 (50%). Водяной газ — это топливо (теплота сгорания 10 500 кДж/м3, или 2730 ккал/мг) и одновременно сырье для синтеза метилового спирта.
Водяной газ, однако, нельзя получать продолжительное время, так как реакция образования его эндотермическая (с поглощением теплоты), и поэтому топливо в генераторе остывает.
Чтобы поддерживать уголь в раскалённом состоянии, вдувание водяного пара в генератор чередуют с вдуванием воздуха, кислород которого, как известно, реагирует с топливом с выделением тепла.
В последнее время для газификации топлива стали широко применять парокислородное дутьё. Одновременное продувание через слой топлива водяного пара и кислорода позволяет вести процесс непрерывно, значительно повышать производительность генератора и получать газ с высоким содержанием водорода и окиси углерода.
Современные газогенераторы — это мощные аппараты непрерывного действия.
Чтобы при подаче топлива в газогенератор горючие и ядовитые газы не проникали в атмосферу, загрузочный барабан делают двойным.
В то время как топливо поступает в одно отделение барабана, из другого отделения топливо высыпается в генератор; при вращении барабана эти процессы повторяются, генератор же всё время остаётся изолированным от атмосферы.
Равномерное распределение топлива в генераторе осуществляется при помощи конуса, который может устанавливаться на различной высоте. Когда его опускают, уголь ложится ближе к центру генератора, когда конус поднимают, уголь отбрасывается ближе к стенкам генератора.
Удаление золы из газогенератора механизировано. Колосниковая решётка, имеющая конусовидную форму, медленно вращается электродвигателем. При этом зола смещается к стенкам генератора и особыми приспособлениями сбрасывается в зольный ящик, откуда периодически удаляется.
Совет
Первые газовые фонари зажглись в Санкт-Петербурге на Аптекарском острове в 1819 году. Газ, который применялся, получали путем газификации каменного угля. Он назывался светильным газом.
Великий русский учёный Д. И. Менделеев (1834-1907) впервые высказал идею о том, что газификацию каменного угля можно производить непосредственно под землёй, не поднимая его наружу. Царское правительство не оценило этого предложения Менделеева.
Идею подземной газификации горячо поддержал В. И. Ленин. Он назвал её «одной из великих побед техники». Подземную газификацию осуществило впервые Советское государство. Уже до Великой Отечественной войны в Советском Союзе работали подземные генераторы в Донецком и Подмосковном угольных бассейнах.
Представление об одном из способов подземной газификации даёт рисунок 3. В угольный пласт прокладывают две скважины, которые внизу соединяют каналом.
Уголь поджигают в таком канале у одной из скважин и подают туда дутьё.
Продукты горения, двигаясь по каналу, взаимодействуют с раскалённым углем, в результате чего образуется горючий газ как и в обычном генераторе. Газ выходит на поверхность через вторую скважину.
Генераторный газ широко применяется для обогрева промышленных печей — металлургических, коксовых и в качестве топлива в автомобилях (рис. 4).
Рис. 3. Схема подземной газификации каменного угля.
Из водорода и окиси углерода водяного газа синтезируют ряд органических продуктов, например жидкое топливо. Синтетическое жидкое топливо — горючее (в основном бензин), получаемое синтезом из окиси углерода и водорода при 150-170 гр Цельсия и давлении 0,7 — 20 МН/м2 (200 кгс/см2), в присутствии катализатора (никель, железо, кобальт).
Первое производство синтетического жидкого топлива организовано в Германии во время 2й Мировой войны в связи с нехваткой нефти. Широкого распространения синтетическое жидкое топливо не получило из-за его высокой стоимости. Водяной газ используют для производства водорода.
Обратите внимание
Для этого водяной газ в смеси с водяным паром нагревают в присутствии катализатора и в результате получают водород дополнительно к уже имеющемуся в водяном газе: СО+Н2О=СО2+Н2
Из полученной смеси удаляют двуокись углерода, растворяя её в воде под давлением. Водород применяют для синтеза аммиака и для других целей.
Источник: http://www.sergey-osetrov.narod.ru/Projects/Boiler/GAS_FUEL.htm