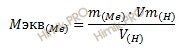Определение
эквивалентной массы металла
Цель работы:
определение эквивалентной массы металла,
которая находится методом вытеснения
водорода из раствора кислоты.
Основные
теоретические положения: эквивалентом
вещества называется такое его количество,
которое соединяется с одним молем атомов
водорода или замещает то же количество
атомов водорода в химических реакциях.
Эквивалентной массой называется масса
одного эквивалента вещества.
Формулы для
вычисления, перечень символов: Согласно
закону эквивалентов массы, вступающие
в реакцию веществ, пропорциональны
эквивалентам этих веществ:
, где
М1 и М2 – массы реагирующих веществ, кг;
Э1 и Э2 – их эквиваленты.
Эквивалентная
масса элемента:
Э = А/n , где А –
масса одного моля атомов элемента;
n –
его валентность.
Методика
эксперимента
-
Получили навеску
опилок металла у преподавателя. -
Перед началом
опыта проверили сосуд на герметичность. -
Подготовили
эвдиометр для собирания водорода.
Заполнили его до краев водой (с помощью
стакана), зажали открытый конец пальцем
и, перевернув, погрузили в чашку с водой. -
С помощью мерного
цилиндра отмерили 5 мл раствора соляной
кислоты HCl
(в объемном соотношении I:I),
влили ее через воронку в пробирку так,
чтобы не замочить стенки изнутри. Держа
пробирку в слегка наклонном положении,
поместили внутрь на сухую стенку навеску
опилок металла в папирусной бумаге,
закрыли пробирку пробкой и конец
газоотводной трубки подвели под водой
внутрь эвдиометра. -
Повернули пробирку
в вертикальное положение (навеска
металла при этом упала в кислоту) и
поставили в деревянный штатив. После
окончания химической реакции (прекращение
выделения пузырьков газа) дали охладиться
системе до комнатной температуры в
течении 8-10 минут. -
Атмосферное
давление записали по показаниям
барометра:
1 мм рт. ст. = 1, 333 ·
102
Па
763 мм рт. ст. =
1001707,9 Па
-
Комнатную
температуру зафиксировали ртутным
термометром:
22 ºС + 273 = 295 К
-
Значение парциального
давления водяных паров h
при температуре комнаты нашли по
таблице:
h = 2643,3
Па
-
Объем полученного
водорода Vt
= 31 · 10-6
привели к нормальным условиям:
;
V0
– объем выделившегося водорода при
нормальных условиях (Т0
= 273 К, Р0
= 101325 Па), м3
РН2
– парциальное давление водорода, Па;
Т – температура
опыта.
-
Используя закон
эквивалентов, рассчитали эквивалентную
массу металла:
ЭМе
/ 0,0112 = mМе
/ V0
ЭМе
=
м3/моль
ЭМе
– эквивалентная масса металла, кг/моль;
mMe
– навеска металла, кг;
0,0112 – эквивалентный
объем водорода при нормальных условиях,
м3/моль.
11. Вычислим по
соотношению Э = А/n теоретическую
эквивалентную массу металла Эт
Эт
(Zn)
=
м3/моль
12. Вычислим
абсолютную и относительную погрешности
в определении эквивалентной массы
металла в процентах:
Уравнение химической
реакции в молекулярном и ионном виде:
2
+ Zn ZnCl2
+ H2
2
+ 2Cl—
+ Zn0
Zn2+
+ 2Cl—
+ 2H0
2
+ Zn0
Zn2+
+ 2H0
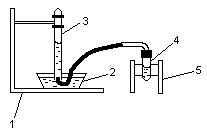
Схема установки:
Рис 1. Схема
установки: 1
– штатив; 2 – чашка с водой; 3 – эвдиометр;
4 – пробирка с газоотводной трубкой; 5
– деревянный штатив.
Экспериментальные
результаты:
|
Условия |
|||||
|
Навеска |
Температура |
Атмосферное |
Парциальное |
Объем |
Парциальное |
|
0,0880 |
295 |
101707,9 |
2643,3 |
31· |
99064,6 |
Вывод: В
результате работы был исследован способ
определения эквивалентной массы металла,
которая находится методом вытеснения
водорода из раствора кислоты.
Соседние файлы в предмете Химия
- #
- #
- #
- #
- #
- #
- #
- #
Эквивалентная масса металла
При растворении в кислоте металла массой 11,9 грамм выделился водород объемом 2,24 литра (нормальные условия). Чему равна эквивалентная масса металла ( Мэкв) и фактор эквивалентности металла (fэкв).
Решение
Согласно закону эквивалентов: массы (объемы)реагирующих веществ пропорциональны молярным массам (объемам) эквивалента этих веществ.
Учитывая, что эквивалентный объем водорода (H) равна 11,2 л, определим эквивалентную массу металла по закону эквивалентов:
Откуда выразим эквивалентную массу металла:
Получаем:
M экв (Me) = 11,9 ∙ 11,2 / 2,24 = 59,5 (г/моль).
Молярная масса эквивалента – равна произведению фактора эквивалентности на молярную массу вещества.
Если валентность металла z (Ме) = 1, то М = Мэ = 59,5 г/моль — одновалентного металла с такой молярной массой нет (смотри таблицу Менделеева).
Если z(Ме) = 2, то М = 2Мэ = 119 г/моль – двухвалентного металла с такой молярной массой нет.
Если z(Ме) = 3, то М = 3Мэ = 178,5 г/моль – гафний.
Фактор эквивалентности металла 1/3.
Ответ:
эквивалентная масса металла 59,5 г/моль;
фактор эквивалентности металла 1/3.
Как вычислить эквивалентные массы оксида и металла
Эквивалент – такое количество химического элемента, которое либо связывает, либо замещает один моль атомов водорода. Соответственно, масса одного эквивалента называется эквивалентной массой (Мэ), и выражается в г/моль. Перед учащимися на химии часто ставят задачу определить эквивалентную массу того или иного вещества (соединения). Например, металла и образованного им оксида.

Инструкция
В первую очередь следует запомнить несколько простых правил. Если речь идет о металле, его эквивалентная масса рассчитывается по формуле: Мэ=М/В, где М – атомная масса металла, а В – его валентность. Рассмотрите это правило на конкретных примерах.
Кальций (Са). Его атомная масса 40,08. Округленно примите ее за 40. Валентность равна 2. Следовательно, Мэ(Са) = 40/2 = 20 г/моль. Алюминий (Al). Его атомная масса 26,98. (Округленно 27). Валентность равна 3. Таким образом, Мэ(Al) = 27/3 = 9 г/моль.
Перечисленные способы применимы, если речь идет о чистых металлах. А если они входят в состав какого-либо соединения, например, тех же оксидов? Тут надо запомнить другое правило: эквивалентная масса оксида вычисляется по формуле: Мэ + Мо, где Мо – эквивалентная масса кислорода. Она, соответственно, рассчитывается по уже рассмотренной формуле М/В, то есть 16/2 = 8.
Предположим, у вас есть основной оксид алюминия, Al2O3. Как посчитать его эквивалентную массу? Очень просто: 27/3 + 16/2 = 17 г/моль.
Есть ли другой способ определения эквивалентных масс металла и его оксида? Да, и весьма эффективный. Он основан на так называемом законе эквивалентов, согласно которому все вещества реагируют друг с другом в эквивалентных количествах. Например: металл массой 33,4 грамма вступил в реакцию окисления с кислородом воздуха. В результате получился оксид общей массой 43 грамма. Требуется определить эквивалентные массы самого металла и его оксида.
Сначала вычислите, сколько кислорода соединилось с металлом в ходе этой реакции: 43 – 33,4 = 9,6 грамм. Согласно закону эквивалентов, эта масса во столько же раз больше эквивалентной массы кислорода (которая, напомним, равна 8), во сколько раз эквивалентная масса металла меньше его первоначального количества. То есть 33,4/Мэ(ме) = 9,6/8. Следовательно, Мэ(ме) = 33,4*8/9,6 = 27,833 г/моль, или округленно 27,8 г/моль. Такова эквивалентная масса металла.
Эквивалентную же массу оксида найдите следующим действием: 27,8 + 8 = 35,8 г/моль.
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
Материалы из методички: Сборник задач по теоретическим основам химии для студентов заочно-дистанционного отделения / Барботина Н.Н., К.К. Власенко, Щербаков В.В. – М.: РХТУ им. Д.И. Менделеева, 2007. -155 с.
Эквивалент. Закон эквивалентов
Эквивалент – реальная или условная частица вещества Х, которая в данной кислотно-основной реакции или реакции обмена эквивалентна одному иону водорода Н+ (одному иону ОН— или единичному заряду), а в данной окислительно-восстановительной реакции эквивалентна одному электрону.
Фактор эквивалентности fэкв(X) – число, показывающее, какая доля реальной или условной частицы вещества Х эквивалентна одному иону водорода или одному электрону в данной реакции, т.е. доля, которую составляет эквивалент от молекулы, иона, атома или формульной единицы вещества.
Наряду с понятием “количество вещества”, соответствующее числу его моль, используется также понятие количество эквивалентов вещества.
Закон эквивалентов: вещества реагируют в количествах, пропорциональных их эквивалентам. Если взято n(экв1) моль эквивалентов одного вещества, то столько же моль эквивалентов другого вещества n(экв2) потребуется в данной реакции, т.е.
n(экв1) = n(экв2) (2.1)
При проведении расчетов необходимо использовать следующие соотношения:
1. Молярная масса эквивалента вещества X равна его молярной массе, умноженной на фактор эквивалентности:
Мэкв(X) = М(X)× fэкв(X). (2.2)
2. Количество эквивалентов вещества X определяется делением его массы на молярную массу эквивалента:
nэкв(X) = m(X)/Мэкв(X). (2.3)
3. Объём моль-эквивалента газа Х при н.у. равен молярному объёму газа, умноженному на фактор эквивалентности:
Vэкв(X) = V(X) × fэкв(X) = 22,4× fэкв(X). (2.4)
4. Молярная масса эквивалента сложного вещества равна сумме молярных масс эквивалентов составляющих это вещество атомов (ионов).
5. Молярная масса эквивалента оксида равна молярной массе эквивалента элемента плюс молярная масса эквивалента кислорода.
6. Молярная масса эквивалента гидроксида металла равна молярной массе эквивалента металла плюс молярная масса эквивалента гидроксила, например:
М[½Са(ОН)2] = 20 + 17 = 37 г/моль.
7. Молярная масса эквивалента сульфата металла равна молярной массе эквивалента металла плюс молярная масса эквивалента SO42-, например,
М(½ СаSO4) = 20 + 48 = 68 г/моль.
Эквивалент в кислотно-основных реакциях
На примере взаимодействия ортофосфорной кислоты со щелочью с образованием дигидро-, гидро- и среднего фосфата рассмотрим эквивалент вещества H3PO4.
H3PO4 + NaOH = NaH2PO4 + H2O, fэкв(H3PO4) =1.
H3PO4 + 2NaOH = Na2HPO4 + 2H2O, fэкв(H3PO4) =1/2.
H3PO4 + 3NaOH = Na3PO4 + 3H2O, fэкв(H3PO4) =1/3.
Эквивалент NaOH соответствует формульной единице этого вещества, так как фактор эквивалентности NaOH равен единице. В первом уравнении реакции молярное соотношение реагентов равно 1:1, следовательно, фактор эквивалентности H3PO4 в этой реакции равен 1, а эквивалентом является формульная единица вещества H3PO4.
Во втором уравнении реакции молярное отношение реагентов H3PO4 и NaOH составляет 1:2, т.е. фактор эквивалентности H3PO4 равен 1/2 и её эквивалентом является 1/2 часть формульной единицы вещества H3PO4 .
В третьем уравнении реакции количество веществ реагентов относятся друг к другу как 1:3. Следовательно, фактор эквивалентности H3PO4 равен 1/3, а её эквивалентом является 1/3 часть формульной единицы вещества H3PO4.
Таким образом, эквивалент вещества зависит от вида химического превращения, в котором принимает участие рассматриваемое вещество.
Следует обратить внимание на эффективность применения закона эквивалентов: стехиометрические расчёты упрощаются при использовании закона эквивалентов, в частности, при проведении этих расчётов отпадает необходимость записывать полное уравнение химической реакции и учитывать стехиометрические коэффициенты. Например, на взаимодействие без остатка 0,25 моль-экв ортофосфата натрия потребуется равное количество эквивалентов вещества хлорида кальция, т.е. n(1/2CaCl2) = 0,25 моль.
Эквивалент в окислительно-восстановительных реакциях
Фактор эквивалентности соединений в окислительно-восстановительных реакциях равен:
fэкв(X) = 1/n, (2.5)
где n – число отданных или присоединенных электронов.
Для определения фактора эквивалентности рассмотрим три уравнения реакций с участием перманганата калия:
2KMnO4 + 5Na2SO3 + 3H2SO4 = 5Na2SO4 + 2MnSO4 + K2SO4 + 3H2O.
2KMnO4 + 2Na2SO3 + H2O = 2Na2SO4 + 2MnO2 + 2KOH.
2KMnO4 + Na2SO3 + 2NaOH = Na2SO4 + K2MnO4 + Na2MnO4 + H2O.
В результате получаем следующую схему превращения KMnO4.
в кислой среде: Mn+7 + 5e = Mn+2
в нейтральной среде: Mn+7 + 3e = Mn+4
в щелочной среде: Mn+7 + 1e = Mn+6
Схема превращений KMnO4 в различных средах
Таким образом, в первой реакции fэкв(KMnO4) = 1/5, во второй – fэкв(KMnO4) = 1/3, в третьей – fэкв(KMnO4) = 1.
Следует подчеркнуть, что фактор эквивалентности дихромата калия, реагирующего в качестве окислителя в кислой среде, равен 1/6:
Cr2O72- + 6e + 14H+ = 2 Cr3+ + 7H2O
Примеры решения задач
Задача 1. Определить фактор эквивалентности сульфата алюминия, который взаимодействует со щелочью.
Решение. В данном случае возможно несколько вариантов ответа:
Al2(SО4)3 + 6 KOH = 2 Аl(ОН)3 + 3 K2SО4, fэкв(Al2(SО4)3) = 1/6,
Al2(SО4)3 + 8 KOH(изб) = 2 K[Al(OH)4 ] + 3 K2SО4, fэкв (Al2(SО4)3) = 1/8,
Al2(SО4)3 + 12KOH(изб) = 2K3[Al(OH)6] + 3K2SО4, fэкв (Al2(SО4)3) = 1/12.
Задача 2. Определить факторы эквивалентности Fe3О4 и KCr(SO4)2 в реакциях взаимодействия оксида железа с избытком хлороводородной кислоты и взаимодействия двойной соли KCr(SO4)2 со стехиометрическим количеством щёлочи КОН с образованием гидроксида хрома (III).
Решение.
Fe3О4 + 8 НСl = 2 FeСl3 + FeСl2 + 4 Н2О, fэкв(Fe3О4) = 1/8,
KCr(SO4)2 + 3 КОН = 2 K2SO4 + Сr(ОН)3, fэкв(KCr(SO4)2) = 1/3.
Задача 3. Определить факторы эквивалентности и молярные массы эквивалентов оксидов CrО, Cr2О3 и CrО3 в кислотно-основных реакциях.
CrО + 2 HCl = CrCl2 + H2О; fэкв(CrО) = 1/2,
Cr2О3 + 6 HCl = 2 CrCl3 + 3 H2О; fэкв(Cr2О3) = 1/6,
CrО3 – кислотный оксид. Он взаимодействует со щёлочью:
CrО3 + 2 KОH = K2CrО4 + H2О; fэкв(CrО3) = 1/2.
Молярные массы эквивалентов рассматриваемых оксидов равны:
Мэкв(CrО) = 68(1/2) = 34 г/моль,
Мэкв(Cr2О3) = 152(1/6) = 25,3 г/моль,
Мэкв(CrО3) = 100(1/2) = 50 г/моль.
Задача 4. Определить объём 1 моль-экв О2, NH3 и H2S при н.у. в реакциях:
4 NH3 + 3 О2 2 N2 + 6 H2О;
4 NH3 + 5 О2 4 NO + 6 H2О;
2 H2S + 3 О2 2 SО2 + 2 H2О.
Решение.
Vэкв(О2) = 22,4× 1/4 = 5,6 л.
Vэкв(NH3) = 22,4× 1/3 = 7,47 л – в первой реакции.
Vэкв(NH3) = 22,4× 1/5 = 4,48 л – во второй реакции.
В третьей реакции для сероводорода Vэкв(H2S)=22,4 1/6 = 3,73 л.
Задача 5. 0,45 г металла вытесняют из кислоты 0,56 л (н.у.) водорода. Определить молярную массу эквивалента металла, его оксида, гидроксида и сульфата.
Решение.
nэкв(Ме) = nэкв(Н2) = 0,56:(22,4× 1/2) = 0,05 моль.
Мэкв(X) = m(Ме)/nэкв(Мe) = 0,45:0,05 = 9 г/моль.
Мэкв(МеxOy) = Мэкв(Ме) + Мэкв(O2) = 9 + 32× 1/4 = 9 + 8 = 17 г/моль.
Мэкв(Ме(OH)y) = Мэкв(Ме) + Мэкв(OH—) = 9+17 = 26 г/моль.
Мэкв(Меx(SO4)y) = Мэкв(Ме) + Мэкв(SO42-) = 9 + 96× 1/2 = 57 г/моль.
Задача 6. Рассчитать массу перманганата калия, необходимую для окисления 7,9 г сульфита калия в кислой и нейтральной средах.
Решение.
fэкв(K2SО3) = 1/2 (в кислой и нейтральной среде).
Мэкв(K2SО3) = 158× 1/2 = 79 г/моль.
nэкв (KMnO4) = nэкв(K2SО3) = 7,9/79 = 0,1 моль.
В кислой среде Мэкв(KMnO4) = 158·1/5 = 31,6 г/моль, m(KMnO4) = 0,1·31,6 = 3,16 г.
В нейтральной среде Мэкв (KMnO4) = 158·1/3 = 52,7 г/моль, m(KMnO4) = 0,1·52,7 =5,27 г.
Задача 7. Рассчитать молярную массу эквивалента металла, если оксид этого металла содержит 47 мас.% кислорода.
Решение.
Выбираем для расчётов образец оксида металла массой 100 г. Тогда масса кислорода в оксиде составляет 47 г, а масса металла – 53 г.
В оксиде: nэкв (металла) = nэкв(кислорода). Следовательно:
m(Ме):Мэкв(Ме) = m(кислорода):Мэкв(кислорода);
53:Мэкв(Ме) = 47:(32·1/4). В результате получаем Мэкв(Ме) = 9 г/моль.
Задачи для самостоятельного решения
2.1. Молярная масса эквивалента металла равна 9 г/моль. Рассчитать молярную массу эквивалента его нитрата и сульфата.
Ответ: 71 г/моль; 57 г/моль.
2.2. Молярная масса эквивалента карбоната некоторого металла составляет 74 г/моль. Определить молярные массы эквивалентов этого металла и его оксида.
Ответ: 44 г/моль; 52 г/моль.
2.3. Рассчитать объём 1 моля эквивалента сероводорода (н.у.), который окисляется до оксида серы (IV).
2.4. Определить молярную массу эквивалента Ni(OH)Cl в реакциях:
Ni(OH)Cl + H2S = NiS + HCl + H2O;
Ni(OH)Cl + NaOH = Ni(OH)2 + NaCl.
Ответ: 55,6 г/моль; 111,2 г/моль.
2.5. При взаимодействии 4,8 г неизвестного металла и 13 г цинка с соляной кислотой выделяется одинаковый объём водорода. Вычислить молярные массы эквивалентов металла, его оксида и его хлорида.
Ответ: МЭ(металла)=12 г/моль; МЭ(оксида)=20 г/моль, МЭ(хлорида)=47,5 г/моль.
2.6. Рассчитать молярные массы эквивалентов металла и его гидроксида, если хлорид этого металла содержит 79,7 мас.% хлора, а молярная масса эквивалента хлора равна 35,5 г/моль.
Ответ: МЭ(металла)=9 г/моль; МЭ(оксида)=26 г/моль.
2.7. Какой объём 0,6 М раствора H2O2 пойдёт на окисление 150 мл 2н. раствора FeSO4 в реакции:
H2O2 + 2 FeSO4 + H2SO4 = Fe2(SO4)3 + 2 H2O.
2.8. Определить объём хлора (н.у), необходимый для окисления 100 мл 0,5н раствора K2MnO4.
2.9. 0,66 г кислоты требуются для нейтрализации 10 мл 1М раствора КОН. Найти молярные массы эквивалентов кислоты и ее кальциевой соли в обменной реакции.
Ответ: МЭ(кислоты)=66 г/моль; МЭ(соли)=85 г/моль.
2.10. Бромид металла в результате обменной реакции полностью переведен в сульфат, при этом масса уменьшилась в 1,47 раз. Найти молярную массу эквивалента металла. Определить какой это металл.
Ответ: МЭ(металла)=20 г/моль; Са.