Определите массовые доли элементов в ортофосфорной кислоте…
Задание:
Определите массовые доли элементов в ортофосфорной кислоте.
Решение:
M(H3PO4) = 3 · M(H) + M(P) + 4 · M(O) = 3 · 1 + 31 + 4 · 16 = 98 г/моль.
ω(Н) = 3 · M(H) / M(H3PO4) = 3 · 1 / 98= 0,0306 (3,06%);
ω(Р) = M(P) / M(H3PO4) = 31 / 98 = 0,3163 (31,63%);
ω(О) = 4 · M(O) / M(H3PO4) = 4 · 16 / 98 = 0,6531 (65,31%).
Ответ: ω(Н) = 3,06%; ω(Р) = 31,63%; ω(О) = 65,31%
поделиться знаниями или
запомнить страничку
- Все категории
-
экономические
43,662 -
гуманитарные
33,654 -
юридические
17,917 -
школьный раздел
611,985 -
разное
16,906
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Для начала, из таблицы Менделеева берем значения масс атомов, каждого из элементов в соединении.
Масса атома Н равна 1 грамм.
Масса атома Р равна 31 грамм.
Масса атома О равна 16 грамм.
А теперь вычислим молекулярную массу Н3 РО4.
Mr (H3PO4) = 1*3+31*1+4*16=3+31+64=98 грамм.
По формуле массовой доли, найдем массовою долю каждого из элементов.
Формула массовой доли W (X) = m (x) * 100%/Mr
Подставим значения.
W (H) = 3*100%/98=3.06%
W (P) = 31*100%/98=31,6%
W (O) = 64*100%/98=65,34%
Ответ: массовая доля водорода в Н3 РО4 равна 3.06%, массовая доля фосфора в Н3 РО4 равна 31.6% и массовая доля кислорода в Н3 РО4 равна 65.34%.
Главная
-
- 0
-
?
Елисей Асхатов
Вопрос задан 1 октября 2019 в
5 — 9 классы,
Химия.
-
Комментариев (0)
Добавить
Отмена
1 Ответ (-а, -ов)
- По голосам
- По дате
-
- 0
-
Mr(H3PO4)=3*1+31+4*16=98
W(H)=3/98=0.031=3.1%
W(P)=31/98=0.316=31.6%
W(O)=64/98=0.653=65.3%
Отмена
Ксения Абаквмова
Отвечено 1 октября 2019
-
Комментариев (0)
Добавить
Отмена
Ваш ответ
Фосфорная кислота
H3PO4
1. Из Периодической таблицы имени Д. И. Менделеева выписываем значения относительных масс атомов элементов, входящих в состав фосфорной кислоты
Ar(H)=1
Ar(P)=31
Ar(O)=16
2. Вычисляем относительную атомную массу соединения
Mr(H3PO4) = 3·Ar(H) + Ar(P) + 4·Ar(O) = 3·1 + 31 + 4·16 = 98
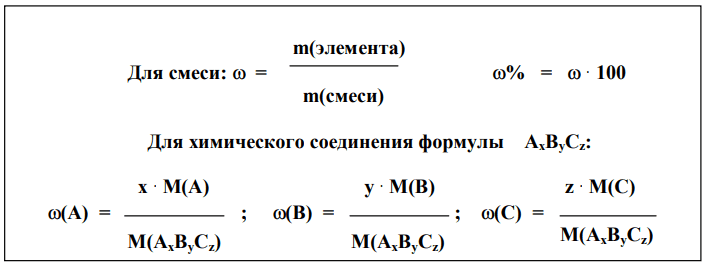
3. Вычисляем массовые доли элементов по формуле:
w(элемента) = (n· Ar(элемента) · 100%) / Mr(вещества)
w(H) = n(H)·Ar(H)·100% / Mr(H3PO4) = 3·1·100% / 98 = 3,06%
w(P) = n(P)·Ar(P)·100% / Mr(H3PO4) = 1·31·100% / 98 = 31,63%
w(O) = n(O)·Ar(O)·100% / Mr(H3PO4) = 4·16·100% / 98 = 65,31%
Сумма значений массовых долей всех элементов должна составить 100% w(H) + w(P) + w(O) = 100%
Подставляем значения,
3,06% + 31,63% + 65,31% = 100%
Таким образом, массовые доли элементов в фосфорной кислоте вычислены правильно.
w%(H)
w%(P)
w%(O)
Ответ:
w(H) = 3,06%
w(P) = 31,63%
w(O) = 65,31%