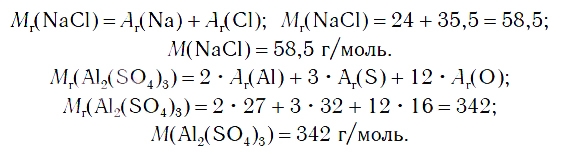В уроке 25 «Соли» из курса «Химия для чайников» узнаем, как правильно называть соли, их состав и научимся составлять химические формулы солей.
Как отмечалось в предыдущем уроке, в реакциях кислот с металлами выделяется простое вещество водород Н2. Кроме водорода, образуются и сложные вещества: ZnCl2, MgSO4 и др. Это представители класса широко распространенных в химии соединений — солей (рис. 102).
Здесь же мы рассмотрим состав солей, научимся составлять их формулы, узнаем, как называть соли.
Cостав солей
Сравним формулы кислот HCl и H2SO4 c формулами солей ZnCl2 и FeSO4. Мы видим, что в этих формулах одинаковые кислотные остатки Cl(I) и SO4(II). Но в молекулах кислот они соединены с атомами водорода Н, а в формульных единицах солей — с атомами цинка Zn и железа Fe. Значит, эти и другие соли можно рассматривать как продукты замещения атомов водорода в молекулах кислот на атомы металлов. Вещества, подобные ZnCl2 и FeSO4, относят к классу солей.
Соли — это сложные вещества, состоящие из атомов металлов и кислотных остатков.
В солях кислотные остатки соединяются с атомами металлов в соответствии с их валентностью. Для составления химической формулы соли необходимо знать валентность атома металла и валентность кислотного остатка. При этом пользуются тем же правилом, что и при составлении формул бинарных соединений. Для солей это правило следующее: сумма единиц валентности всех атомов металла должна быть равна сумме единиц валентности всех кислотных остатков.
Для примера составим формулу соли, в которую входят атомы кальция и кислотный остаток фосфорной кислоты PO4(III). Кальций проявляет постоянную валентность II, а валентность кислотного остатка PO4 равна III.
Названия солей
Соли образованы атомами разных металлов и различными кислотными остатками. Поэтому состав солей самый разнообразный. Давайте научимся давать им правильные названия.
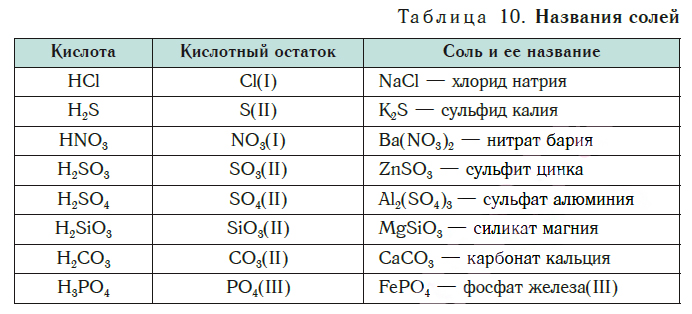
Название соли состоит из названия кислотного остатка и названия металла в родительном падеже. Например, соль состава NaCl называют «хлорид натрия».
Если входящий в формульную единицу соли атом металла имеет переменную валентность, то она указывается римской цифрой в круглых скобках после его названия. Так, соль FeCl3 называют «хлорид железа(III)», а cоль FeCl2 — «хлорид железа(II)».
В таблице 10 приведены названия некоторых солей.
Соли — это вещества немолекулярного строения. Поэтому их состав выражают с помощью формульных единиц. В них отражено соотношение атомов металлов и кислотных остатков. Например, в формульной единице NaCl на один атом Na приходится один кислотный остаток Cl.
По химической формуле соли можно вычислить ее относительную формульную массу Mr, а также молярную массу M, например:
К солям относится не только поваренная соль (NaCl), но и мел, мрамор (СаСО3), сода (Na2CO3), марганцовка (KMnO4) и др.
Краткие выводы урока:
- Соли — сложные вещества, которые состоят из атомов металлов и кислотных остатков.
- Соли образуются при замещении атомов водорода в молекулах кислот на атомы металлов.
- Соли — вещества немолекулярного строения.
Надеюсь урок 25 «Соли» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Пожалуйста, используйте таблицу Растворимость оснований и солей в воде (она на обложке в конце). По горизонтали записаны катионы (частицы с зарядом +) и по вертикали анионы (частицы с зарядом -).
Aнионы, за исключением первого группы OH⁻, и будут кислотные остатки.
Кислотный остаток он в составе кислот:
Например, HCI соляная кислота, H⁺CI⁻ ион хлора кислотный остаток.
H₂SO₄ серная кислота H₂⁺SO₄²⁻
Кислотный остаток он в составе солей:Теперь берете катион с зарядом + и соединяете с группой OH⁻ .
Заметьте для себя, что молукула соли, которая у Вас получится электронейтральна равна 0, то есть число положительных зарядов + должно равняться числу отрицательных зарядов -.
K⁺CI⁻ хлорид кали
NH₄⁺CI⁻хлорид аммония
(NH₄)₂⁺SO₄²⁻ сульфат аммония
(NH₄)₃⁺PO₄³⁻ фосфат аммония
Ca²⁺CI₂⁻ хлорид кальция
Ca²⁺SO₄²⁺ сульфат кальция
Ca₃²⁺(PO₄)₂³⁻ фосфат кальция
Кислотный остаток
- Кислотный остаток
-
Кислотный остаток — это анион, который является второй частью формулы сложного химического соединения. Они способны замещать определенное количество атомов или групп атомов. Ни у одного кислотного остатка нет свободных реакциоспособных электронов. Как правило, кислотный остаток состоит из атомов неметаллов.
- В кислотах — это атомы без водорода (H2SO4: H (водород) — катион, SO4 (сульфат) — кислотный остаток).
- В солях — атомы без металла (Na2CO3: Na (натрий) — металл, CO3 (карбонат)- кислотный остаток).
- В гидроксидах (основаниях) — атомы гидроксильной группы (OH) (Mg(OH)2: Mg (магний — металл, (OH)2 — атомы гидроксильной группы. Валентность OH всегда равна I.
Таблица самых распространенных кислотных остатков
Кислотный остаток Валентность Название Тривиальное название кислоты -Cl I хлорид соляная кислота -NO3 I нитрат азотная кислота -SO4 II сульфат серная кислота -SO3 II сульфит сернистая кислота -S II сульфид сероводородная кислота -SiO3 II силикат кремниевая кислота -CO3 II карбонат угольная кислота -PO4 III ортофосфат ортофосфатная кислота -NO2 I нитрит нитритная кислота -F I фторид плавиковая кислота -I I иодид иодидная кислота -Br I бромид бромидная кислота
Wikimedia Foundation.
2010.
Полезное
Смотреть что такое «Кислотный остаток» в других словарях:
-
кислотный остаток — — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN acid residue … Справочник технического переводчика
-
кислотный остаток — rūgšties liekana statusas T sritis chemija apibrėžtis Rūgšties anijonas. atitikmenys: angl. acid residue rus. кислотный остаток … Chemijos terminų aiškinamasis žodynas
-
кислотный остаток — кислотный радикал … Cловарь химических синонимов I
-
кислотный радикал — кислотный остаток … Cловарь химических синонимов I
-
Эфиры сложные — (хим.) представляют собой сочетания спиртов с кислотами, происходящие путем выделения воды за счет водных остатков этих соединений. Названия [В немецкой химической литературе сложные Э. весьма целесообразно названы, по предложению Гмелина, особым … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
-
Число координатное — химических соединений — Термин введен в науку А. Вернером, который предполагает, что ему удалось открыть закономерность, определяющую состав гидратов, аммиакатов (ср. Кобальтиаковые соединения), двойных (и простых, кислородсодержащих) солей и вообще неорганических и… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
-
Анион — Анион отрицательно заряженный ион. Характеризуется величиной отрицательного электрического заряда; например, Cl− однозарядный анион, а SO42− двузарядный анион. В электрическом поле анионы перемещаются к положительному… … Википедия
-
диазосоединения — органические соединения общей формулы RN2 (алифатические диазосоединения; R алкил) или ArN2X (ароматические диазосоединения; Ar арил, Х гидроксильная группа или кислотный остаток), из которых наиболее важны последние соли диазония.… … Энциклопедический словарь
-
ртутьорганические соединения — содержат в молекуле атом ртути, непосредственно связанный с углеродом. Известны ртутьорганические соединения типа R2Hg и RHgX, где R органический радикал, Х галоген, ОН, кислотный остаток. Применяются в органическом синтезе, как фунгициды.… … Энциклопедический словарь
-
соли — продукты замещения атомов водорода кислоты на металл или групп ОН основания на кислотный остаток. При полном замещении образуются средние, или нормальные, соли (NaCl, K2SO4 и др.), при неполном замещении атомов Н кислые (напр., NaHCO3), неполном … Энциклопедический словарь
|
Формула кислоты всегда начинается с «H». Например, H2SO4(серная кислота), HCl(соляная кислота). Если видишь первую «H», значит, это кислота. Основания имеют гидроксо группу OH в формуле Например, NaOH(гидроксид натрия), Ca(OH)2 (гидроксид кальция). В формуле солей первая скажем так буква — металл или неметалл ПС. Например, NaCl(хлорид натрия), Na3PO4 Еще раз: если первая «Н», значит, кислота. Если есть «ОН», значит, основание. Если первый металл или неметалл, значит, соль автор вопроса выбрал этот ответ лучшим Krustall 7 месяцев назад Это вопрос из курса школьной химии, достаточно простой, но требующий разъяснения и запоминания. Кислоты — это то, что в растворе диссоциирует только на катионы Н+ и анионы кислотного остатка. Основания — это то, что в растворе диссоциируют на катионы металлов и гидроксид-анионы ОН-. Соли — электролиты, который диссоциируют на катионы металла, анионы кислотного остатка, а еще в некоторых случаях ЕЩЁ на Н+ (кислые соли): NaHCO3 и ОН- (Основные соли) Fe(OH)Cl2. Ну и добавим нужную расшифровку про Оксиды, это такие бинарные (то есть, два элемента) соединения, в которых один из элементов — это всегда кислород. Sagavaha 2 года назад Мне очень нравятся простейшие пояснения из видео на вот этом канале — реально за несколько минут химия становится понятнее, чем после длинных школьных уроков. Если же вам нужно именно текстовое пояснение — то кратко это можно описать вот так: Если же нужно, чтоб было ещё и определение каждой группы — тогда ниже более развёрнуто, но и сложнее для понимания КорнетОболенский 5 месяцев назад Вопрос из школьного курса химии. Но попробуем его соотнести с обыденной жизнью. Сначала рассмотрим химические формулы кислот, оснований и солей на примерах:
Видим, что во всех химических формулах кислот на первом месте стоит первый элемент таблицы Менделеева — водород. При этом всё, что стоит после водорода, является кислотным остатком.
Химические формулы оснований обязательно содержат в себе элемент (ОН) — соединение кислорода и водорода. Вспомним, что многие химические вещества, содержащие в своем составе атомы кислорода, называются оксидами, а водорода — гидридами. Признак основания — элемент (ОН) содержит в себе атомы кислорода и водорода одновременно. Поэтому второе название оснований — гидроксиды.
Несложно увидеть, что соли — ни что иное, как соединения атомов металлов и кислотных остатков. Т.е. Заменив в формуле кислоты водород металлом, получим ту или иную соль. Однако различить эти три разновидности химических веществ можно не только по формулам, но и на простых бытовых примерах. Уже из названия «кислота» следует, что на вкус она кислая (например, лимонная кислота, применяемая в кулинарии или муравьиная (это если запустить руку в лесной муравейник и лизнуть палец после этого) Основания — это всем известные вещества едкий натр (каустическая сода), гашеная известь. Соли — это огромное количество веществ, превышающее количество кислот и гидроксидов вместе взятых. Классическим примером соли является поваренная соль NaCl на кухонном столе или неорганические удобрения для сада и огорода (калийная селитра, сульфат аммония и пр.) G11111 4 месяца назад Химия достаточно простая наука, но это становится понятно не сразу. Когда я учился в школе долго не мог врубиться в смысл, но потом в голове что то щелкнуло и все стало на свои места — формулы и определения стали понятны буквально с одного взгляда. Сейчас это за ненадобностью снова ушло куда то в сторону, но попробую что то вспомнить. В формулах кислот всегда впереди находится водород (Н) Основания определяются по признакам:
Химические формулы соли строятся с учетом валентностей металла и кислотного остатка. Можно сказать, что все соли это ионные соединения, в солях связаны между собой ионы металла и ионы кислотных остатков. Долинн 5 месяцев назад Соль и кислота очень похожи, только у кислоты в составе всегда есть водород, и в формуле водород пишут первым (символ — Н), а у соли на его месте металл. HCl — это соляная кислота. NaCl — это хлорид натрия (поваренная соль). А в основании всегда будет ОН. Так что, если у нас есть соединение, про которое мы точно знаем, что это либо кислота, либо соль, либо основание, смотрим, что идет первым. Водород? Кислота. H2SO4 — серная кислота Далее смотрим, есть ли в завершении формулы ОН (произносится о-аш). Есть? Это основание. NaOH — едкий натр. Если в формуле первым идет металл, то это соль. MgSO4 — соль, сульфат магния. Утренняя роса 2 года назад Основания, кислоты и соли — это сложные вещества, образованные катионами и анионами. Сравним кислоты и соли: И те и другие имеют в своем составе кислотные остатки. В этом их сходство. Различие солей и кислот в том, что в кислотах кислотный остаток соединен с катионами водорода, а в солях кислотный остаток соединен с катионами металла. Например: H2SO4 (серная кислота) и CaSO4 (сульфат кальция — соль), кислотный остаток одинаковый, но в кислоте — водород, а в соли — металл кальций. Сравним соли и основания: Соль состоит из катионов металла и анионов кислотного остатка — CaSO4. Основание состоит из катионов металла и анионов гидроксогрупп (-ОН)- Ca(OH)2 Кислоты и основания, на первый взгляд, сравнить нельзя, но надо учесть, что и кислоты и основания — это гидроксиды (гидр-оксиды, то есть оксид с водой). Кислоты — это гидроксиды неметаллов, а основания — это гидроксиды металлов. Кислота + основание = соль + вода (реакция нейтрализации). SVFE48 4 месяца назад Основания, соли и кислоты можно различать по своим химическим свойствам. Основания — это вещества, которые обладают способностью отдавать протоны (положительно заряженные частицы). Они характеризуются также высокой pH (более 7). Соли — это вещества, образующиеся в результате реакции оснований и кислот. Они содержат ионы, но у них нет способности отдавать или принимать протоны. Кислоты — это вещества, которые обладают способностью принимать протоны. Они характеризуются низким pH (менее 7). Обычно они имеют кислый вкус и могут окислять металлы. В некоторых случаях можно различать основания, соли и кислоты также с помощью цветных индикаторов. Например, розовый цвет индикатора фенолофталеин указывает на присутствие основания, зеленый цвет индикатора метилового зеленого указывает на присутствие кислоты, а желтый цвет индикатора хлорофилла указывает на присутствие соли. Однако стоит помнить, что цветные индикаторы не всегда точно показывают наличие оснований, солей и кислот, поэтому лучше всего использовать их в сочетании с другими методами анализа. Степан БВ 3 месяца назад Основания, соли и кислоты можно различать по своей реакции с водой. Основания растворяются в воде и при добавлении индикатора (например, фенолфталеина) происходит появление розового цвета. Соли не растворяются в воде, но при добавлении индикатора появляется желтый цвет. Кислоты при добавлении индикатора происходит появление зеленого цвета. Также можно использовать тесты на рН, чтобы определить, какое вещество имеется в веществе. РН больше 7 означает, что это основание, РН меньше 7 означает, что это кислота. Rnd 3 месяца назад Химические реакции могут быть легко определены по первой букве в формуле вещества. Начинается ли она с «H»? Тогда это кислота, как в случае с серной кислотой (H2SO4) или соляной кислотой (HCl). Ищешь группу «OH»? Тогда это основание, как гидроксид натрия (NaOH) или гидроксид кальция (Ca(OH)2). Если же первый элемент — металл или неметалл, то это соль, как хлорид натрия (NaCl) или фосфат натрия (Na3PO4). Запомни это правило и определяй химические соединения с уверенностью! Знаете ответ? |